Clear Sky Science · fr
Un mécanisme intrinsèque aux tissus sensibilise les particules du VIH-1 aux réponses immunitaires innées déclenchées par les TLR
Comment nos tissus combattent discrètement le VIH
Le VIH fait généralement les gros titres pour sa capacité à neutraliser le système immunitaire, mais cette étude renverse la perspective : elle explore ce que font nos tissus pour riposter. Au cœur des ganglions lymphatiques et d’autres organes, cellules immunitaires et virus circulent au sein d’un maillage tridimensionnel de collagène et d’autres protéines. Ce travail montre que ce maillage n’est pas un simple échafaudage passif. Il affaiblit activement la capacité du VIH à infecter les cellules tout en rendant simultanément le virus plus visible pour nos défenses immunitaires innées.
Le monde caché entre les cellules
Dans notre corps, les cellules sont entourées d’un réseau complexe appelé matrice extracellulaire, constitué en grande partie de fibres de collagène. Les chercheurs ont fabriqué des gels « de type tissulaire » simplifiés composés de différents types de collagène pour reproduire cet environnement. Ils ont laissé des particules de VIH se déplacer dans ces gels tridimensionnels et les ont comparées à des virus conservés en culture liquide ordinaire. Ils ont constaté qu’un bref contact physique avec les fibres de collagène suffisait à réduire fortement la capacité du virus à infecter de nouvelles cellules, phénomène qu’ils qualifient de restriction extracellulaire de l’infectiosité des virions. Cet effet survient rapidement, dépend d’un contact direct avec la matrice, et a été observé pour différentes souches de VIH et plusieurs matériaux riches en collagène, mais pas dans des gels non adhésifs comme l’agarose.
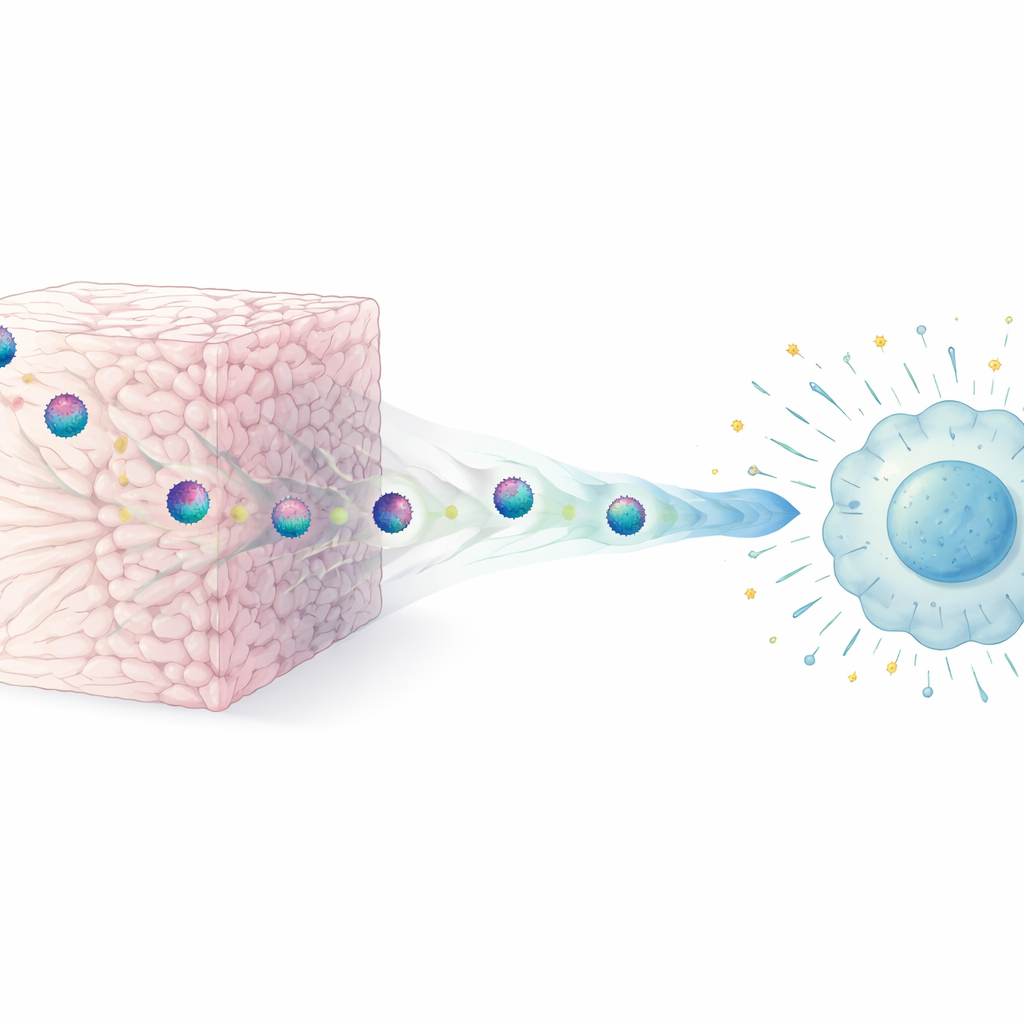
Comment le collagène dompte le virus
Une crainte évidente était que le collagène détruisît simplement les particules virales. Grâce à la microscopie électronique à haute résolution, l’équipe a montré que ce n’était pas le cas : les particules de VIH sortant des gels de collagène semblaient structurellement normales, avec des membranes et des noyaux intacts. Le collagène n’enlevait pas non plus les protéines de surface du virus. La modification clé est d’ordre fonctionnel. Les virus exposés au collagène se fixaient encore aux cellules cibles, mais fusionnaient beaucoup moins efficacement avec elles, ce qui signifie que l’entrée dans la cellule était bloquée à une toute première étape. Des nanofibres artificielles « boostant l’infectiosité » et favorisant la fusion virale ont pu restaurer l’infectiosité du VIH traité au collagène, renforçant l’idée que la matrice gêne principalement le processus de fusion plutôt que d’endommager globalement le virus.
De particules silencieuses à des alertes immunitaires
La découverte la plus surprenante est que le contact avec le collagène ne se contente pas d’atténuer l’infection : il transforme aussi le VIH en un signal d’alarme plus puissant pour les cellules immunitaires innées, en particulier les macrophages dérivés de monocytes. Lorsque ces cellules étaient exposées au VIH ayant traversé du collagène, elles produisaient beaucoup plus de molécules inflammatoires telles que IL-6, IL-8 et TNF que lorsqu’elles rencontraient le virus ordinaire, même si le niveau d’infection réel n’était réduit que modestement. Le profilage détaillé de l’expression génique a montré que les macrophages activés par le virus « prémuni » par le collagène déclenchaient un vaste programme antiviral, incluant de nombreux facteurs de restriction connus et des signaux d’alerte qui aident à coordonner des réponses immunitaires plus larges.
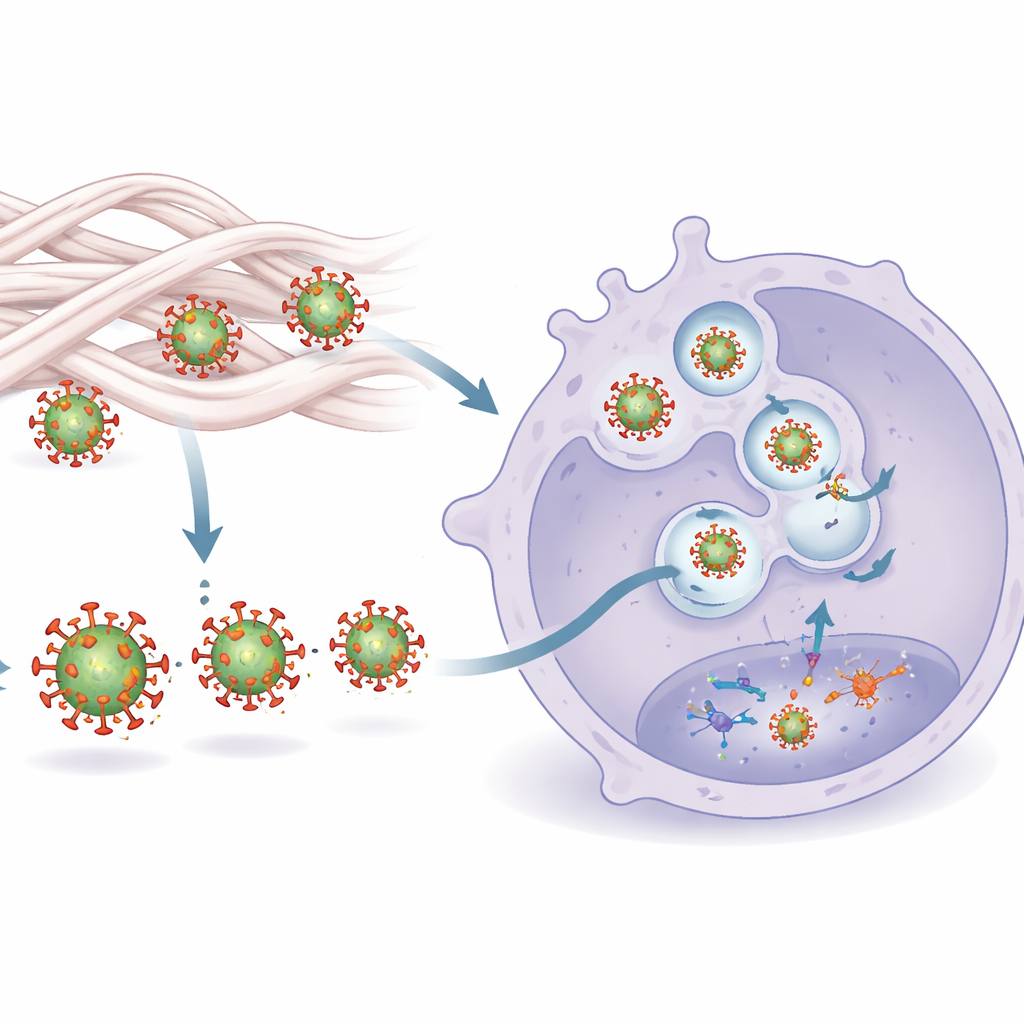
Comment la détection est activée
L’étude a retracé cette sensibilité accrue à un mécanisme en deux volets. D’une part, le contact avec le collagène modifie subtilement la conformation de la protéine d’enveloppe externe du VIH, Env. Ces changements de forme rendent Env plus aisément reconnaissable par un capteur des macrophages, le récepteur de type Toll 2 (TLR2). D’autre part, une fois reconnu à la surface, le virus est plus efficacement acheminé vers des compartiments internes contenant un autre capteur, TLR8, qui détecte le génome ARN du virus. Le blocage de TLR2 ou de TLR8 supprimait la flambée de cytokines induite par le collagène, montrant que les deux signaux sont nécessaires. La microscopie a confirmé que les virus traités au collagène se liaient plus fortement à une forme soluble de TLR2 et étaient plus susceptibles d’aboutir dans des endosomes riches en TLR8, où ils pouvaient déclencher une cascade antivirale robuste.
Pourquoi cela importe pour les personnes vivant avec le VIH
Pour un non-spécialiste, le message principal est que nos tissus ne sont pas un terrain neutre pendant l’infection par le VIH. Les mêmes fibres qui donnent leur structure aux organes peuvent handicaper directement la propagation du VIH et, en même temps, aider les cellules immunitaires à mieux reconnaître le virus. Cette défense « intrinsèque aux tissus » agit en dehors des cellules, en complétant les protéines antivirales mieux connues qui opèrent à l’intérieur d’elles. Le travail suggère aussi une arme à double tranchant : les mêmes signaux inflammatoires qui aident à contrôler le virus peuvent, à long terme, contribuer à la fibrose tissulaire et à l’inflammation chronique observées chez les personnes vivant avec le VIH. Comprendre comment la matrice extracellulaire module cet équilibre pourrait ouvrir de nouvelles voies pour renforcer l’immunité protectrice tout en limitant les dommages à long terme.
Citation: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
Mots-clés: Immunité innée contre le VIH, matrice extracellulaire, collagène et virus, récepteurs de type Toll, défense antivirale tissulaire