Clear Sky Science · tr
Dokuya özgü bir mekanizma HIV-1 partiküllerini TLR tetiklemeli doğuştan bağışıklık tepkilerine hassaslaştırıyor
Dokularımızın HIV ile Sessiz Mücadelesi
HIV genellikle bağışıklık sistemini nasıl devre dışı bıraktığıyla haber olur, fakat bu çalışma hikâyeyi tersine çeviriyor: dokularımızın kendilerinin nasıl karşı koyduğunu soruyor. Lenf düğümleri ve diğer organların derinliklerinde, bağışıklık hücreleri ve virüsler kolajen ve diğer proteinlerden oluşan üç boyutlu bir örgü içinde hareket eder. Bu çalışma bu örgünün yalnızca pasif bir iskelet olmadığını gösteriyor. Bunun yerine, HIV’in hücreleri enfekte etme yeteneğini aktif olarak zayıflatıyor ve aynı zamanda virüsü doğuştan gelen bağışıklık savunmalarımız için daha görünür hâle getiriyor.
Hücreler Arasındaki Gizli Dünya
Vücudumuzun içinde hücreler, büyük ölçüde kolajen liflerinden oluşan ekstrasellüler matriks adı verilen karmaşık bir ağla çevrilidir. Araştırmacılar bu ortamı taklit etmek için farklı tip kolajenlerden oluşan basitleştirilmiş “doku benzeri” jel sistemleri oluşturdular. Ardından HIV partiküllerinin bu üç boyutlu jeller içinde hareket etmesine izin verdiler ve bunları sıradan sıvı kültürde tutulan virüslerle karşılaştırdılar. Kısa süreli, fiziksel temasın virüsün yeni hücreleri enfekte etme yeteneğini keskin bir şekilde azaltmak için yeterli olduğunu buldular; araştırmacılar bu olguyu virion enfektivititesinin ekstrasellüler kısıtlanması olarak adlandırıyor. Bu etki hızla ortaya çıktı, matriksle doğrudan temele bağlıydı ve farklı HIV suşları ve çeşitli kolajen açısından zengin materyallerde görüldü; ancak agaroz gibi yapışmaz jellerde görülmedi.
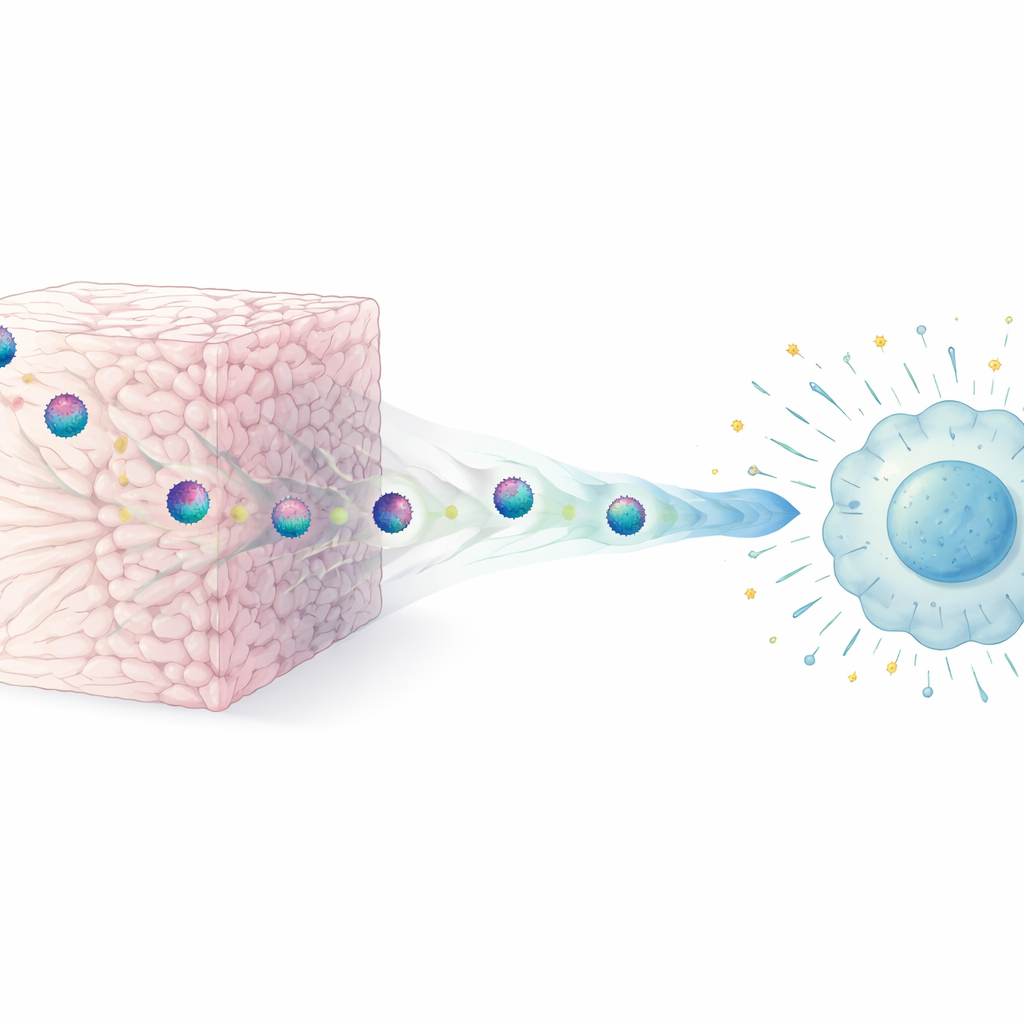
Kolajen Virüsü Nasıl Sakinleştiriyor
Akla gelen ilk kaygı kolajenin virüs partiküllerini basitçe yok ediyor olmasıydı. Yüksek çözünürlüklü elektron mikroskobu kullanarak ekip bunun böyle olmadığını gösterdi: kolajenden çıkan HIV partikülleri yapısal olarak normal göründü; zarları ve çekirdekleri sağlamdı. Kolajen ayrıca virüsün yüzey proteinlerini de koparmıyordu. Bunun yerine kilit değişiklik işlevseldi. Kolajene maruz kalan virüsler hâlâ hedef hücrelere bağlandı, fakat onlarla füzyonları çok daha az verimliydi; bu da hücre içine girişin çok erken bir adımda engellendiği anlamına geliyordu. Virüslerin hücrelerle füzyonuna yardımcı olan yapay “enfektivite arttırıcı” nanofiberler, kolajenle muamele edilmiş HIV’in enfektifliğini geri getirebildi; bu da matrisin virüsü bütünüyle zarar vermekten ziyade esas olarak füzyon sürecine müdahale ettiği fikrini güçlendiriyor.
Sessiz Partiküllerden Bağışıklık Alarmlarına
En şaşırtıcı bulgu, kolajen temasının yalnızca enfeksiyonu köreltememesi değil, aynı zamanda HIV’i doğuştan bağışıklık hücreleri, özellikle monosit kaynaklı makrofajlar için daha güçlü bir alarm sinyaline dönüştürmesiydi. Bu hücreler kolajene maruz kalmış HIV ile karşılaştığında, gerçek enfeksiyon düzeyleri yalnızca kısmen azalmış olsa da IL-6, IL-8 ve TNF gibi çok daha fazla inflamatuar molekül ürettiler. Ayrıntılı gen ifade profillemesi, kolajenle primlenmiş virüs tarafından tetiklenen makrofajların geniş bir antiviral programı açtığını, bunun içinde birçok bilinen bağışıklık kısıtlama faktörü ve daha geniş bağışıklık yanıtlarını koordine etmeye yardımcı uyarı sinyalleri olduğunu gösterdi.
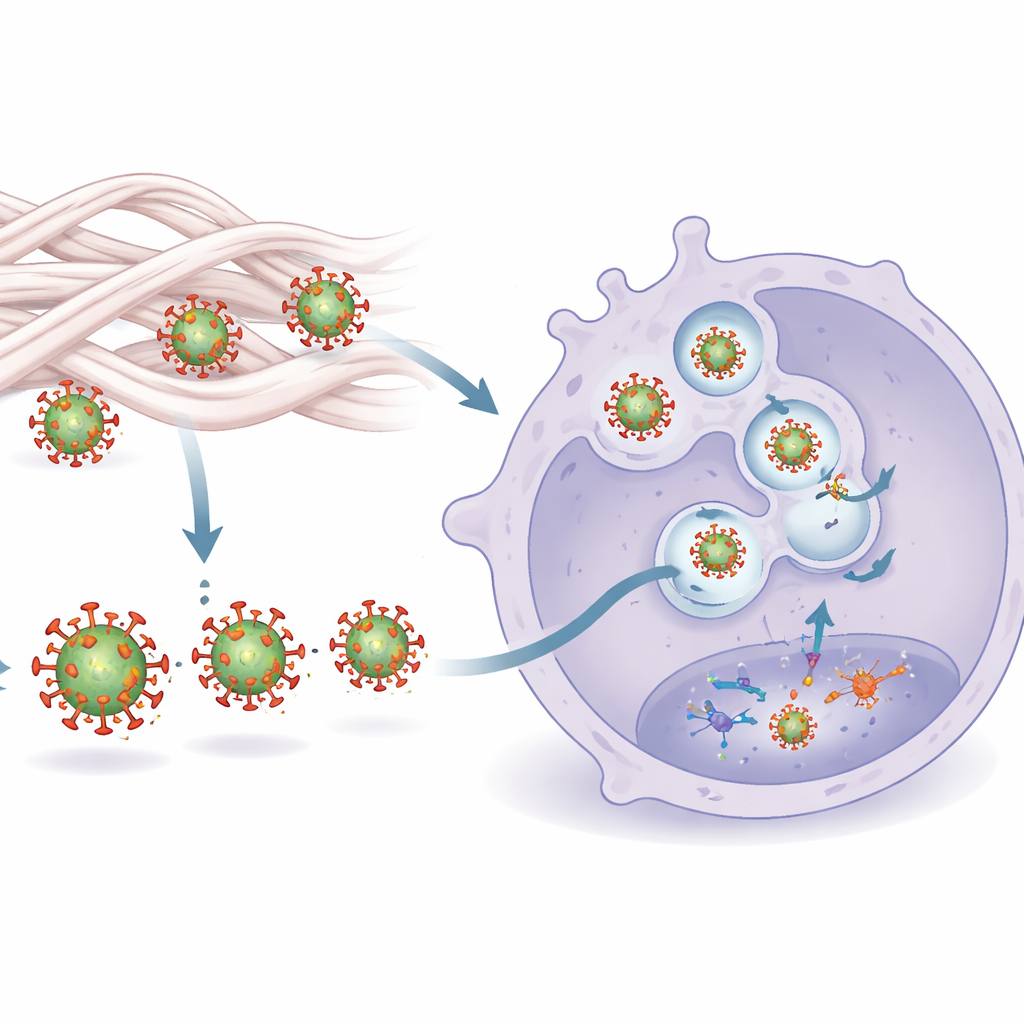
Algılama Nasıl Açığa Çıkıyor
Çalışma bu artmış algılamayı iki parçalı bir mekanizmaya dayandırdı. Birincisi, kolajenle temas HIV’in dış kapak proteini Env’i ince şekilde yeniden şekillendiriyor. Bu şekil değişimleri Env’in makrofajlardaki bir sensör olan Toll-like reseptör 2 (TLR2) tarafından daha kolay yakalanmasını sağlıyor. İkincisi, yüzeyde tanındıktan sonra virüs daha verimli biçimde başka bir sensör olan TLR8’in bulunduğu iç bölmelere gönderiliyor; TLR8 virüsün RNA genomunu algılıyor. TLR2 veya TLR8’in engellenmesi kolajen kaynaklı sitokin artışını durdurdu; bu da her iki sinyalin de gerekli olduğunu gösteriyor. Mikroskopi, kolajenle muamele edilmiş virüslerin çözünür bir TLR2 versiyonuna daha güçlü bağlandığını ve TLR8 açısından zengin endozomlarda sonlanma olasılığının daha yüksek olduğunu doğruladı; bu ortamda güçlü bir antiviral kaskad tetiklenebiliyor.
HIV ile Yaşayan İnsanlar İçin Neden Önemli
Halk için temel mesaj şudur: dokularımız HIV enfeksiyonu sırasında tarafsız zemin değiller. Organlara yapı veren aynı lifler HIV’in yayılma yeteneğini doğrudan zayıflatabilir ve aynı zamanda bağışıklık hücrelerinin virüsü daha net tanımasına yardımcı olabilir. Bu “dokuya özgü” savunma hücre dışı çalışarak hücre içindeki daha iyi bilinen antiviral proteinleri tamamlıyor. Çalışma ayrıca çift yönlü bir bıçağa işaret ediyor: virüsü kontrol etmeye yardımcı olan aynı inflamatuar sinyaller zamanla doku skarlaşmasına ve HIV ile yaşayan kişilerde görülen kronik inflamasyona katkıda bulunabilir. Ekstrasellüler matriksin bu dengeyi nasıl ayarladığını anlamak, uzun vadeli hasarı sınırlarken koruyucu bağışıklığı güçlendirmek için yeni yollar açabilir.
Atıf: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
Anahtar kelimeler: HIV doğuştan bağışıklık, ekstrasellüler matriks, kolajen ve virüs, toll-benzeri reseptörler, doku antiviral savunması