Clear Sky Science · nl
Een weefsel-intrinsiek mechanisme maakt HIV-1-deeltjes gevoeliger voor TLR-geïnduceerde aangeboren immuunreacties
Hoe onze weefsels stilletjes tegen HIV vechten
HIV haalt meestal de krantenkoppen vanwege hoe het het immuunsysteem uitschakelt, maar deze studie keert het verhaal om: ze onderzoekt wat onze weefsels zelf doen om terug te slaan. Diep in lymfeklieren en andere organen bewegen immuuncellen en virussen door een driedimensionaal netwerk van collageen en andere eiwitten. Dit werk toont aan dat dat netwerk geen passief geraamte is. In plaats daarvan verzwakt het actief het vermogen van HIV om cellen te infecteren en maakt het het virus tegelijk zichtbaarder voor onze aangeboren immuunverdediging.
De verborgen wereld tussen cellen
In ons lichaam worden cellen omgeven door een complex web — de extracellulaire matrix — dat grotendeels uit collageendraden bestaat. De onderzoekers maakten vereenvoudigde ‘weefselachtige’ gels van verschillende typen collageen om deze omgeving na te bootsen. Ze lieten HIV-deeltjes door deze driedimensionale gels bewegen en vergeleken die met virus in gewone vloeibare cultuur. Ze ontdekten dat een korte, fysieke aanraking met collageendraden al voldoende was om de infectieuze kracht van het virus sterk te verminderen, een verschijnsel dat ze extracellular restriction of virion infectivity noemen. Dit effect trad snel op, hing af van direct contact met het matrixmateriaal en werd gezien bij verschillende HIV-stammen en meerdere collageenrijke materialen, maar niet in niet-klevende gels zoals agarose.
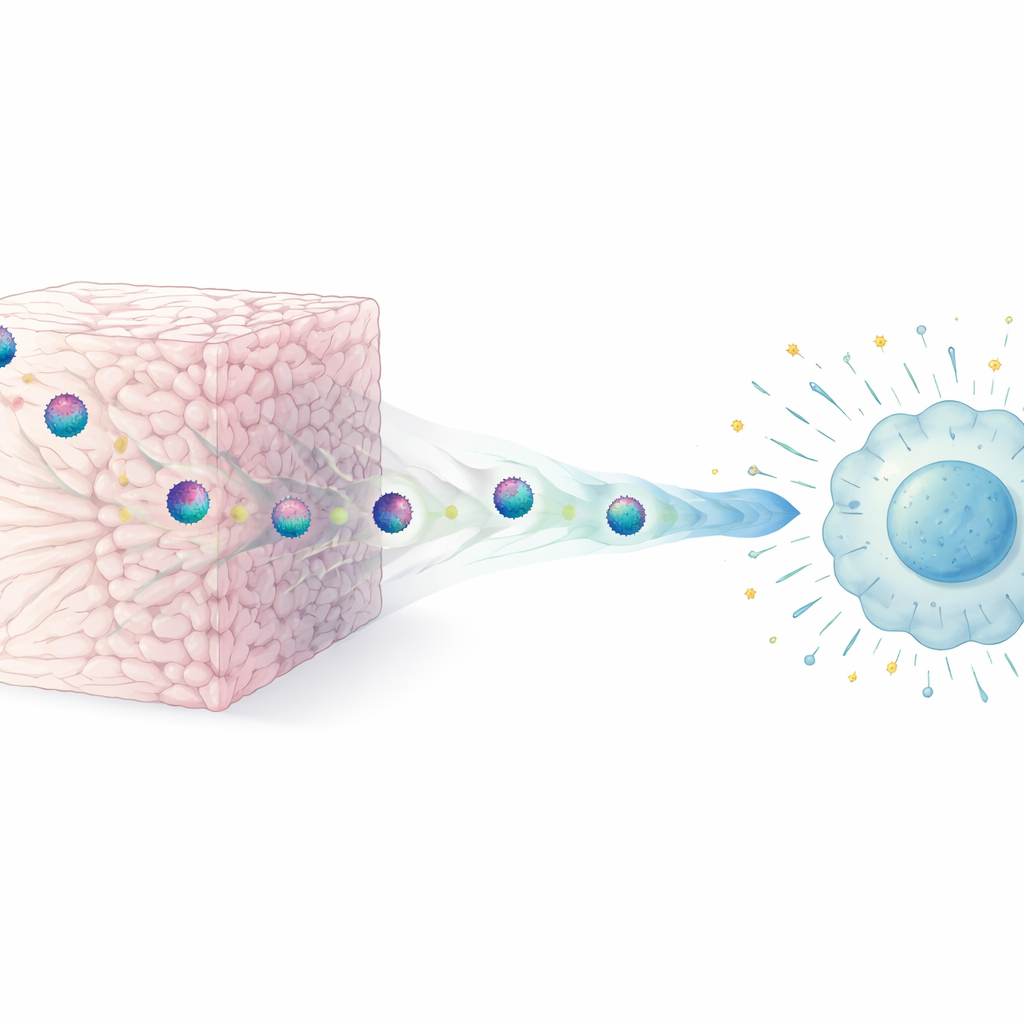
Hoe collageen het virus temt
Een voor de hand liggende zorg was dat collageen de virusdeeltjes simpelweg zou vernietigen. Met behulp van hoogresolutie-elektronenmicroscopie toonde het team aan dat dat niet het geval was: HIV-deeltjes die uit collageengels kwamen, zagen er structureel normaal uit, met intacte membranen en kernen. Collageen verwijderde ook niet de oppervlakte-eiwitten van het virus. In plaats daarvan was de cruciale verandering functioneel. Door collageen blootgestelde virussen hechtten nog steeds aan doelcellen, maar fuseerden veel minder efficiënt, wat betekent dat het binnendringen in de cel al in een vroeg stadium werd geblokkeerd. Kunstmatige ‘infectiviteit-verhogende’ nanovezels die virussen helpen te fuseren met cellen, konden de besmettelijkheid van collageen-behandeld HIV herstellen, wat de gedachte versterkt dat de matrix vooral het fusieproces verstoort in plaats van het virus als geheel te beschadigen.
Van stille deeltjes naar immuunalarmen
De meest verrassende bevinding was dat contact met collageen niet alleen de infectie dempte; het veranderde HIV ook in een sterker alarmsignaal voor aangeboren immuuncellen, met name monocyten-afgeleide macrofagen. Wanneer deze cellen werden blootgesteld aan collageen-ervaren HIV, produceerden ze veel meer ontstekingsmoleculen zoals IL-6, IL-8 en TNF dan bij blootstelling aan gewoon virus, hoewel de daadwerkelijke infectieniveaus slechts matig verminderd waren. Gedetailleerde genexpressieprofilering toonde aan dat macrofagen die door collageen-primed virus werden geactiveerd, een breed antiviraal programma inschakelden, waaronder vele bekende immuunrestrictiefactoren en waarschuwingssignalen die helpen bredere immuunreacties te coördineren.
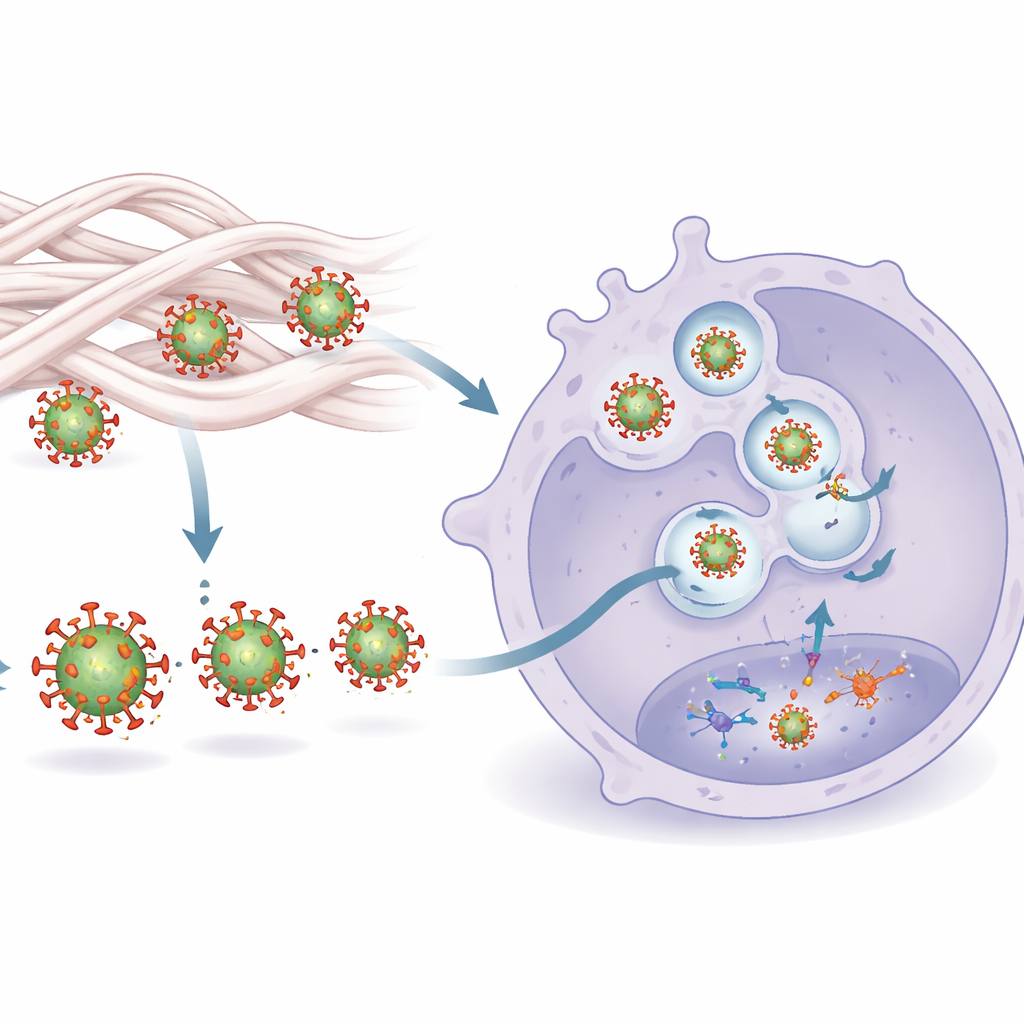
Hoe het waarnemen wordt aangezet
De studie traceerde deze verhoogde waarneming tot een tweedelig mechanisme. Ten eerste vormt contact met collageen het buitenste coat-eiwit van HIV, Env, subtiel om. Deze vormveranderingen maken Env gemakkelijker vatbaar voor een sensor op macrofagen, Toll-like receptor 2 (TLR2). Ten tweede, eenmaal herkend aan het oppervlak, wordt het virus efficiënter naar interne compartimenten getransporteerd die een andere sensor bevatten, TLR8, die het RNA-genoom van het virus detecteert. Blokkeren van ofwel TLR2 of TLR8 zette de collageen-geïnduceerde cytokinesurges uit, wat aantoont dat beide signalen nodig zijn. Microscopie bevestigde dat door collageen behandelde virussen sterker bonden aan een oplosbare versie van TLR2 en vaker in TLR8-rijke endosomen terechtkwamen, waar ze een robuuste antivirale cascade konden activeren.
Waarom dit belangrijk is voor mensen met HIV
Voor een lekenpubliek is de kernboodschap dat onze weefsels geen neutraal terrein zijn tijdens HIV-infectie. De vezels die organen hun structuur geven, kunnen rechtstreeks het vermogen van HIV om zich te verspreiden belemmeren en tegelijk immuuncellen helpen het virus duidelijker te herkennen. Deze ‘weefsel-intrinsieke’ verdediging werkt buiten cellen en vult de beter bekende antivirale eiwitten binnenin aan. Het werk suggereert ook een tweesnijdend zwaard: dezelfde ontstekingssignalen die helpen het virus onder controle te houden, kunnen in de loop van de tijd bijdragen aan weefselverharding en chronische ontsteking die bij mensen met HIV wordt gezien. Inzicht in hoe de extracellulaire matrix dit evenwicht afstemt, zou nieuwe manieren kunnen openen om beschermende immuniteit te versterken en tegelijk langdurige schade te beperken.
Bronvermelding: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
Trefwoorden: HIV aangeboren immuniteit, extracellulaire matrix, collageen en virus, toll-like receptoren, weefsel antivirale verdediging