Clear Sky Science · de
Ein gewebe‑intrinsischer Mechanismus macht HIV‑1‑Partikel empfindlicher für TLR‑ausgelöste angeborene Immunantworten
Wie unser Gewebe heimlich gegen HIV kämpft
In den Medien wird HIV meist dafür bekannt, wie es das Immunsystem schwächt. Diese Studie dreht die Perspektive um: Sie fragt, was unser Gewebe selbst unternimmt, um sich zur Wehr zu setzen. Tief in Lymphknoten und anderen Organen bewegen sich Immunzellen und Viren durch ein dreidimensionales Geflecht aus Kollagen und anderen Proteinen. Diese Arbeit zeigt, dass dieses Geflecht nicht nur passives Gerüst ist. Stattdessen schwächt es aktiv die Fähigkeit von HIV, Zellen zu infizieren, und macht das Virus gleichzeitig für unsere angeborenen Abwehrmechanismen sichtbarer.
Die verborgene Welt zwischen den Zellen
In unserem Körper sind Zellen von einem komplexen Netz umgeben, der sogenannten extrazellulären Matrix, die überwiegend aus Kollagenfasern besteht. Die Forscher stellten vereinfachte „gewebeähnliche“ Gele aus verschiedenen Kollagentypen her, um diese Umgebung nachzuahmen. Sie ließen HIV‑Partikel durch diese dreidimensionalen Gele wandern und verglichen sie mit Virus in gewöhnlichen Flüssigkulturen. Schon kurzzeitiger physischer Kontakt mit Kollagenfasern reichte aus, um die Infektiosität des Virus deutlich zu verringern — ein Phänomen, das sie als extrazelluläre Einschränkung der Vireninfektiosität bezeichnen. Dieser Effekt trat schnell auf, hing von direktem Kontakt mit der Matrix ab und war bei verschiedenen HIV‑Stämmen und mehreren kollagenreichen Materialien zu beobachten, jedoch nicht in nicht‑adhäsiven Gelen wie Agarose.
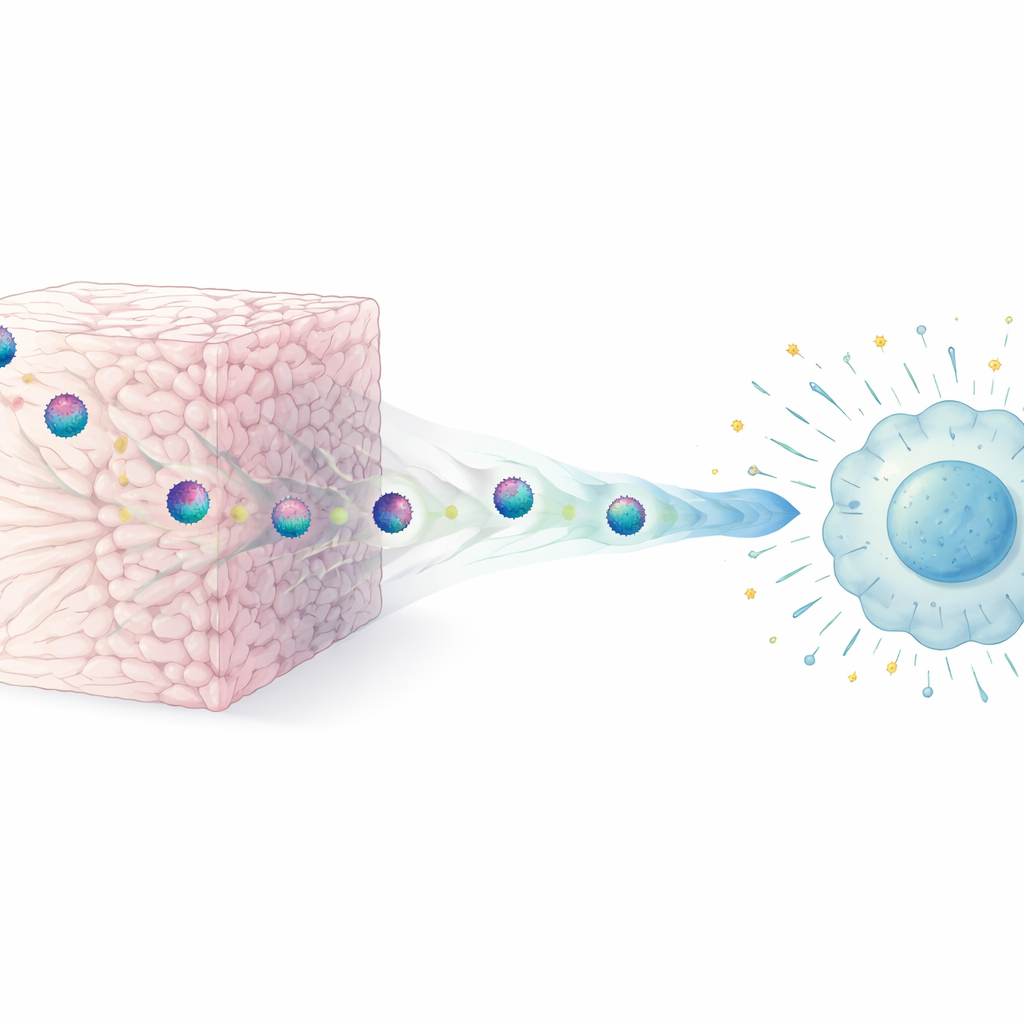
Wie Kollagen das Virus zähmt
Eine naheliegende Befürchtung war, dass Kollagen die Viruspartikel schlicht zerstört. Mithilfe hochauflösender Elektronenmikroskopie zeigte das Team, dass dem nicht so ist: HIV‑Partikel, die aus Kollagengelen kamen, sahen strukturell normal aus, mit intakten Membranen und Kernen. Auch entfernte Kollagen nicht die Oberflächenproteine des Virus. Stattdessen war die entscheidende Veränderung funktionell: Kollagen‑exponierte Viren banden weiterhin an Zielzellen, verschmolzen mit ihnen jedoch deutlich weniger effizient, das heißt der Eintritt in die Zelle wurde sehr früh blockiert. Künstliche „Infektiositätssteigernde“ Nanofasern, die Viren beim Verschmelzen mit Zellen helfen, konnten die Infektiosität von kollagenbehandeltem HIV wiederherstellen, was die Idee stützt, dass die Matrix hauptsächlich den Fusionsschritt stört, statt das Virus insgesamt zu beschädigen.
Von stummen Partikeln zu Immunalarmen
Die überraschendste Beobachtung war, dass Kollagenkontakt nicht nur die Infektion abschwächte, sondern HIV auch zu einem stärkeren Alarmsignal für angeborene Immunzellen, insbesondere monocytenabgeleitete Makrophagen, machte. Wurden diese Zellen mit kollagenerfahrenem HIV exponiert, produzierten sie deutlich mehr entzündliche Moleküle wie IL‑6, IL‑8 und TNF als bei Kontakt mit gewöhnlichem Virus, obwohl die tatsächlichen Infektionsraten nur mäßig vermindert waren. Detaillierte Genexpressionsanalysen zeigten, dass Makrophagen, die durch kollagen‑geprimtes Virus aktiviert wurden, ein breites antivirales Programm einschalteten, einschließlich vieler bekannter Restriktionsfaktoren und Warnsignale, die helfen, eine umfassendere Immunantwort zu koordinieren.
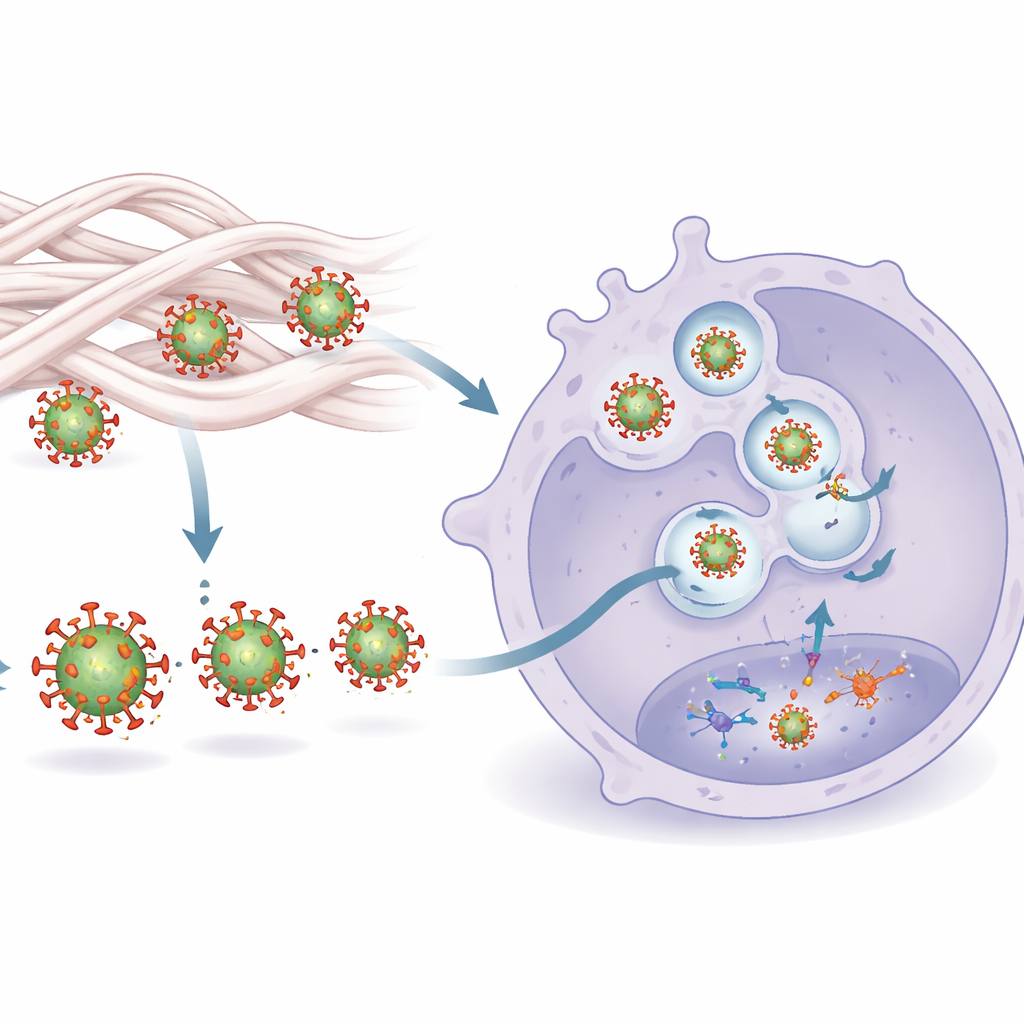
Wie die Erkennung eingeschaltet wird
Die Studie führte diese verstärkte Erkennung auf einen zweiteiligen Mechanismus zurück. Zuerst formt der Kontakt mit Kollagen die Außenhülle des Virusproteins Env subtil um. Diese Formveränderungen machen Env für einen Sensor auf Makrophagen, Toll‑like‑Rezeptor 2 (TLR2), leichter zugänglich. Zweitens wird das an der Oberfläche erkannte Virus effizienter in interne Kompartimente geleitet, die einen weiteren Sensor, TLR8, enthalten und das virale RNA‑Genom erkennen. Die Blockade von TLR2 oder TLR8 unterdrückte den durch Kollagen induzierten Zytokinsturm, was zeigt, dass beide Signale erforderlich sind. Mikroskopische Untersuchungen bestätigten, dass kollagenbehandelte Viren stärker an eine lösliche Form von TLR2 banden und wahrscheinlicher in TLR8‑reiche Endosomen gelangten, wo sie eine robuste antivirale Kaskade auslösen können.
Warum das für Menschen mit HIV wichtig ist
Für Laien lautet die Kernbotschaft: Unser Gewebe ist kein neutraler Schauplatz während einer HIV‑Infektion. Die Fasern, die Organen ihre Struktur geben, können direkt die Ausbreitung von HIV erschweren und gleichzeitig Immunzellen helfen, das Virus deutlicher zu erkennen. Diese „gewebe‑intrinsische“ Abwehr wirkt außerhalb der Zellen und ergänzt die bekannteren antiviralen Proteine im Inneren. Die Arbeit weist auch auf eine Kehrseite hin: Dieselben entzündlichen Signale, die das Virus kontrollieren helfen, könnten über die Zeit zur Gewebsnarbung und chronischen Entzündung beitragen, wie sie bei Menschen mit HIV beobachtet werden. Zu verstehen, wie die extrazelluläre Matrix dieses Gleichgewicht beeinflusst, könnte neue Wege eröffnen, schützende Immunität zu stärken und gleichzeitig Langzeitschäden zu begrenzen.
Zitation: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
Schlüsselwörter: HIV angeborene Immunität, extrazelluläre Matrix, Kollagen und Virus, Toll‑like‑Rezeptoren, gewebsbasierte antivirale Abwehr