Clear Sky Science · it
Un meccanismo intrinseco del tessuto sensibilizza le particelle di HIV‑1 alle risposte immunitarie innate attivate dai TLR
Come i nostri tessuti combattono silenziosamente l’HIV
L’HIV di solito fa notizia per come disattiva il sistema immunitario, ma questo studio rovescia la prospettiva: si chiede cosa fanno i tessuti stessi per respingere il virus. In profondità nei linfonodi e in altri organi, cellule immunitarie e virus si muovono attraverso una rete tridimensionale di collagene e altre proteine. Questo lavoro mostra che tale rete non è solo un’impalcatura passiva. Al contrario, indebolisce attivamente la capacità dell’HIV di infettare le cellule e, allo stesso tempo, rende il virus più visibile alle nostre difese innate.
Il mondo nascosto tra le cellule
Nel nostro corpo, le cellule sono immerse in una complessa rete chiamata matrice extracellulare, costituita in gran parte da fibre di collagene. I ricercatori hanno creato gel semplificati “simili a tessuti” fatti di diversi tipi di collagene per imitare questo ambiente. Hanno quindi lasciato che particelle di HIV si muovessero attraverso questi gel tridimensionali e le hanno confrontate con virus mantenuti in colture liquide ordinarie. Hanno scoperto che un breve contatto fisico con le fibre di collagene era sufficiente per ridurre drasticamente la capacità del virus di infettare nuove cellule, fenomeno che chiamano restrizione extracellulare dell’infettività dei virioni. Questo effetto compariva rapidamente, dipendeva dal contatto diretto con la matrice ed è stato osservato in diversi ceppi di HIV e in vari materiali ricchi di collagene, ma non in gel non adesivi come l’agarosio.
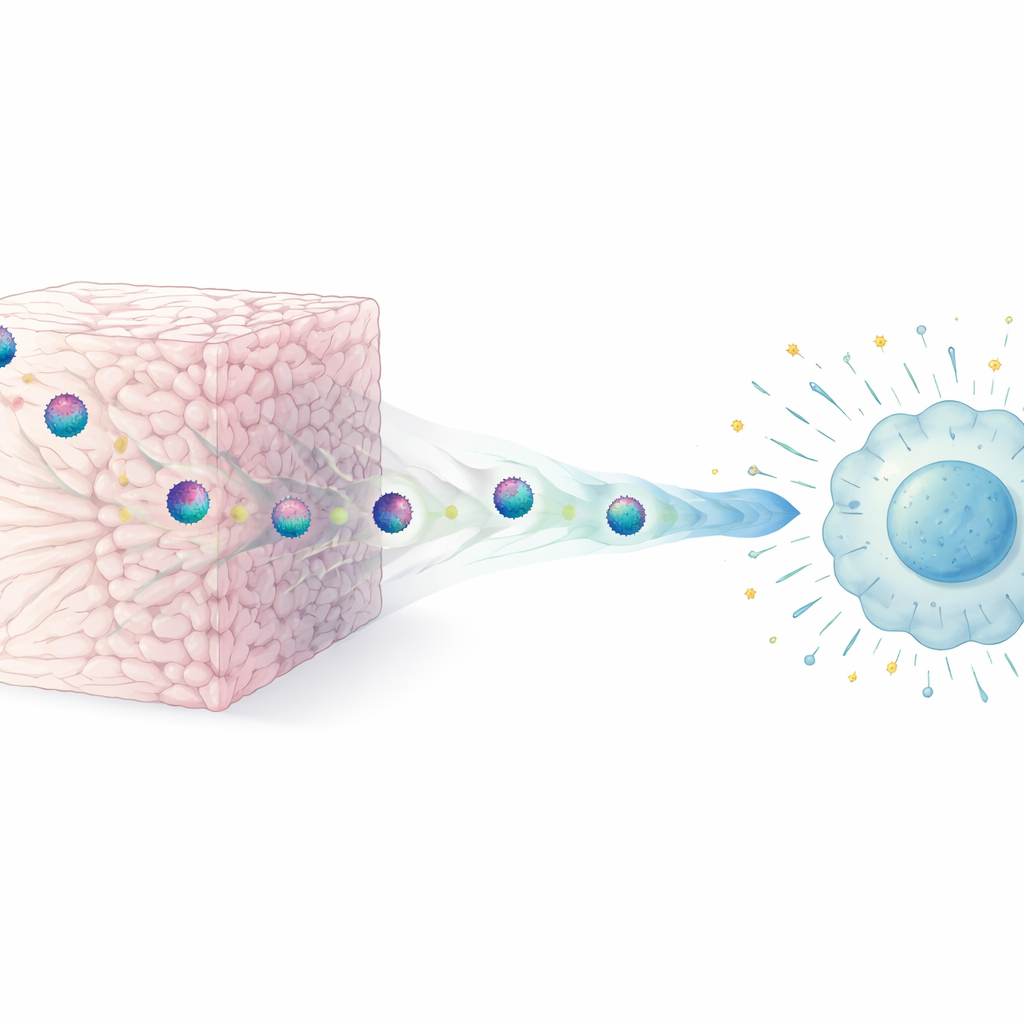
Come il collagene doma il virus
Un timore ovvio era che il collagene potesse semplicemente distruggere le particelle virali. Usando microscopia elettronica ad alta risoluzione, il gruppo ha mostrato che non è così: le particelle di HIV che emergevano dai gel di collagene apparivano strutturalmente normali, con membrane e core intatti. Neppure il collagene rimuoveva le proteine superficiali del virus. La modifica principale era invece funzionale. I virus esposti al collagene si legavano ancora alle cellule bersaglio, ma si fondevano con esse in modo molto meno efficiente, il che significa che l’ingresso nella cellula veniva bloccato a uno stadio molto precoce. Nanofibre artificiali che aumentano l’infettività e facilitano la fusione virale sono state in grado di ripristinare la capacità infettiva dell’HIV trattato con collagene, rafforzando l’idea che la matrice interferisca principalmente con il processo di fusione piuttosto che danneggiare il virus nel suo complesso.
Da particelle silenziose ad allarmi immunitari
La scoperta più sorprendente è stata che il contatto con il collagene non si limitava a ridurre l’infezione; trasformava anche l’HIV in un segnale d’allarme più potente per le cellule immunitarie innate, in particolare i macrofagi derivati dai monociti. Quando queste cellule venivano esposte a virus «esperti» del collagene, producevano molte più molecole infiammatorie come IL‑6, IL‑8 e TNF rispetto all’esposizione al virus normale, anche se i livelli di infezione effettiva erano solo moderatamente ridotti. Un profilo dettagliato dell’espressione genica ha mostrato che i macrofagi attivati dal virus primed dal collagene accendevano un ampio programma antivirale, inclusi molti fattori di restrizione immunitaria noti e segnali di allerta che aiutano a coordinare risposte immunitarie più ampie.
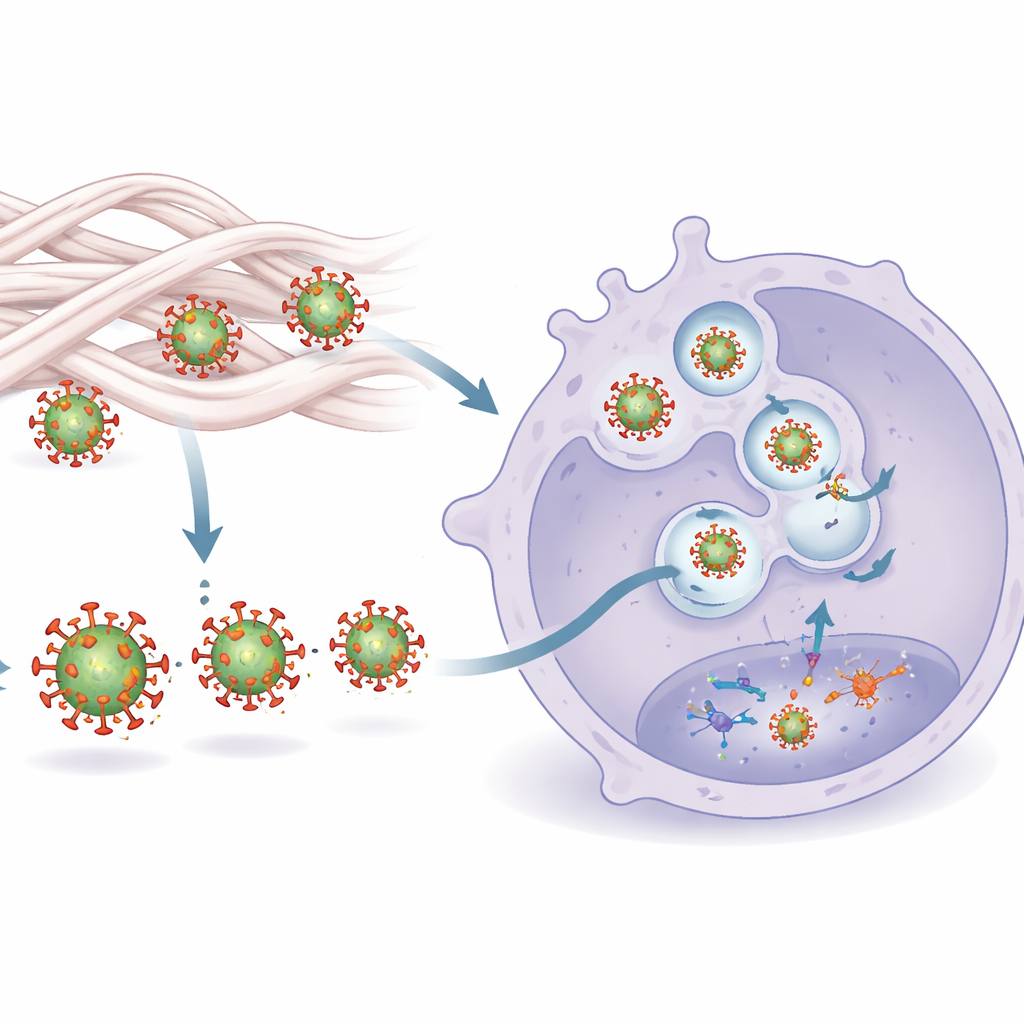
Come si attiva il rilevamento
Lo studio ha ricondotto questo aumento della sensibilità a un meccanismo in due parti. Primo, il contatto con il collagene rimodella sottilmente la proteina di rivestimento esterna dell’HIV, Env. Questi cambiamenti conformazionali rendono Env più facile da riconoscere per un sensore sui macrofagi, il recettore Toll‑like 2 (TLR2). Secondo, una volta riconosciuto in superficie, il virus viene indirizzato più efficacemente verso compartimenti interni che contengono un altro sensore, TLR8, che rileva il genoma RNA del virus. Il blocco di TLR2 o TLR8 sopprimeva l’ondata di citochine indotta dal collagene, dimostrando che entrambi i segnali sono necessari. La microscopia ha confermato che i virus trattati con collagene si legavano più fortemente a una versione solubile di TLR2 ed erano più propensi a finire negli endosomi ricchi di TLR8, dove potevano innescare una robusta cascata antivirale.
Perché questo è importante per le persone che vivono con l’HIV
Per un non specialistico, il messaggio principale è che i nostri tessuti non sono terreno neutro durante l’infezione da HIV. Le stesse fibre che danno struttura agli organi possono ostacolare direttamente la capacità dell’HIV di diffondersi e, allo stesso tempo, aiutare le cellule immunitarie a riconoscere il virus più chiaramente. Questa difesa «intrinseca del tessuto» agisce all’esterno delle cellule, completando le proteine antivirali meglio conosciute che operano all’interno. Il lavoro suggerisce anche una lama a doppio taglio: gli stessi segnali infiammatori che aiutano a controllare il virus potrebbero, nel tempo, contribuire alla formazione di cicatrici tissutali e all’infiammazione cronica osservata nelle persone con HIV. Comprendere come la matrice extracellulare modula questo equilibrio potrebbe aprire nuove vie per potenziare l’immunità protettiva limitando i danni a lungo termine.
Citazione: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
Parole chiave: Immunità innata contro HIV, Matrice extracellulare, collagene e virus, recettori Toll‑like, difesa antivirale tessutale