Clear Sky Science · es
Un mecanismo intrínseco del tejido sensibiliza las partículas de VIH-1 para las respuestas inmunitarias innatas desencadenadas por TLR
Cómo nuestros tejidos luchan en silencio contra el VIH
El VIH suele salir en los titulares por cómo incapacita al sistema inmunitario, pero este estudio invierte la historia: pregunta qué hacen los propios tejidos para contrarrestarlo. En el interior de los ganglios linfáticos y otros órganos, las células inmunitarias y los virus se desplazan por una malla tridimensional de colágeno y otras proteínas. Este trabajo demuestra que esa malla no es solo un andamiaje pasivo. Más bien, debilita activamente la capacidad del VIH para infectar células y, al mismo tiempo, hace que el virus sea más visible para nuestras defensas inmunitarias innatas.
El mundo oculto entre las células
En nuestro cuerpo, las células están rodeadas por una red intrincada llamada matriz extracelular, formada en gran parte por fibras de colágeno. Los investigadores crearon geles «tipo tejido» simplificados hechos de distintos tipos de colágeno para imitar este entorno. Dejaron que partículas de VIH se desplazaran por esos geles tridimensionales y las compararon con virus mantenidos en cultivos líquidos ordinarios. Hallaron que un contacto físico breve con las fibras de colágeno bastaba para reducir drásticamente la capacidad del virus para infectar nuevas células, un fenómeno que denominaron restricción extracelular de la infectividad de los viriones. Este efecto apareció con rapidez, dependía del contacto directo con la matriz y se observó en diferentes cepas de VIH y en varios materiales ricos en colágeno, pero no en geles no adhesivos como la agarosa.
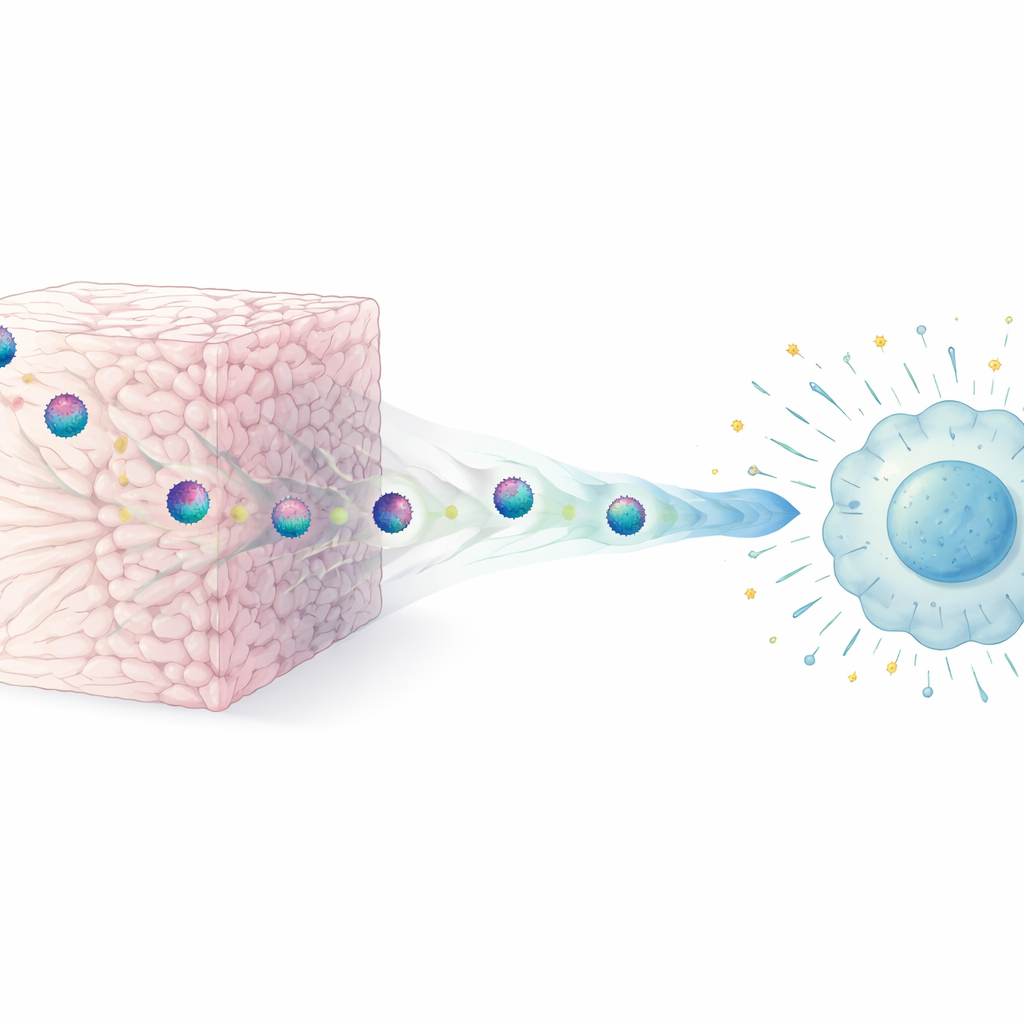
Cómo el colágeno domestica al virus
Una preocupación obvia era que el colágeno pudiera simplemente destruir las partículas virales. Usando microscopía electrónica de alta resolución, el equipo mostró que no era así: las partículas de VIH que salían de los geles de colágeno tenían un aspecto estructuralmente normal, con membranas y núcleos intactos. Tampoco el colágeno arrancó las proteínas superficiales del virus. En cambio, el cambio clave fue funcional. Los virus expuestos al colágeno seguían uniéndose a las células diana, pero se fusionaban con ellas con mucha menos eficiencia, lo que significa que la entrada en la célula se bloqueaba en un paso muy inicial. Nanofibras artificiales «potenciadoras de la infectividad» que ayudan a los virus a fusionarse con las células pudieron restaurar la capacidad infecciosa del VIH tratado con colágeno, lo que refuerza la idea de que la matriz interfiere principalmente con el proceso de fusión en lugar de dañar el virus en su conjunto.
De partículas silenciosas a alarmas inmunitarias
El hallazgo más sorprendente fue que el contacto con colágeno no solo atenuaba la infección; también convertía al VIH en una señal de alarma más potente para las células inmunitarias innatas, en particular los macrófagos derivados de monocitos. Cuando estas células se exponían al VIH «experto» en colágeno, producían muchos más mediadores inflamatorios como IL-6, IL-8 y TNF que al exponerse al virus habitual, aunque los niveles de infección reales solo se reducían modestamente. Un perfil detallado de expresión génica mostró que los macrófagos activados por el virus primado con colágeno encendían un amplio programa antiviral, que incluye muchos factores de restricción inmunitaria conocidos y señales de alerta que ayudan a coordinar respuestas inmunes más amplias.
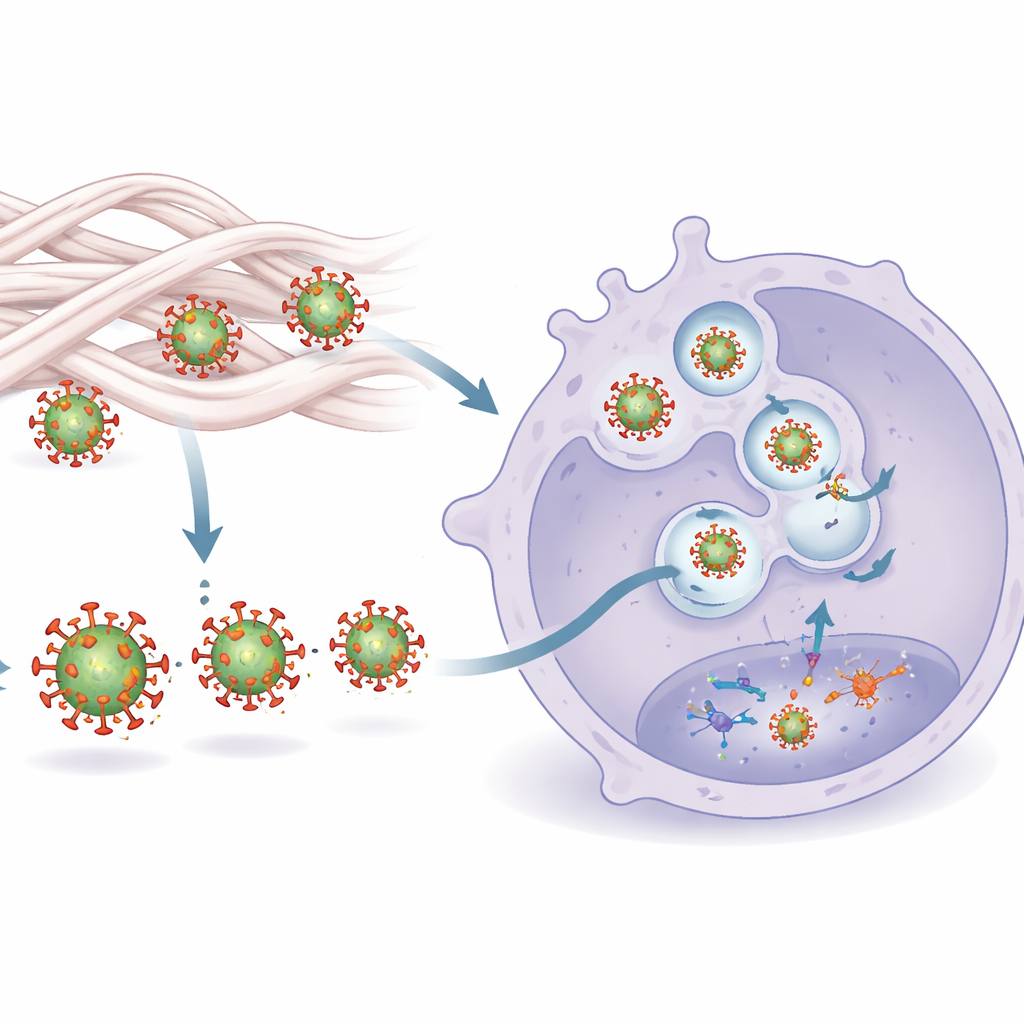
Cómo se activa la detección
El estudio rastreó esta mayor capacidad de detección hasta un mecanismo de dos partes. Primero, el contacto con el colágeno remodela sutilmente la proteína de cubierta externa del VIH, Env. Estos cambios conformacionales hacen que Env sea más accesible para un sensor en los macrófagos, el receptor tipo Toll 2 (TLR2). Segundo, una vez reconocido en la superficie, el virus se transporta con mayor eficiencia a compartimentos internos que contienen otro sensor, TLR8, que detecta el genoma de ARN del virus. Bloquear TLR2 o TLR8 suprimió el aumento de citocinas inducido por el colágeno, lo que muestra que se necesitan ambas señales. La microscopía confirmó que los virus tratados con colágeno se unían con más fuerza a una versión soluble de TLR2 y que era más probable que terminaran en endosomas ricos en TLR8, donde podían desencadenar una potente cascada antiviral.
Por qué esto importa para las personas que viven con VIH
Para el público general, el mensaje central es que nuestros tejidos no son un terreno neutral durante la infección por VIH. Las mismas fibras que dan estructura a los órganos pueden entorpecer directamente la capacidad del VIH para propagarse y, al mismo tiempo, ayudar a las células inmunitarias a reconocer el virus con mayor claridad. Esta defensa «intrínseca del tejido» actúa fuera de las células, complementando las proteínas antivirales mejor conocidas que actúan dentro de ellas. El trabajo también sugiere una espada de doble filo: las mismas señales inflamatorias que ayudan a controlar el virus pueden, con el tiempo, contribuir a la cicatrización tisular y la inflamación crónica observadas en personas que viven con VIH. Comprender cómo la matriz extracelular ajusta este equilibrio podría abrir nuevas vías para potenciar la inmunidad protectora y, al mismo tiempo, limitar el daño a largo plazo.
Cita: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
Palabras clave: inmunidad innata frente al VIH, matriz extracelular, colágeno y virus, receptores tipo Toll, defensa antiviral tisular