Clear Sky Science · zh
通过囊泡外排进行无损转录组学
在不破坏细胞的情况下观察活细胞
我们的细胞不断地开关基因,科学家通过读取 RNA(携带遗传指令的信使分子)来追踪这种活动。但问题是:几乎所有现有方法都需要将细胞破碎,因此每次测量都会毁掉被研究的细胞。本文介绍了一种方法,可以在不伤害细胞的情况下连续多天窃听细胞的 RNA“对话”,从而能够跟踪相同细胞在药物作用下的反应或如何成熟为心肌或神经元等组织。
让细胞成为温和的信息发送者
研究者开发了他们称为“通过囊泡外排的无损转录组学”(NTVE)的平台。NTVE 并不破坏细胞,而是促使细胞定期释放微小的泡状囊泡,这些囊泡将细胞 RNA 的样本安全地带入周围液体中。囊泡由一种简化的 HIV 蛋白外壳构建,这种外壳会自然地从细胞表面出芽。通过在外壳内部加入分子“把手”,团队确保 RNA 分子被拉入出芽的囊泡;通过在囊泡表面添加不同的标记,他们可以在共培养的不同细胞类型之间分离囊泡。 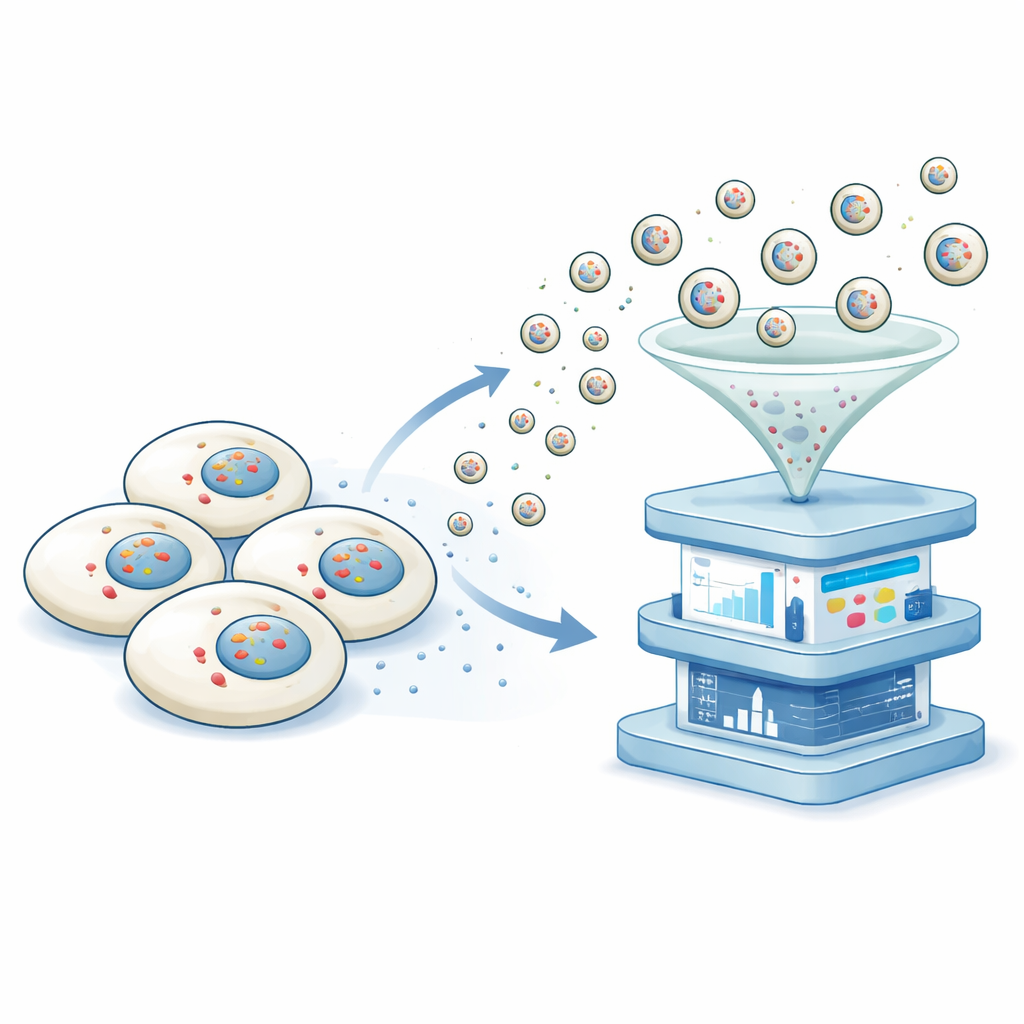
捕捉完整的 RNA 全貌
一个关键挑战是确保这些外排的囊泡真实反映细胞内的情况,而不是仅仅抓取有偏的 RNA 子集或泄漏受损材料。为了解决这一点,作者将一种正常细胞蛋白的片段——可结合大多数信使 RNA 尾部的片段——融合到囊泡外壳的内侧。此设计能够从靠近细胞表面的区域吸引广泛且平衡的 RNA 信息集合。通过将囊泡中的 RNA 与来自同一细胞的传统破坏性取样的 RNA 进行比较,他们在 14,000 多个基因上显示出高度一致性。重要的是,可能指示膜损伤和泄漏的线粒体 RNA 被明显耗尽,这表明细胞在外排 RNA 的同时保持完整和健康。
跟踪细胞的变化过程
有了 NTVE,团队测试了它是否能随时间跟踪细胞对特定刺激的反应。在人细胞中,NTVE 正确报告了由 CRISPR 基因激活器驱动的单个“开启”基因的激活;当细胞暴露于免疫信号干扰素-γ 时,NTVE 与传统方法高度吻合,捕捉到了相同的通路和响应基因。研究者随后转向更脆弱的系统:小鼠原代神经元和人类干细胞。通过将 NTVE 装置封装进病毒载体或转座子,他们创造了可用简单药物诱导开始囊泡生产的神经元和干细胞系。在神经元中,NTVE 捕捉到了随 forskolin(已知可激活与记忆相关信号)刺激而出现的基因活动波动。
观察干细胞成为组织的过程
由于 NTVE 不会杀死细胞,它特别适合观察像干细胞分化这样需要数天的缓慢过程。作者改造了人诱导多能干细胞以表达 NTVE,并将其分别引导向三条发育路径:类神经、类肌肉和类肠道谱系。通过每天采样囊泡 RNA,他们重建了这些细胞群体的分叉轨迹,并评估了哪些标记基因最能区分各谱系。在另一项实验中,他们跟踪了干细胞在九天内成熟为有节律跳动的心肌细胞。每日的 NTVE 测量捕捉到了关键心脏基因的升降,并显示心脏特异性标记的激增与首个可见收缩同时发生。 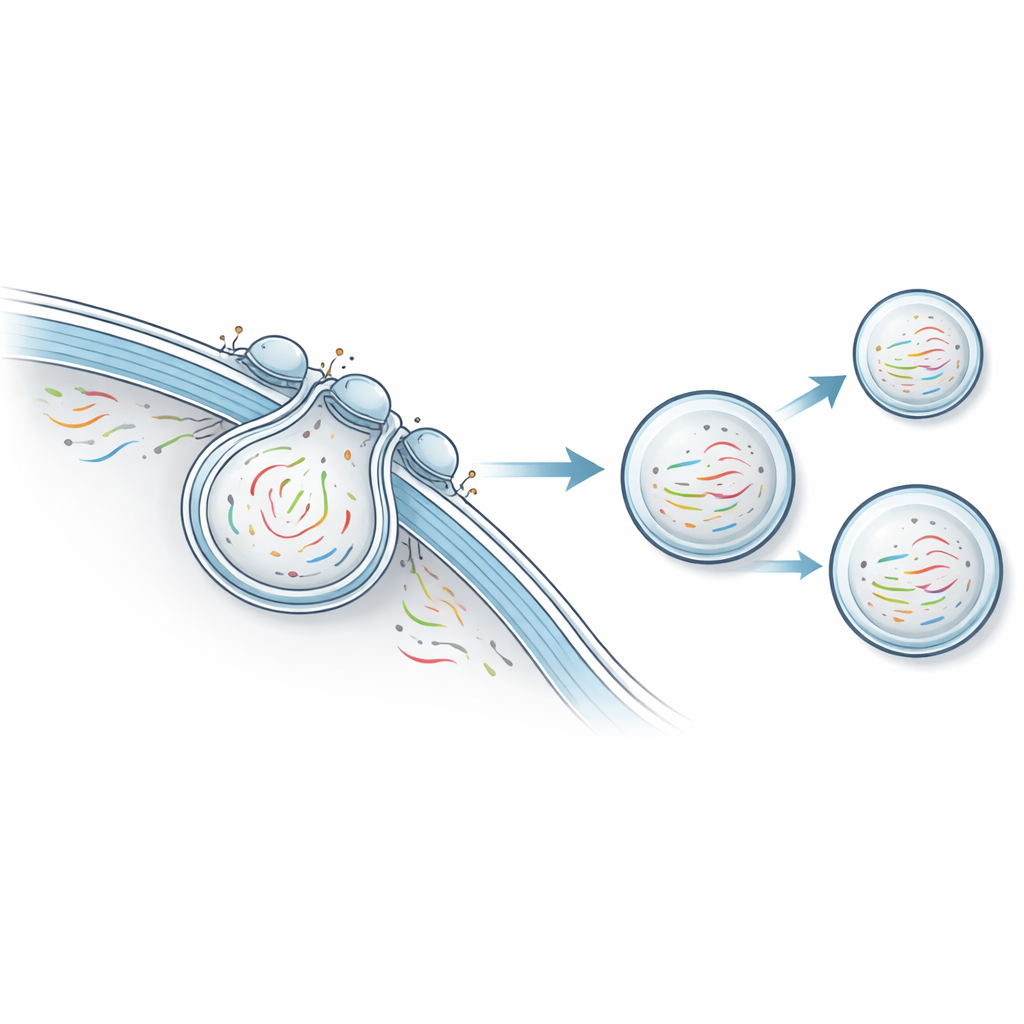
在细胞间发送信息
除了被动监测外,NTVE 囊泡还可以被改造成递送载体。团队证明可以将信使 RNA 或基因编辑蛋白复合体装入囊泡,并利用病毒衣壳蛋白作为定向装置将其导向特定的“接收”细胞。在共培养细胞中,这使一类细胞能够发送囊泡去开启另一个细胞群体中的基因开关或改写 DNA,创建了一个可编程的细胞间通信通道,该通道基于与 RNA 读取相同的囊泡平台。
这对未来研究的重要性
对非专业读者来说,关键思想是 NTVE 允许科学家对培养皿中的活细胞反复进行“液体活检”,日复一日地读取它们的基因活动而不牺牲细胞。这克服了标准 RNA 分型的一个主要限制:每个时间点都需要一批新的细胞,从而掩盖了单个细胞如何演变。有了 NTVE,每个培养物——甚至每个类器官——都可以作为自身的基线,提高检测细微变化的能力,使对发育、疾病模型和药物反应的长期研究更为精确。尽管该方法目前聚焦于细胞质中的信使 RNA,且尚不能将囊泡 RNA 指定到单个细胞,但它已提供了一种可及且多用途的方式来实时观察细胞分子生命的展开。
引用: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
关键词: RNA 外排, 活细胞转录组学, 细胞外囊泡, 干细胞分化, 基因表达动态