Clear Sky Science · nl
Niet-destructieve transcriptomica via vesiculaire export
Levende cellen observeren zonder ze te beschadigen
Onze cellen schakelen voortdurend genen aan en uit, en wetenschappers volgen die activiteit door RNA af te lezen, de boodschappermoleculen die genetische instructies overbrengen. Maar er is een probleem: bijna alle huidige methoden vereisen het openbreken van cellen, waardoor elke meting de onderzochte cellen vernietigt. Dit artikel introduceert een manier om het RNA‑verkeer van een cel dagenlang af te luisteren zonder de cellen te schaden, wat het mogelijk maakt te volgen hoe dezelfde cellen op medicijnen reageren of uitrijpen tot weefsels zoals hartspier of neuronen.
Cellen veranderen in rustige boodschappers
De onderzoekers ontwikkelden een platform dat zij niet-destructieve transcriptomica via vesiculaire export noemen, of NTVE. In plaats van cellen open te breken, verleidt NTVE ze ertoe regelmatig kleine blaasjes, of vesikels, uit te stoten die veilig een staal van hun RNA in de omringende vloeistof dragen. Deze vesikels worden gebouwd met een uitgeklede vorm van een HIV-eiwitschil die van nature van het celoppervlak afsnoert. Door moleculaire "handvatten" binnenin deze schaal toe te voegen, zorgt het team ervoor dat RNA-moleculen in de zich vormende vesikels worden getrokken, en door onderscheidende merkers op het vesikeloppervlak te plaatsen, kunnen ze later vesikels van verschillende celtypen die samen gekweekt zijn scheiden. 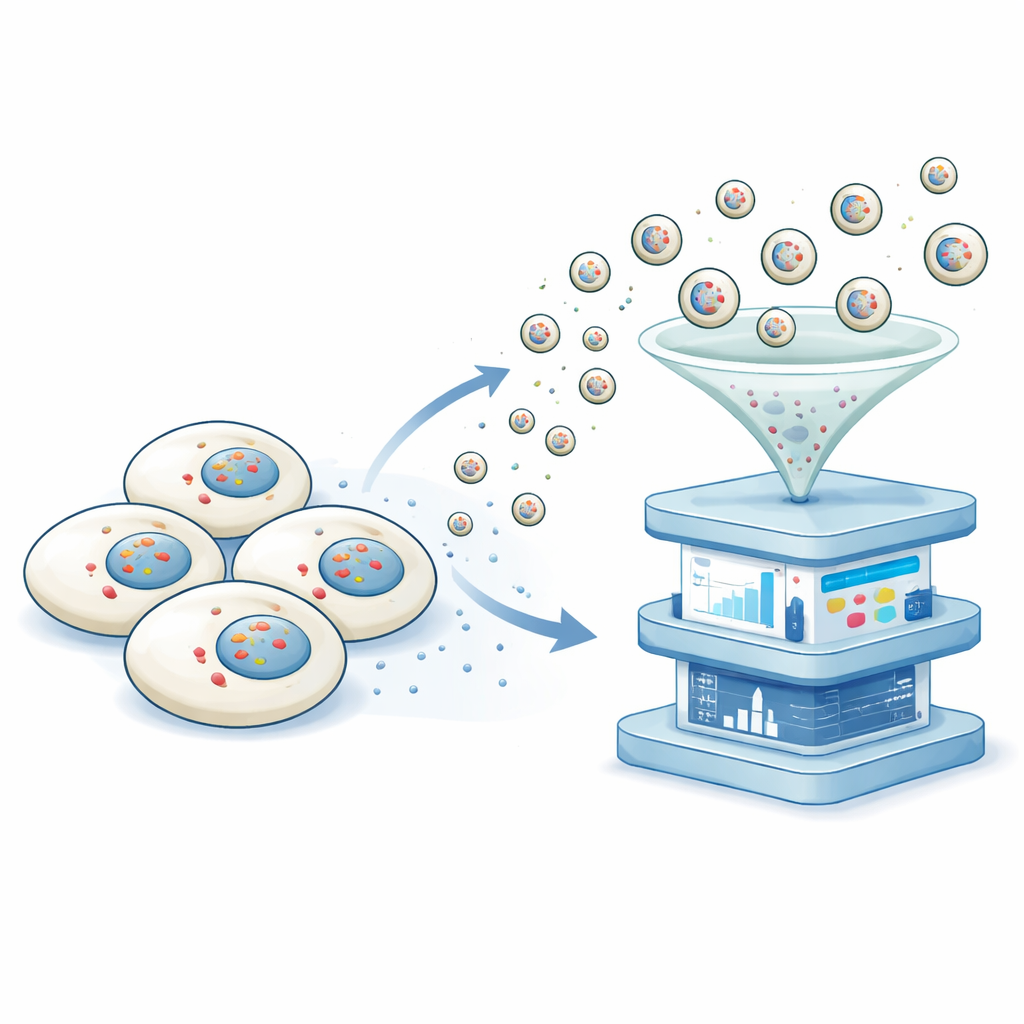
Het volledige RNA‑plaatje vangen
Een belangrijke uitdaging is ervoor te zorgen dat deze geëxporteerde vesikels echt weerspiegelen wat er binnenin de cel gebeurt, en niet slechts een bevooroordeelde subset van RNA’s grijpen of beschadigd materiaal lekken. Om dit op te lossen fuseerden de auteurs een deel van een normaal cellulair eiwit dat aan de staart van de meeste boodschapper‑RNA’s bindt aan de binnenkant van de vesikelschaal. Dit ontwerp trekt een brede en evenwichtige verzameling RNA‑boodschappen aan van dichtbij het celoppervlak. Door het RNA uit vesikels te vergelijken met RNA uit traditionele destructieve monsters van dezelfde cellen, toonden ze een zeer sterke overeenkomst voor meer dan 14.000 genen. Belangrijk is dat mitochondriale RNA’s, die op membraanschade en lekkage zouden wijzen, sterk uitgeput waren, wat suggereert dat de cellen intact en gezond blijven terwijl ze RNA exporteren.
Cellen volgen tijdens verandering
Met NTVE op zijn plaats testte het team of het kon volgen hoe cellen in de loop van de tijd op specifieke triggers reageren. In menselijke cellen rapporteerde NTVE correct de activering van een enkel "aangeslagen" gen aangedreven door een CRISPR‑gebaseerde activator, en het kwam nauw overeen met conventionele methoden toen cellen werden blootgesteld aan het immuunsignaal interferon‑gamma, waarbij dezelfde paden en responsergenen werden vastgelegd. De onderzoekers gingen daarna naar gevoeliger systemen: primaire muisneuronen en menselijke stamcellen. Door de NTVE‑machinerie in virale vectoren of transposons te verpakken, creëerden ze neuronale en stamcellijnen die met een eenvoudig geneesmiddel geïnduceerd konden worden om vesikelproductie te starten. In neuronen legde NTVE de golf van genactiviteit vast die volgt op stimulatie met forskolin, een verbinding die bekendstaat om geheugen-gerelateerde signaalering te activeren.
Stamcellen zien veranderen in weefsels
Omdat NTVE de cellen niet doodt, is het bijzonder geschikt om langzame, meerdaagse processen zoals stamceldifferentiatie te volgen. De auteurs programmeerden menselijk geïnduceerde pluripotente stamcellen om NTVE tot expressie te brengen en stuurden ze vervolgens langs drie ontwikkelingspaden: richting zenuw‑, spier‑ en darmachtige lijnen. Door dagelijks vesikel‑RNA te bemonsteren reconstructeerden ze de vertakkende trajecten van deze celpopulaties en evalueerden ze welke markergenen elke lijn het beste onderscheidden. In een apart experiment volgden ze stamcellen die over negen dagen uitrijpten tot kloppende hartcellen. Dagelijkse NTVE‑metingen legden het opkomen en weer afnemen van belangrijke cardiale genen vast en toonden dat de piek in hart‑specifieke markers samenviel met de eerste zichtbare contracties. 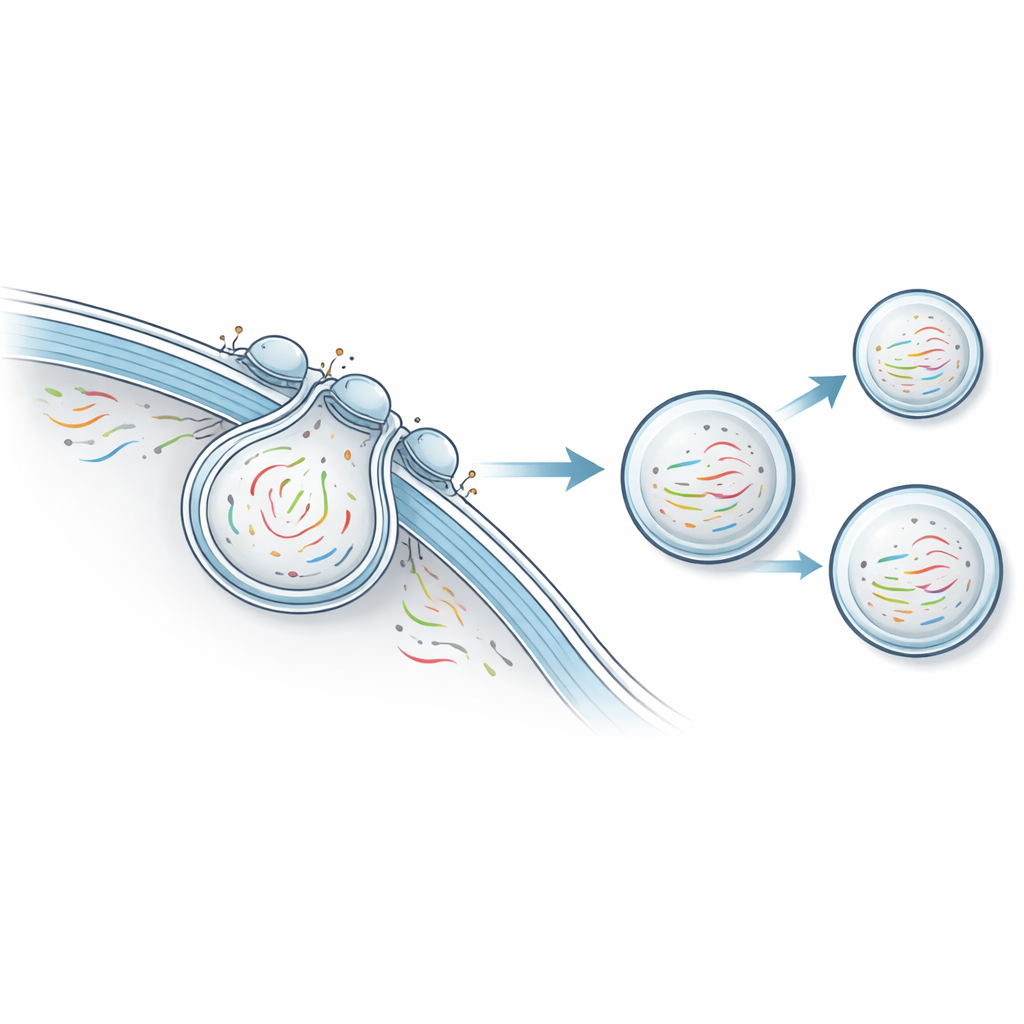
Boodschappen tussen cellen sturen
Buiten passieve monitoring kunnen NTVE‑vesikels ook worden omgezet in afleveringsvoertuigen. Het team demonstreerde dat vesikels geladen konden worden met boodschapper‑RNA’s of genbewerkings‑eiwitcomplexen en gericht konden worden op specifieke "ontvangende" cellen met behulp van virale schileiwitten als targetingsapparaten. In co‑gekweekte cellen maakte dit het mogelijk dat de ene populatie vesikels verzond die genetische schakelaars omschakelden of DNA herschreven in een andere populatie, waardoor een programmeerbaar kanaal voor cel‑tot‑celcommunicatie ontstond dat gebruikmaakt van hetzelfde vesikelplatform dat voor RNA‑aflezing wordt gebruikt.
Waarom dit belangrijk is voor toekomstig onderzoek
Voor niet‑specialisten is het belangrijkste idee dat NTVE wetenschappers in staat stelt herhaaldelijk "vloeibare biopsies" van levende cellen in een schaaltje te nemen en hun genactiviteit dag na dag af te lezen zonder de cellen op te offeren. Dit overwint een grote beperking van standaard RNA‑profilering, waarbij elk tijdstip een nieuwe partij cellen vereist en het moeilijk wordt te zien hoe individuele cellen zich ontwikkelen. Met NTVE kan elke cultuur — of zelfs elk organoïde — als zijn eigen referentie dienen, wat de gevoeligheid voor subtiele veranderingen verbetert en langlopende studies van ontwikkeling, ziektemodellen en medicijnreacties preciezer maakt. Hoewel de methode zich momenteel richt op cytoplasmatische boodschapper‑RNA’s en vesikel‑RNA’s nog niet aan individuele cellen kan worden toegewezen, biedt ze al een toegankelijke en veelzijdige manier om het moleculaire leven van cellen in realtime te volgen.
Bronvermelding: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Trefwoorden: RNA-export, live-cell transcriptomica, extracellulaire vesikels, stamcel-differentiatie, genexpressiedynamiek