Clear Sky Science · pl
Transkryptomika niedestrukcyjna przez eksport pęcherzykowy
Obserwowanie żywych komórek bez ich niszczenia
Nasze komórki nieustannie włączają i wyłączają geny, a naukowcy śledzą tę aktywność, odczytując RNA — nośniki informacji genetycznej. Jest jednak haczyk: niemal wszystkie dostępne metody wymagają rozerwania komórek, więc każde badanie niszczy właśnie te komórki, które się bada. W pracy tej przedstawiono sposób podsłuchiwania „rozmów” RNA komórki przez wiele dni bez szkody dla komórek, co umożliwia śledzenie, jak te same komórki reagują na leki lub dojrzewają w tkanki takie jak mięsień sercowy czy neurony.
Przekształcanie komórek w delikatnych posłańców
Naukowcy opracowali platformę nazwaną niedestrukcyjną transkryptomiką przez eksport pęcherzykowy (NTVE). Zamiast rozrywać komórki, NTVE zachęca je do regularnego wysyłania małych pęcherzyków, które bezpiecznie przenoszą próbki RNA do otaczającego płynu. Pęcherzyki te powstają z uproszczonej formy białkowej otoczki wirusa HIV, która naturalnie odcina się od powierzchni komórki. Poprzez dodanie molekularnych „uchwytów” wewnątrz tej otoczki zespół zapewnia, że cząsteczki RNA są wciągane do tworzących się pęcherzyków, a przez umieszczenie charakterystycznych znaczników na powierzchni pęcherzyków mogą później oddzielić pęcherzyki pochodzące z różnych typów komórek hodowanych razem. 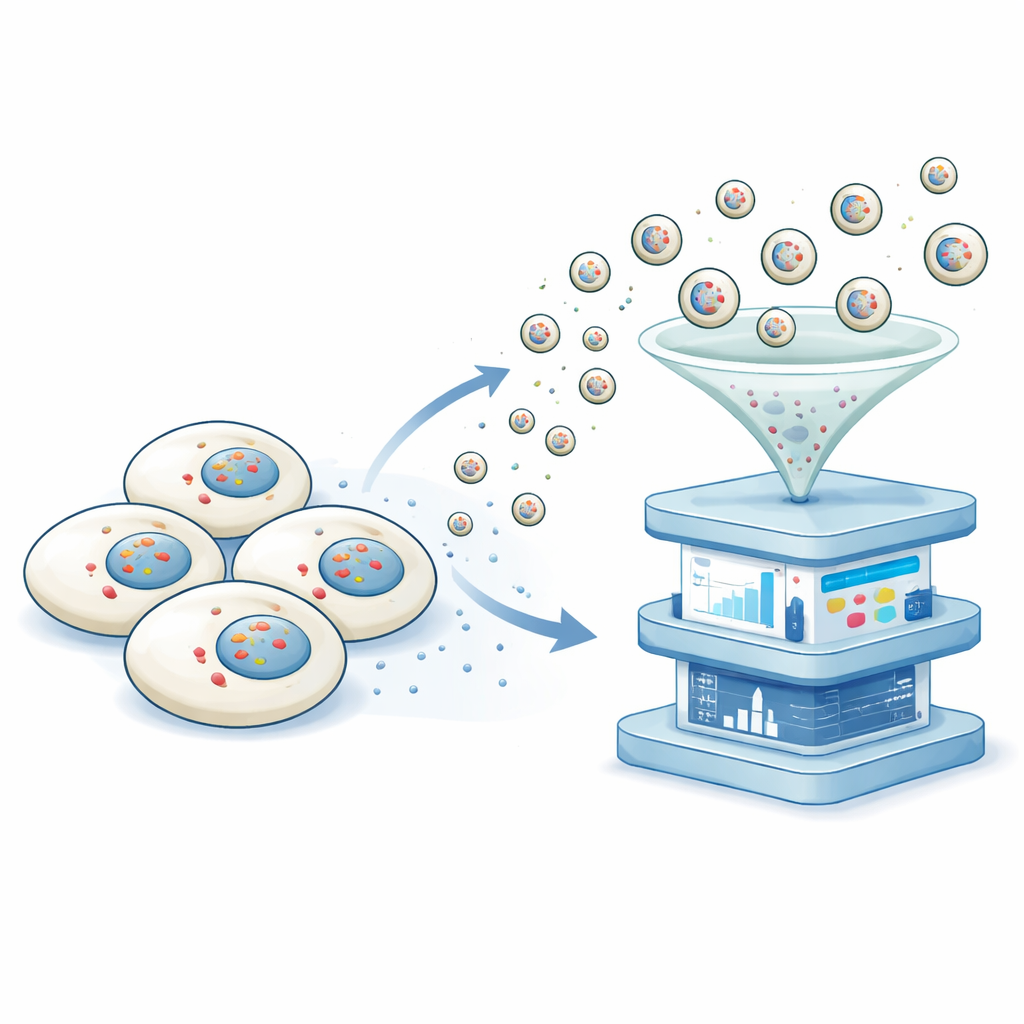
Uchwycenie pełnego obrazu RNA
Kluczowym wyzwaniem jest zapewnienie, że eksportowane pęcherzyki rzeczywiście odzwierciedlają to, co dzieje się we wnętrzu komórki, zamiast wybiórczo zbierać pewne RNA lub przewozić uszkodzone materiały. Aby to rozwiązać, autorzy dołączylI część normalnego białka komórkowego wiążącego ogon większości mRNA do wnętrza otoczki pęcherzyka. Ten zabieg przyciąga szeroką i zrównoważoną kolekcję komunikatów RNA pochodzących z rejonu blisko powierzchni komórki. Porównując RNA z pęcherzyków z RNA uzyskanym tradycyjną, destrukcyjną metodą z tych samych komórek, wykazali bardzo silne zgodności dla ponad 14 000 genów. Co ważne, RNA mitochondrialne, które mogłoby wskazywać na uszkodzenie błon i wyciek materiału, było silnie zubożone, co sugeruje, że komórki pozostają nienaruszone i zdrowe podczas eksportu RNA.
Śledzenie komórek w trakcie zmian
Dzięki NTVE zespół sprawdził, czy metoda może śledzić, jak komórki reagują w czasie na określone bodźce. W komórkach ludzkich NTVE poprawnie wykazało aktywację pojedynczego „włączonego” genu napędzanego aktywatorem opartym na CRISPR, a także dobrze dublowało wyniki konwencjonalnych metod, gdy komórki wystawiono na działanie sygnału immunologicznego interferonu gamma, odzwierciedlając te same ścieżki i geny odpowiedzi. Badacze później przeszli do delikatniejszych układów: pierwotnych neuronów mysich i ludzkich komórek macierzystych. Pakując aparat NTVE w wektory wirusowe lub transpozony, stworzyli linie neuronowe i komórkowe, które można było indukować prostym lekiem do rozpoczęcia produkcji pęcherzyków. W neuronach NTVE uchwyciło falę aktywności genów następującą po stymulacji forskoliną, związkiem znanym z aktywacji sygnalizacji pamięciowej.
Obserwowanie, jak komórki macierzyste stają się tkankami
Ponieważ NTVE nie zabija komórek, jest szczególnie przydatne do obserwacji powolnych, wielodniowych procesów, takich jak różnicowanie komórek macierzystych. Autorzy zaprojektowali ludzkie indukowane pluripotentne komórki macierzyste do ekspresji NTVE, a następnie skierowali je trzema ścieżkami rozwojowymi: w kierunku linii podobnych do nerwów, mięśni i jelit. Próbkując RNA pęcherzyków codziennie, odtworzyli rozgałęziające się trajektorie tych populacji komórkowych i ocenili, które geny markerowe najlepiej odróżniają poszczególne linie. W oddzielnym eksperymencie śledzili dojrzewanie komórek macierzystych w bijące komórki serca przez dziewięć dni. Codzienne pomiary NTVE uchwyciły wzrost i spadek kluczowych genów sercowych i pokazały, że fala markerów specyficznych dla serca zbiegła się z pierwszymi widocznymi skurczami. 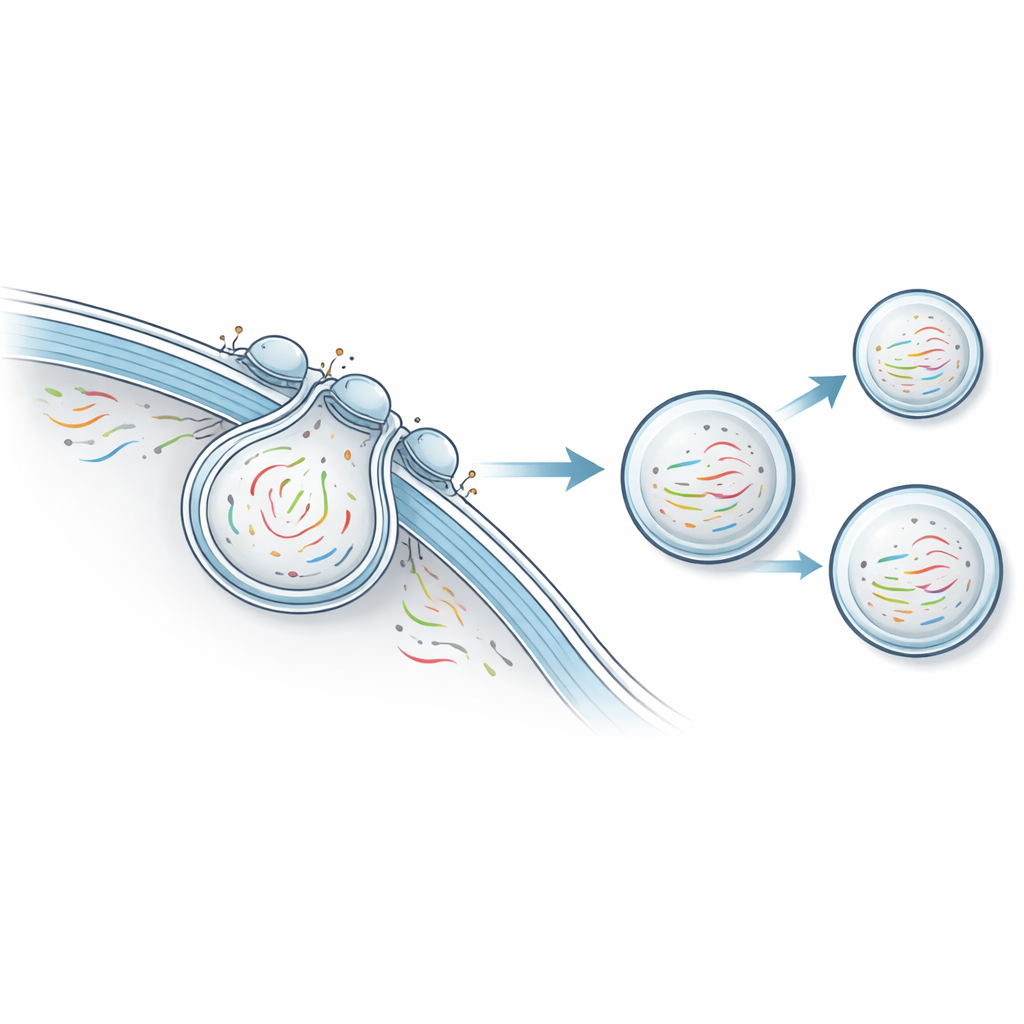
Wysyłanie wiadomości między komórkami
Poza biernym monitorowaniem, pęcherzyki NTVE można także przekształcić w nośniki dostaw. Zespół wykazał, że pęcherzyki można załadować mRNA lub kompleksami białek do edycji genów i skierować do określonych „odbiorczych” komórek, używając białek osłonowych wirusa jako urządzeń celujących. W hodowli współkulturowej pozwoliło to jednej populacji wysyłać pęcherzyki, które przełączały genetyczne przełączniki lub zmieniały DNA w innej populacji, tworząc programowalny kanał komunikacji międzykomórkowej oparty na tej samej platformie pęcherzyków używanej do odczytu RNA.
Dlaczego to ma znaczenie dla przyszłych badań
Dla osób spoza specjalności kluczowa idea jest taka: NTVE pozwala naukowcom wielokrotnie pobierać „płynne biopsje” żywych komórek na szalkach, odczytując ich aktywność genową dzień po dniu bez poświęcania komórek. To przezwycięża główne ograniczenie standardowego profilowania RNA, gdzie każdy punkt czasowy wymaga nowej partii komórek i zaciera, jak pojedyncze komórki się zmieniają. Z NTVE każda kultura — a nawet każdy organoid — może służyć jako własna baza odniesienia, zwiększając moc wykrywania subtelnych zmian i umożliwiając bardziej precyzyjne długoterminowe badania rozwoju, modeli chorób i odpowiedzi na leki. Chociaż metoda koncentruje się obecnie na cytoplazmatycznych mRNA i jeszcze nie pozwala przypisać RNA z pęcherzyków do pojedynczych komórek, już dziś oferuje przystępny i wszechstronny sposób obserwacji molekularnego życia komórek w czasie rzeczywistym.
Cytowanie: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Słowa kluczowe: eksport RNA, transkryptomika komórek żywych, pęcherzyki zewnątrzkomórkowe, różnicowanie komórek macierzystych, dynamiczne zmiany ekspresji genów