Clear Sky Science · ru
Неразрушающая транскриптомика через везикулярный экспорт
Наблюдение за живыми клетками без их разрушения
Наши клетки постоянно включают и выключают гены, и учёные отслеживают эту активность, считывая РНК — молекулы-переносчики генетических инструкций. Но есть проблема: почти все существующие методы требуют разрушения клеток, поэтому каждое измерение уничтожает сами клетки, которые исследуются. В этой статье описан подход, позволяющий подслушивать «РНК‑разговоры» клетки в течение нескольких дней без вреда для неё, что открывает возможность наблюдать, как одни и те же клетки реагируют на лекарства или созревают в ткани вроде сердечной мышцы или нейронов.
Преобразование клеток в бережных посланцев
Исследователи разработали платформу, которую назвали неразрушающая транскриптомика через везикулярный экспорт (NTVE). Вместо того чтобы вскрывать клетки, NTVE побуждает их регулярно посылать крошечные пузырьки — везикулы, которые безопасно переносят образцы их РНК в окружающую среду. Эти везикулы формируют на основе упрощённой оболочки белка ВИЧ, которая естественно отщёлкивается от поверхности клетки. Добавив молекулярные «ручки» внутрь этой оболочки, команда обеспечивает втягивание РНК в образующиеся везикулы, а пометив поверхность везикул различимыми маркерами, можно позже разделять везикулы от разных типов клеток, растущих вместе. 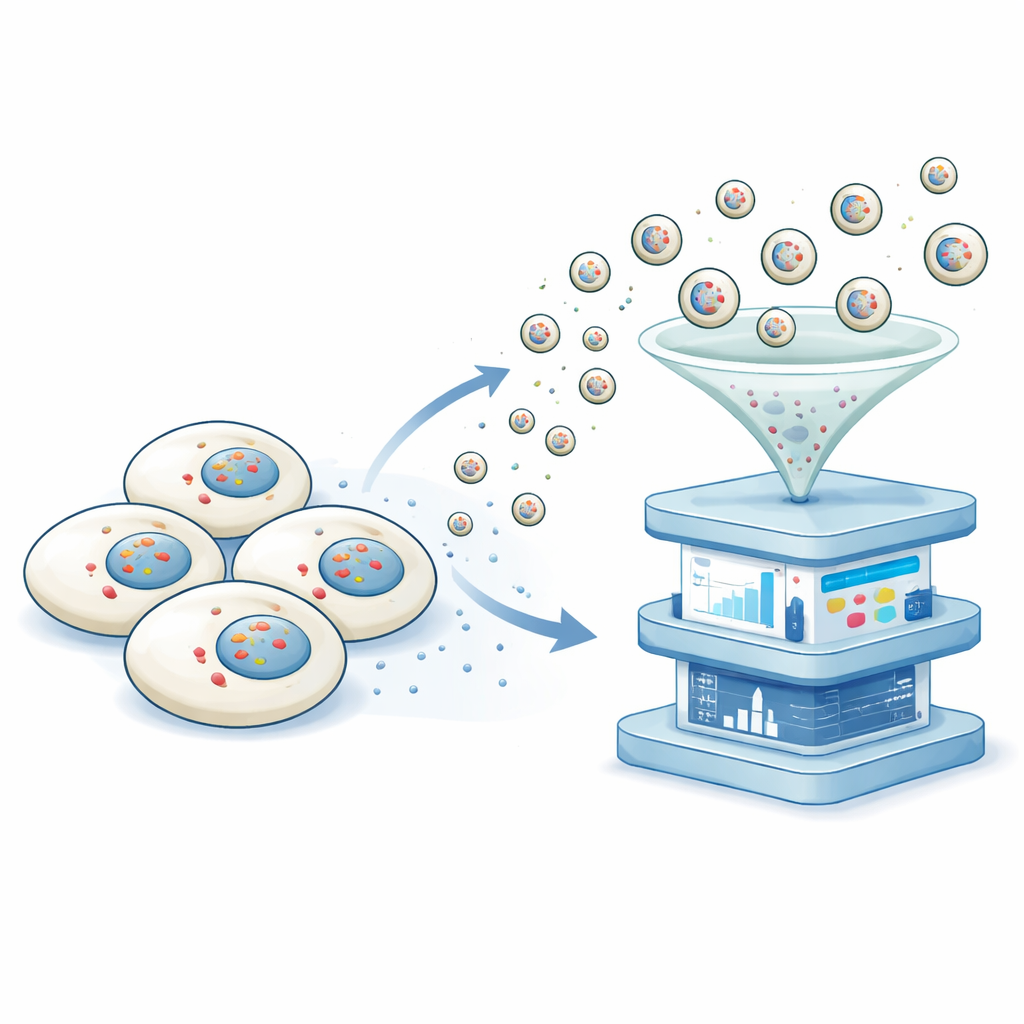
Фиксация полной картины РНК
Ключевая задача — убедиться, что экспортируемые везикулы действительно отражают то, что происходит внутри клетки, а не отбирают смещённый набор РНК или уносят повреждённый материал. Для этого авторы слили часть нормального клеточного белка, связывающего хвост большинства мРНК, с внутренней стороной везикулярной оболочки. Такая конструкция притягивает широкий и сбалансированный набор сообщений РНК из околосурфактных областей клетки. Сравнив РНК из везикул с РНК, полученной традиционным разрушающим способом из тех же клеток, они показали очень сильное соответствие более чем по 14 000 генов. Важно, что митохондриальные РНК, которые могли бы указывать на повреждение мембраны и утечку, были сильно обеднены, что предполагает, что клетки остаются целыми и здоровыми во время экспорта РНК.
Отслеживание клеток в процессе изменений
С NTVE команда проверила, можно ли с его помощью отслеживать реакцию клеток на хронологические стимулы. В человеческих клетках NTVE корректно фиксировал активацию одного «включённого» гена, вызванную активатором на основе CRISPR, а также близко сходился с традиционными методами при обработке клеток иммунным сигналом интерфероном‑гамма, отражая те же пути и ответные гены. Затем исследователи перешли к более деликатным системам: первичным нейронам мыши и человеческим стволовым клеткам. Упаковав механизмы NTVE в вирусные векторы или транспозоны, они создали линии нейронов и стволовых клеток, которые можно было индуцировать простым лекарственным веществом для запуска производства везикул. У нейронов NTVE зафиксировал волну активности генов, следующую за стимуляцией форсколином — соединением, известным активацией сигналов, связанных с памятью.
Наблюдение превращения стволовых клеток в ткани
Поскольку NTVE не уничтожает клетки, он особенно полезен для наблюдения медленных многодневных процессов, таких как дифференцировка стволовых клеток. Авторы модифицировали индуцированные плюрипотентные стволовые клетки человека для экспрессии NTVE и затем направили их по трём путям развития: к нервоподобной, мышечной и кишечной линиям. Ежедневно отбирая РНК из везикул, они реконструировали ветвящиеся траектории этих популяций клеток и оценивали, какие маркерные гены лучше всего различают каждую линию. В отдельном эксперименте они отслеживали созревание стволовых клеток в бьющиеся клетки сердца в течение девяти дней. Ежедневные измерения NTVE зафиксировали подъёмы и спады ключевых сердечных генов и показали, что всплеск маркеров, специфичных для сердца, совпал с первыми видимыми сокращениями. 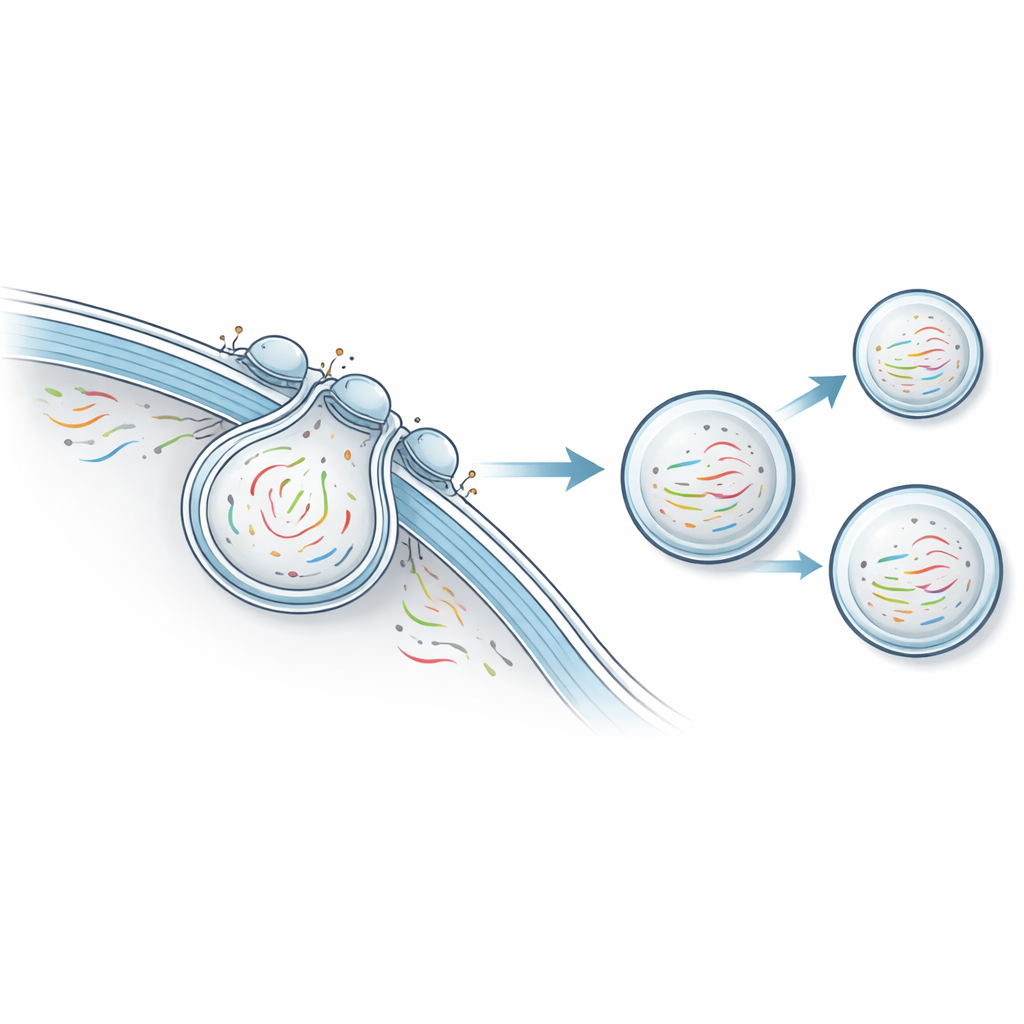
Передача сообщений между клетками
Помимо пассивного мониторинга, везикулы NTVE могут быть превращены в транспортные средства для доставки. Команда продемонстрировала, что везикулы можно загрузить мРНК или комплексами для редактирования генов и направлять к конкретным «приёмным» клеткам, используя вирусные оболочные белки в качестве целевых устройств. В ко‑культуре это позволило одной популяции отправлять везикулы, которые переключали генетические выключатели или переписывали ДНК в другой популяции, создавая программируемый канал для межклеточной коммуникации на той же платформе, что и для считывания РНК.
Почему это важно для будущих исследований
Для неспециалистов ключевая идея в том, что NTVE позволяет учёным многократно брать «жидкие биопсии» живых клеток в чашке Петри, считывая их генетическую активность день за днём, не жертвуя клетками. Это устраняет серьёзное ограничение стандартного РНК‑профилирования, где каждая временная точка требует новой партии клеток и скрывает, как индивидуальные клетки развиваются. С NTVE каждая культура — или даже каждый органоид — может служить собственной отправной точкой, повышая чувствительность к обнаружению тонких изменений и делая долгосрочные исследования развития, модельных заболеваний и ответов на лекарства более точными. Хотя метод в настоящий момент фокусируется на цитоплазматических мРНК и пока не позволяет привязывать везикулярную РНК к отдельным клеткам, он уже предлагает доступный и универсальный способ наблюдать молекулярную жизнь клеток в реальном времени.
Цитирование: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Ключевые слова: Экспорт РНК, транскриптомика живых клеток, внеклеточные везикулы, дифференцировка стволовых клеток, динамика экспрессии генов