Clear Sky Science · es
Transcriptómica no destructiva mediante exportación vesicular
Observar células vivas sin destruirlas
Nuestras células están constantemente activando y desactivando genes, y los científicos siguen esta actividad leyendo el ARN, las moléculas mensajeras que transportan las instrucciones genéticas. Pero hay un problema: casi todos los métodos actuales requieren romper las células, de modo que cada medición destruye las células que se estudian. Este trabajo presenta una forma de escuchar las conversaciones de ARN de una célula durante varios días sin dañarla, lo que abre la posibilidad de seguir cómo las mismas células responden a fármacos o maduran en tejidos como el músculo cardiaco o las neuronas.
Convertir las células en mensajeras delicadas
Los investigadores desarrollaron una plataforma que llaman transcriptómica no destructiva por exportación vesicular, o NTVE. En lugar de abrir las células, NTVE las induce a enviar regularmente pequeñas burbujas, o vesículas, que transportan de forma segura muestras de su ARN hacia el fluido circundante. Estas vesículas se construyen usando una forma reducida de la cubierta proteica del VIH que naturalmente brota de la superficie celular. Al añadir “asas” moleculares dentro de esta cubierta, el equipo asegura que las moléculas de ARN se incorporen a las vesículas en formación, y al añadir marcadores distintos en la superficie de las vesículas, luego pueden separar vesículas provenientes de distintos tipos celulares cultivados juntos. 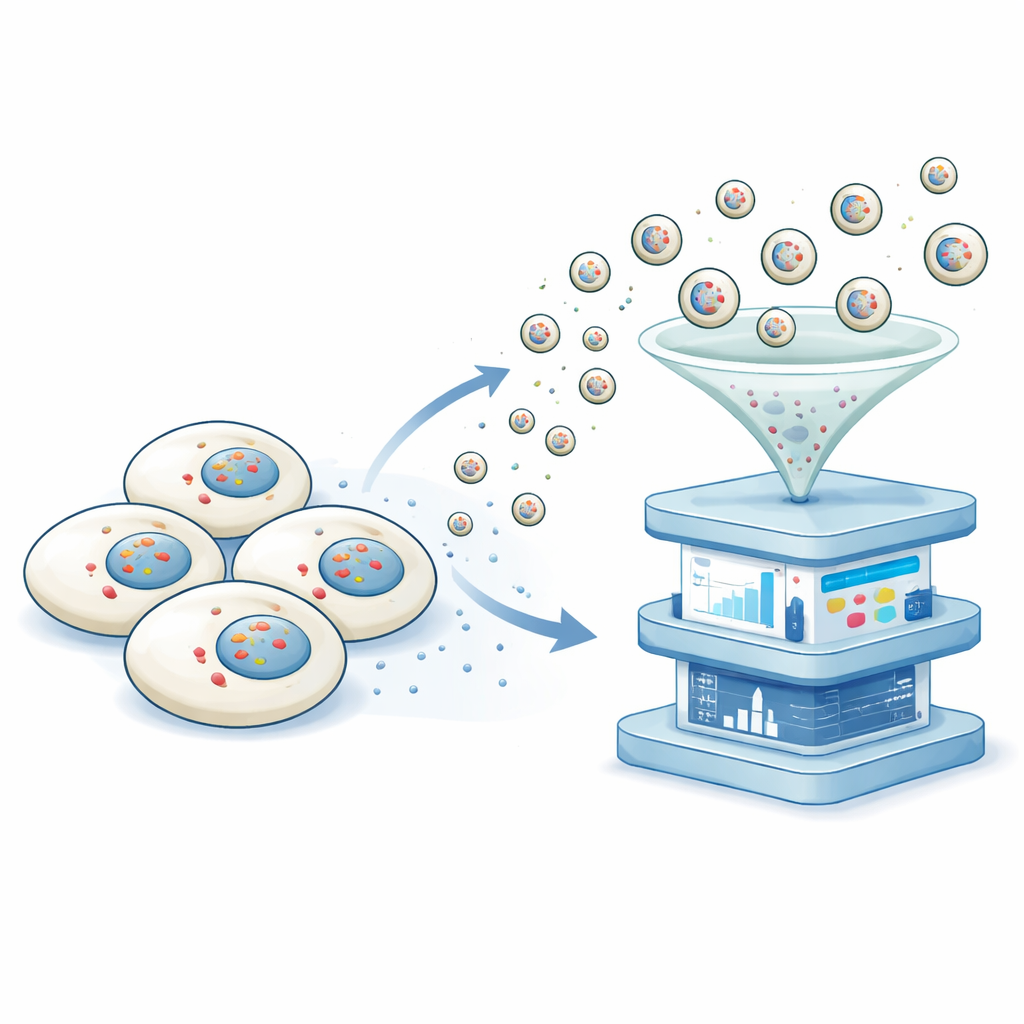
Captar el panorama completo del ARN
Un desafío clave es asegurarse de que estas vesículas exportadas reflejen fielmente lo que ocurre dentro de la célula, en lugar de recoger solo un subconjunto sesgado de ARN o filtrar material dañado. Para resolver esto, los autores fusionaron una parte de una proteína celular normal que se une a la cola de la mayoría de los ARN mensajeros al interior de la cubierta vesicular. Este diseño atrae una colección amplia y equilibrada de mensajes de ARN desde la proximidad de la superficie celular. Al comparar el ARN de las vesículas con el ARN obtenido por muestreo destructivo tradicional de las mismas células, mostraron una concordancia muy alta en más de 14.000 genes. Es importante que los ARN mitocondriales, que podrían indicar daño de membrana y fugas, estaban fuertemente deprimidos, lo que sugiere que las células permanecen intactas y sanas mientras exportan ARN.
Seguir a las células durante el cambio
Con NTVE en funcionamiento, el equipo probó si podía seguir cómo responden las células en el tiempo a estímulos específicos. En células humanas, NTVE informó correctamente la activación de un único gen «encendido» impulsado por un activador basado en CRISPR, y coincidió estrechamente con métodos convencionales cuando las células se expusieron a la señal inmune interferón gamma, capturando las mismas vías y genes de respuesta. Los investigadores pasaron luego a sistemas más delicados: neuronas primarias de ratón y células madre humanas. Al empaquetar la maquinaria NTVE en vectores virales o transposones, crearon líneas neuronales y de células madre que podían ser inducidas con un fármaco sencillo para iniciar la producción de vesículas. En neuronas, NTVE capturó la ola de actividad génica que sigue a la estimulación con forskolina, un compuesto conocido por activar señales relacionadas con la memoria.
Observar cómo las células madre se convierten en tejidos
Dado que NTVE no mata las células, es especialmente útil para observar procesos lentos de varios días como la diferenciación de células madre. Los autores diseñaron células madre pluripotentes inducidas humanas para expresar NTVE y luego las impulsaron por tres trayectorias de desarrollo: hacia linajes similares a nervios, músculo y mucosa intestinal. Al muestrear el ARN de las vesículas cada día, reconstruyeron las trayectorias ramificadas de estas poblaciones celulares y evaluaron qué genes marcadores distinguían mejor cada linaje. En un experimento separado, siguieron células madre madurando hasta convertirse en células cardiacas palpitantes durante nueve días. Las mediciones diarias con NTVE capturaron el ascenso y descenso de genes cardíacos clave y mostraron que el aumento de marcadores específicos del corazón coincidió con las primeras contracciones visibles. 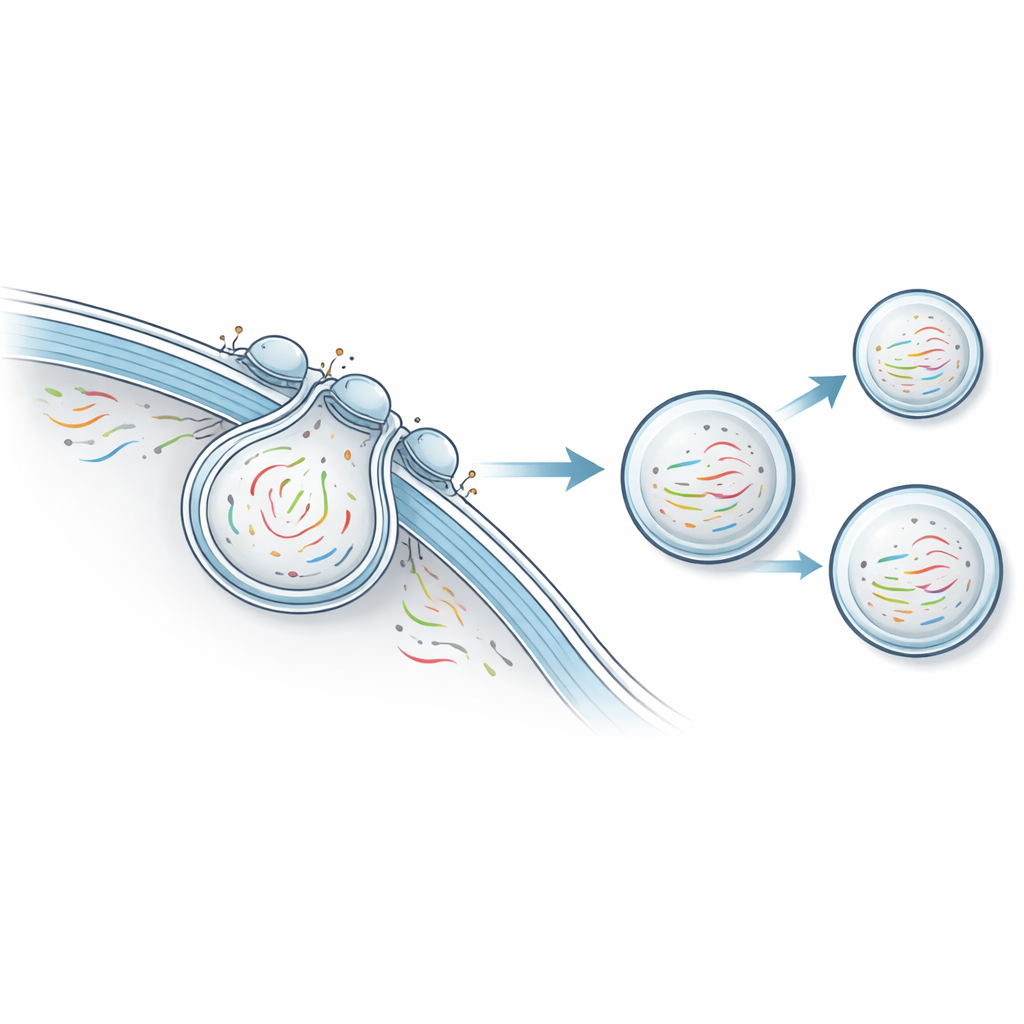
Enviar mensajes entre células
Más allá de la monitorización pasiva, las vesículas NTVE también pueden convertirse en vehículos de entrega. El equipo demostró que las vesículas podían cargarse con ARNm o complejos proteicos de edición génica y dirigirse a células «receptoras» específicas usando proteínas de la cubierta viral como dispositivos de direccionamiento. En cultivos mixtos, esto permitió que una población enviara vesículas que activaban interruptores genéticos o reescribían ADN en otra población, creando un canal programable de comunicación célula a célula que se apoya en la misma plataforma vesicular usada para la lectura de ARN.
Por qué esto importa para la investigación futura
Para los no especialistas, la idea clave es que NTVE permite a los científicos tomar repetidamente «biopsias líquidas» de células vivas en una placa, leyendo su actividad génica día tras día sin sacrificar las células. Esto supera una limitación importante del perfilado de ARN estándar, en el que cada punto temporal requiere un nuevo lote de células y oculta cómo evolucionan las células individuales. Con NTVE, cada cultivo—o incluso cada organoide—puede servir como su propia línea de base, mejorando la capacidad para detectar cambios sutiles y haciendo que los estudios a largo plazo de desarrollo, modelos de enfermedad y respuestas a fármacos sean más precisos. Aunque el método se centra actualmente en los ARN mensajeros citoplasmáticos y aún no puede asignar los ARN de las vesículas a células individuales, ya ofrece una forma accesible y versátil de observar la vida molecular de las células desarrollarse en tiempo real.
Cita: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Palabras clave: Exportación de ARN, transcriptómica en células vivas, vesículas extracelulares, diferenciación de células madre, dinámica de la expresión génica