Clear Sky Science · it
Trascrittomica non distruttiva tramite esportazione vesicolare
Osservare le cellule vive senza distruggerle
Le nostre cellule accendono e spengono continuamente geni, e gli scienziati tracciano questa attività leggendo l'RNA, le molecole messaggere che portano le istruzioni genetiche. Ma c'è una limitazione: quasi tutti i metodi attuali richiedono di aprire le cellule, dunque ogni misurazione distrugge le stesse cellule studiate. Questo articolo introduce un modo per ascoltare le conversazioni di RNA di una cellula per molti giorni senza danneggiarla, aprendo la possibilità di seguire come le stesse cellule rispondono a farmaci o maturano in tessuti come il muscolo cardiaco o i neuroni.
Trasformare le cellule in messaggere gentili
I ricercatori hanno sviluppato una piattaforma che chiamano trascrittomica non distruttiva tramite esportazione vesicolare, o NTVE. Invece di rompere le cellule, NTVE le induce a inviare regolarmente piccole bolle, o vescicole, che trasportano in modo sicuro campioni del loro RNA nel fluido circostante. Queste vescicole sono costruite usando una forma ridotta del guscio proteico dell'HIV che naturalmente si stacca dalla superficie cellulare. Aggiungendo maniglie molecolari all'interno di questo guscio, il gruppo si assicura che le molecole di RNA vengano convogliate nelle vescicole in formazione, e aggiungendo marcatori distinti sulla superficie delle vescicole possono poi separare vescicole provenienti da diversi tipi cellulari coltivati insieme. 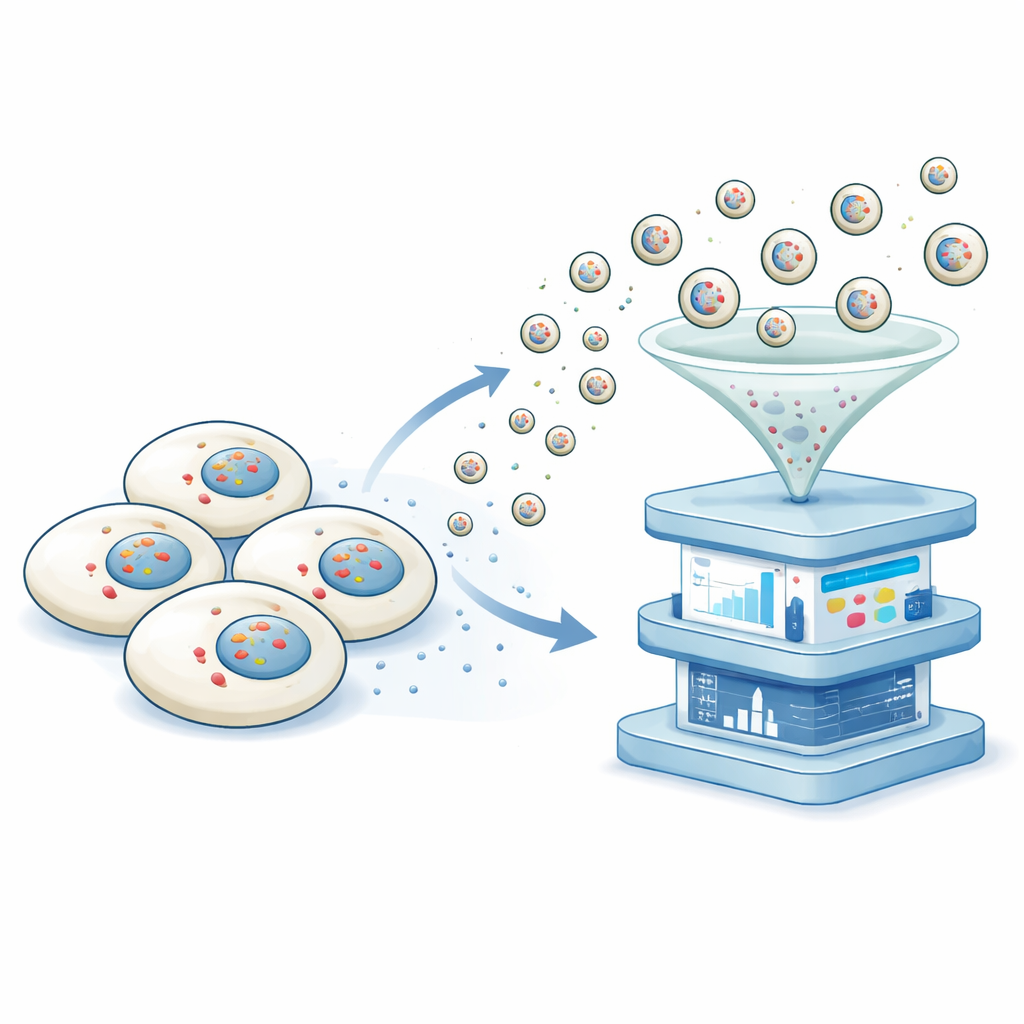
Catturare l'intero quadro dell'RNA
Una sfida chiave è assicurarsi che queste vescicole esportate riflettano davvero ciò che avviene all'interno della cellula, e non che raccolgano un sottoinsieme distorto di RNA o materiale danneggiato. Per risolvere questo problema, gli autori hanno fuso una parte di una proteina cellulare normale che si lega alla coda della maggior parte degli mRNA all'interno del guscio della vescicola. Questo design attira una raccolta ampia e bilanciata di messaggi RNA dalla zona vicina alla superficie cellulare. Confrontando l'RNA delle vescicole con l'RNA ottenuto tramite campionamento distruttivo tradizionale delle stesse cellule, hanno mostrato una forte corrispondenza su oltre 14.000 geni. Importante, gli RNA mitocondriali, che potrebbero indicare danni alla membrana e perdite, risultavano fortemente depauperati, suggerendo che le cellule rimangono integre e sane mentre esportano RNA.
Seguire le cellule durante il cambiamento
Con NTVE in funzione, il gruppo ha testato se potesse tracciare come le cellule rispondono nel tempo a stimoli specifici. In cellule umane, NTVE ha riportato correttamente l'attivazione di un singolo gene «acceso» guidato da un attivatore basato su CRISPR, e ha rispecchiato da vicino i metodi convenzionali quando le cellule sono state esposte al segnale immunitario interferone-gamma, catturando le stesse vie e geni di risposta. I ricercatori sono poi passati a sistemi più delicati: neuroni primari di topo e cellule staminali umane. Impacchettando la macchina NTVE in vettori virali o transposoni, hanno creato linee di neuroni e cellule staminali che potevano essere indotte con un semplice farmaco a iniziare la produzione di vescicole. Nei neuroni, NTVE ha catturato l'ondata di attività genica che segue la stimolazione con forskolina, un composto noto per attivare segnali legati alla memoria.
Osservare le cellule staminali diventare tessuti
Poiché NTVE non uccide le cellule, è particolarmente potente per osservare processi lenti e plurigiornalieri come la differenziazione delle cellule staminali. Gli autori hanno ingegnerizzato cellule staminali pluripotenti indotte umane per esprimere NTVE e poi le hanno indirizzate lungo tre percorsi di sviluppo: verso linee simili a nervi, a muscolo e a intestino. Campionando l'RNA delle vescicole ogni giorno, hanno ricostruito le traiettorie ramificate di queste popolazioni cellulari e valutato quali geni marcatore distinguessero meglio ciascuna linea. In un esperimento separato, hanno seguito cellule staminali in maturazione in cellule cardiache battenti per nove giorni. Le misurazioni giornaliere con NTVE hanno catturato l'aumento e il calo di geni cardiaci chiave e hanno mostrato che l'impennata dei marcatori specifici del cuore coincideva con le prime contrazioni visibili. 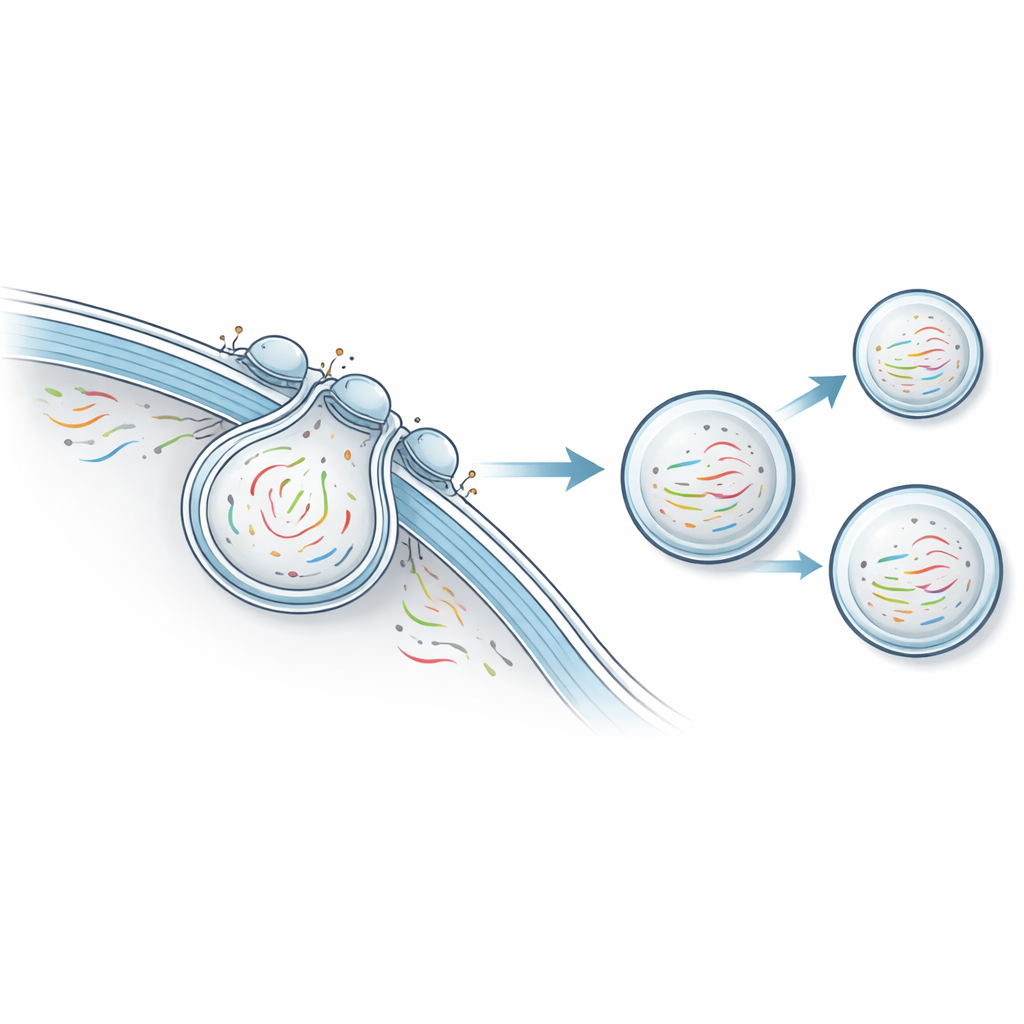
Inviare messaggi tra le cellule
Oltre al monitoraggio passivo, le vescicole NTVE possono anche essere trasformate in veicoli di consegna. Il team ha dimostrato che le vescicole possono essere caricate con mRNA o complessi proteici per l'editing genico e indirizzate a specifiche cellule «riceventi» usando proteine del rivestimento virale come dispositivi di targeting. Nelle co-colture, questo ha permesso a una popolazione di inviare vescicole che attivavano interruttori genetici o riscrivevano il DNA in un'altra popolazione, creando un canale programmabile di comunicazione cellula-cellula che sfrutta la stessa piattaforma vesicolare usata per la lettura dell'RNA.
Perché questo è importante per la ricerca futura
Per i non specialisti, l'idea chiave è che NTVE permette agli scienziati di effettuare ripetute «biopsie liquide» di cellule vive in una piastra, leggendo la loro attività genica giorno dopo giorno senza sacrificare le cellule. Questo supera un grande limite del profilo RNA standard, dove ogni punto temporale richiede un nuovo lotto di cellule e rende opaco come singole cellule si evolvono. Con NTVE, ogni coltura — o anche ogni organoide — può fungere da proprio riferimento di base, migliorando la capacità di rilevare cambiamenti sottili e rendendo più precise le indagini a lungo termine su sviluppo, modelli di malattia e risposte ai farmaci. Sebbene il metodo si concentri attualmente sugli mRNA citoplasmatici e non possa ancora assegnare gli RNA delle vescicole a singole cellule, offre già un modo accessibile e versatile per osservare la vita molecolare delle cellule mentre si svolge in tempo reale.
Citazione: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Parole chiave: Esportazione di RNA, trascrittomica in cellule vive, vescicole extracellulari, differenziazione delle cellule staminali, dinamiche dell'espressione genica