Clear Sky Science · de
Nicht-destruktive Transkriptomik über vesikulären Export
Lebende Zellen beobachten, ohne sie zu zerstören
Unsere Zellen schalten ständig Gene an und aus; Wissenschaftler verfolgen diese Aktivität, indem sie die RNA lesen, die Botenmoleküle, die genetische Anweisungen tragen. Es gibt jedoch einen Haken: Fast alle aktuellen Methoden erfordern, dass Zellen aufgebrochen werden, sodass jede Messung genau die Zellen zerstört, die untersucht werden sollen. Diese Arbeit stellt eine Methode vor, mit der man die RNA‑Konversationen einer Zelle über viele Tage belauschen kann, ohne die Zellen zu schädigen — und eröffnet damit die Möglichkeit, nachzuvollziehen, wie dieselben Zellen auf Medikamente reagieren oder sich zu Geweben wie Herzmuskel oder Neuronen entwickeln.
Zellen in sanfte Boten verwandeln
Die Forscher entwickelten eine Plattform, die sie nicht-destruktive Transkriptomik durch vesikulären Export nennen, kurz NTVE. Statt Zellen aufzubrechen, veranlasst NTVE sie, regelmäßig winzige Bläschen oder Vesikel auszusenden, die sicher Proben ihrer RNA in die umgebende Flüssigkeit transportieren. Diese Vesikel werden mithilfe einer entkern-ten Form einer HIV-Proteinhülle aufgebaut, die natürlicherweise von der Zelloberfläche abschnürt. Durch das Hinzufügen molekularer „Griffe“ in dieser Hülle sorgt das Team dafür, dass RNA‑Moleküle in die entstehenden Vesikel gezogen werden, und durch das Anbringen unterschiedlicher Marker auf der Vesikeloberfläche lassen sich später Vesikel verschiedener Zelltypen, die zusammen kultiviert wurden, voneinander trennen. 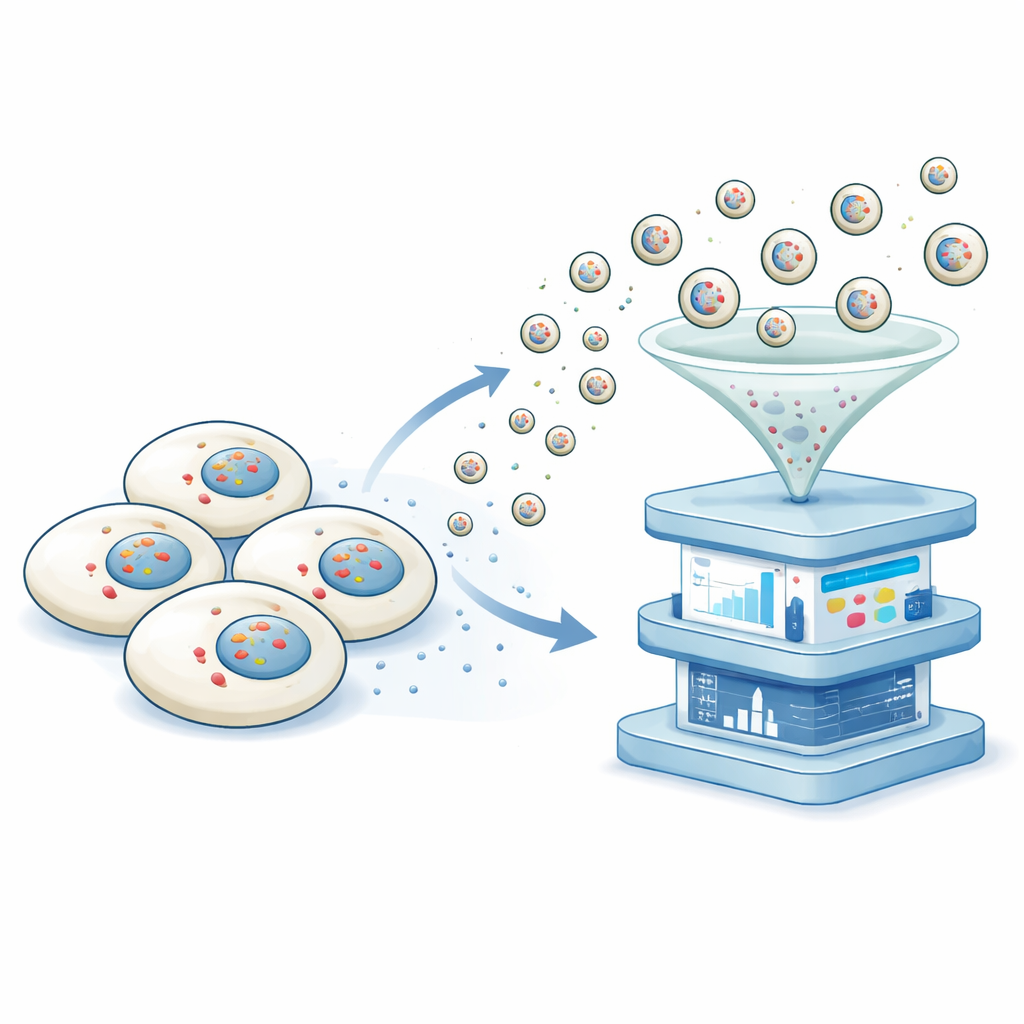
Das vollständige RNA‑Bild einfangen
Eine zentrale Herausforderung besteht darin sicherzustellen, dass diese exportierten Vesikel tatsächlich widerspiegeln, was in der Zelle vor sich geht, statt nur eine verzerrte Untergruppe von RNAs zu erfassen oder beschädigtes Material zu lecken. Um das zu lösen, fusionierten die Autorinnen und Autoren einen Teil eines normalen zellulären Proteins, das an das Ende der meisten Boten-RNAs bindet, an die Innenseite der Vesikelhülle. Dieses Design zieht eine breite und ausgewogene Sammlung von RNA‑Botschaften aus der Nähe der Zelloberfläche an. Durch den Vergleich der RNA aus Vesikeln mit der RNA aus herkömmlichen destruktiven Proben derselben Zellen zeigten sie eine sehr starke Übereinstimmung über mehr als 14.000 Gene hinweg. Wichtig ist, dass mitochondriale RNAs, die auf Membranschäden und Leckagen hindeuten könnten, stark vermindert waren, was darauf schließen lässt, dass die Zellen intakt und gesund bleiben, während sie RNA exportieren.
Zellen beim Wandel folgen
Mit NTVE prüfte das Team, ob sich damit verfolgen lässt, wie Zellen zeitlich auf bestimmte Auslöser reagieren. In menschlichen Zellen meldete NTVE korrekt die Aktivierung eines einzelnen „eingeschalteten“ Gens, das von einem CRISPR‑basierten Aktivator gesteuert wurde, und stimmte eng mit konventionellen Methoden überein, als Zellen dem Immunsignal Interferon‑gamma ausgesetzt wurden, wobei dieselben Signalwege und Antwortgene erfasst wurden. Die Forschenden gingen dann zu empfindlicheren Systemen über: primäre Mausneuronen und menschliche Stammzellen. Indem sie die NTVE‑Maschinerie in viralen Vektoren oder Transposons verpackten, erzeugten sie Neuronen‑ und Stammzelllinien, die durch ein einfaches Medikament zur Vesikelproduktion angeregt werden konnten. In Neuronen zeichnete NTVE die Genaktivitätswelle auf, die nach Stimulation mit Forskolin folgt — einer Verbindung, die dafür bekannt ist, gedächtnisbezogene Signalwege zu aktivieren.
Beobachtung, wie Stammzellen zu Geweben werden
Da NTVE die Zellen nicht tötet, ist die Methode besonders geeignet, langsame, mehrtägige Prozesse wie die Differenzierung von Stammzellen zu beobachten. Die Autoren konstruierten menschliche induzierte pluripotente Stammzellen, die NTVE exprimierten, und leiteten sie dann in drei Entwicklungsrichtungen: zu nervenähnlichen, muskelähnlichen und darmähnlichen Linien. Durch tägliche Probenahme der Vesikel‑RNA rekonstruierten sie die verzweigenden Entwicklungsverläufe dieser Zellpopulationen und bewerteten, welche Markergene jede Linie am besten unterscheiden. In einem separaten Experiment verfolgten sie Stammzellen, die sich über neun Tage zu schlagenden Herzmuskelzellen entwickelten. Tägliche NTVE‑Messungen zeichneten das Auf- und Ab wichtiger kardialer Gene auf und zeigten, dass der Anstieg herzspezifischer Marker mit den ersten sichtbaren Kontraktionen zusammenfiel. 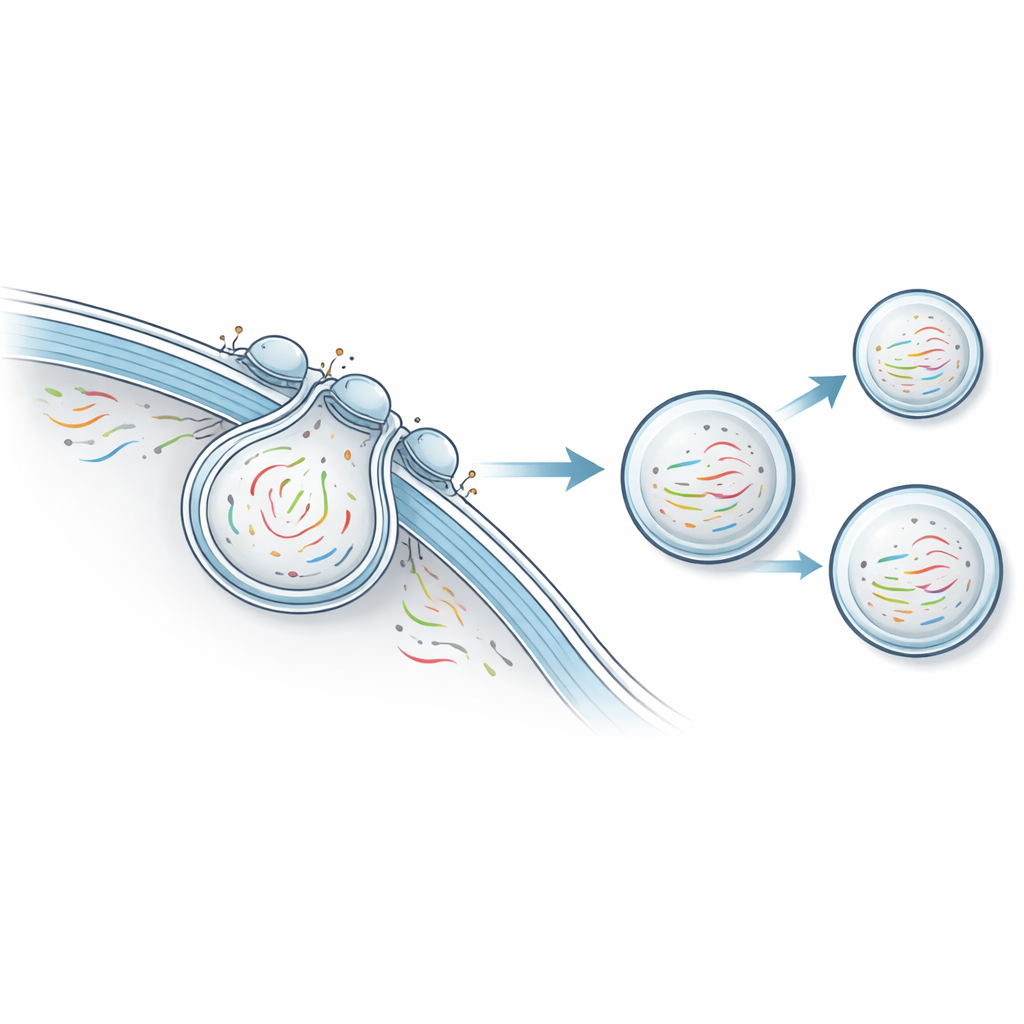
Nachrichten zwischen Zellen senden
Über passives Monitoring hinaus lassen sich NTVE‑Vesikel auch als Transportvehikel nutzen. Das Team zeigte, dass Vesikel mit Boten‑RNAs oder Geneditier‑Proteinkomplexen beladen und mithilfe viraler Hüllproteine als Zielscheiben auf bestimmte „Empfänger“zellen gerichtet werden können. In Ko‑Kulturen ermöglichte dies einer Population, Vesikel zu senden, die genetische Schalter in einer anderen Population umlegten oder DNA umschrieben — und schuf so einen programmierbaren Kanal für Zell‑zu‑Zell‑Kommunikation, der auf derselben Vesikelplattform basiert, die auch für die RNA‑Auslese genutzt wird.
Warum das für zukünftige Forschung wichtig ist
Für Nicht‑Spezialisten besteht die Kernidee darin, dass NTVE es Forschern erlaubt, wiederholt „Flüssigbiopsien" lebender Zellen in einer Kultur durchzuführen und ihre Genaktivität Tag für Tag zu lesen, ohne die Zellen zu opfern. Das überwindet eine wichtige Einschränkung der üblichen RNA‑Profile, bei denen jeder Zeitpunkt eine neue Zellcharge erfordert und verbirgt, wie einzelne Zellen sich entwickeln. Mit NTVE kann jede Kultur — oder sogar jedes Organoid — als eigene Grundlage dienen, was die Sensitivität für subtile Veränderungen erhöht und Langzeitstudien zu Entwicklung, Krankheitsmodellen und Wirkstoffreaktionen präziser macht. Obwohl die Methode derzeit auf zytoplasmatische Boten‑RNAs fokussiert ist und Vesikel‑RNA noch nicht einzelnen Zellen zugeordnet werden kann, bietet sie bereits einen zugänglichen und vielseitigen Weg, das molekulare Leben von Zellen in Echtzeit zu verfolgen.
Zitation: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Schlüsselwörter: RNA-Export, Lebendzell-Transkriptomik, extrazelluläre Vesikel, Stammzell-Differenzierung, Dynamik der Genexpression