Clear Sky Science · sv
Icke-destruktiv transkriptomik via vesikulär export
Att iaktta levande celler utan att bryta sönder dem
Våra celler slår ständigt på och av gener, och forskare följer denna aktivitet genom att läsa av RNA — budbärarmolekylerna som bär genetiska instruktioner. Men det finns ett problem: nästan alla nuvarande metoder kräver att celler öppnas, så varje mätning förstör de celler som studeras. Denna artikel presenterar ett sätt att lyssna på en cells RNA-samtal över många dagar utan att skada cellerna, vilket öppnar dörren för att följa hur samma celler reagerar på läkemedel eller mognar till vävnader som hjärtmuskel eller neuroner.
Att förvandla celler till varsamma budbärare
Forskarna utvecklade en plattform som de kallar icke-destruktiv transkriptomik via vesikulär export, eller NTVE. Istället för att krossa cellerna får NTVE dem att regelbundet skicka ut små bubblor, eller vesiklar, som säkert bär prover av deras RNA ut i omgivande vätska. Dessa vesiklar byggs med en avskalad form av ett HIV-proteinskal som naturligt knoppas av från cellens yta. Genom att lägga till molekylära ”handtag” inne i detta skal ser teamet till att RNA-molekyler dras in i de knoppande vesiklarna, och genom att fästa särskilda markörer på vesiklarnas yta kan de senare separera vesiklar från olika celltyper som odlas tillsammans. 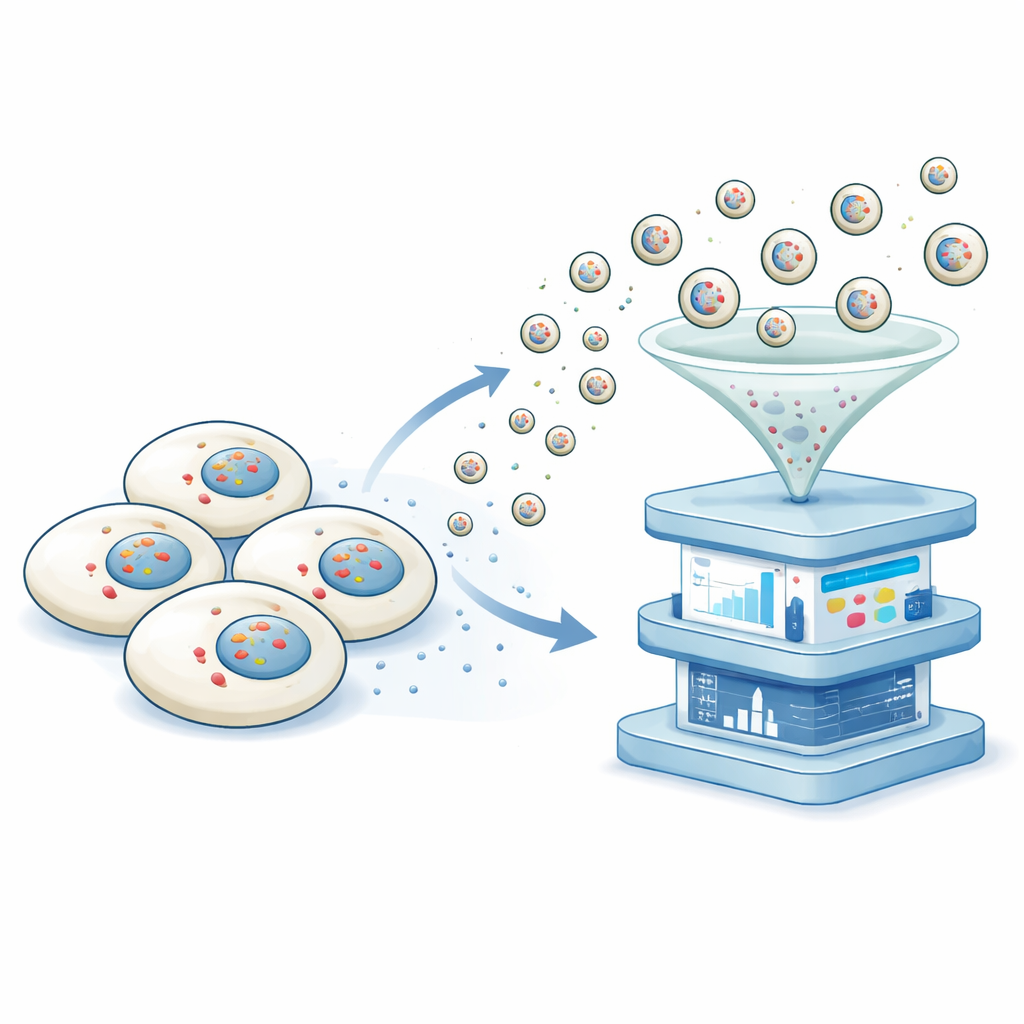
Att fånga hela RNA-bilden
En viktig utmaning är att försäkra sig om att dessa exporterade vesiklar verkligen speglar vad som händer inne i cellen, snarare än att bara fånga en partisk undergrupp av RNA eller läcka skadat material. För att lösa detta fäste författarna en del av ett normalt cellprotein som binder till svansen på de flesta budbärar-RNA på insidan av vesikelskalet. Denna konstruktion drar in en bred och balanserad samling av RNA-meddelanden från nära cellens yta. Genom att jämföra RNA från vesiklar med RNA från traditionell destruktiv provtagning av samma celler visade de mycket stark överensstämmelse över mer än 14 000 gener. Viktigt är att mitokondriellt RNA, vilket kan indikera membranskada och läckage, var starkt utarmat, vilket tyder på att cellerna förblir intakta och friska medan de exporterar RNA.
Att följa celler genom förändring
Med NTVE på plats testade teamet om metoden kunde spåra hur celler reagerar över tid på specifika pådrivare. I humana celler rapporterade NTVE korrekt aktiveringen av en enskild ”påslagen” gen som drevs av en CRISPR-baserad aktivator, och den matchade nära konventionella metoder när celler exponerades för immunsignalen interferon-gamma, och fångade samma vägar och responsgener. Forskarna gick sedan vidare till mer känsliga system: primära musneuroner och humana stamceller. Genom att paketera NTVE-mekaniken i virusvektorer eller transposoner skapade de neuron- och stamcellsrader som kunde induceras med ett enkelt läkemedel för att starta vesikelproduktion. I neuroner fångade NTVE vågen av genaktivitet som följer stimulering med forskolin, en förening känd för att aktivera minnesrelaterad signalering.
Att iaktta stamceller bli vävnader
Eftersom NTVE inte dödar celler är metoden särskilt kraftfull för att följa långsamma, flerdagarsprocesser som stamcellsdifferentiering. Författarna konstruerade humana inducerade pluripotenta stamceller att uttrycka NTVE och drev dem sedan längs tre utvecklingsvägar: mot nervliknande, muskelliknande och tarmliknande linjer. Genom att ta prover av vesikel-RNA varje dag rekonstruerade de förgreningstrajektorierna för dessa cellpopulationer och utvärderade vilka markörgener som bäst särskiljde varje linje. I ett separat experiment följde de stamceller som mognade till slagande hjärtceller över nio dagar. Dagliga NTVE-mätningar fångade uppgången och nedgången av viktiga kardiella gener och visade att ökningen i hjärtspecifika markörer sammanföll med de första synliga sammandragningarna. 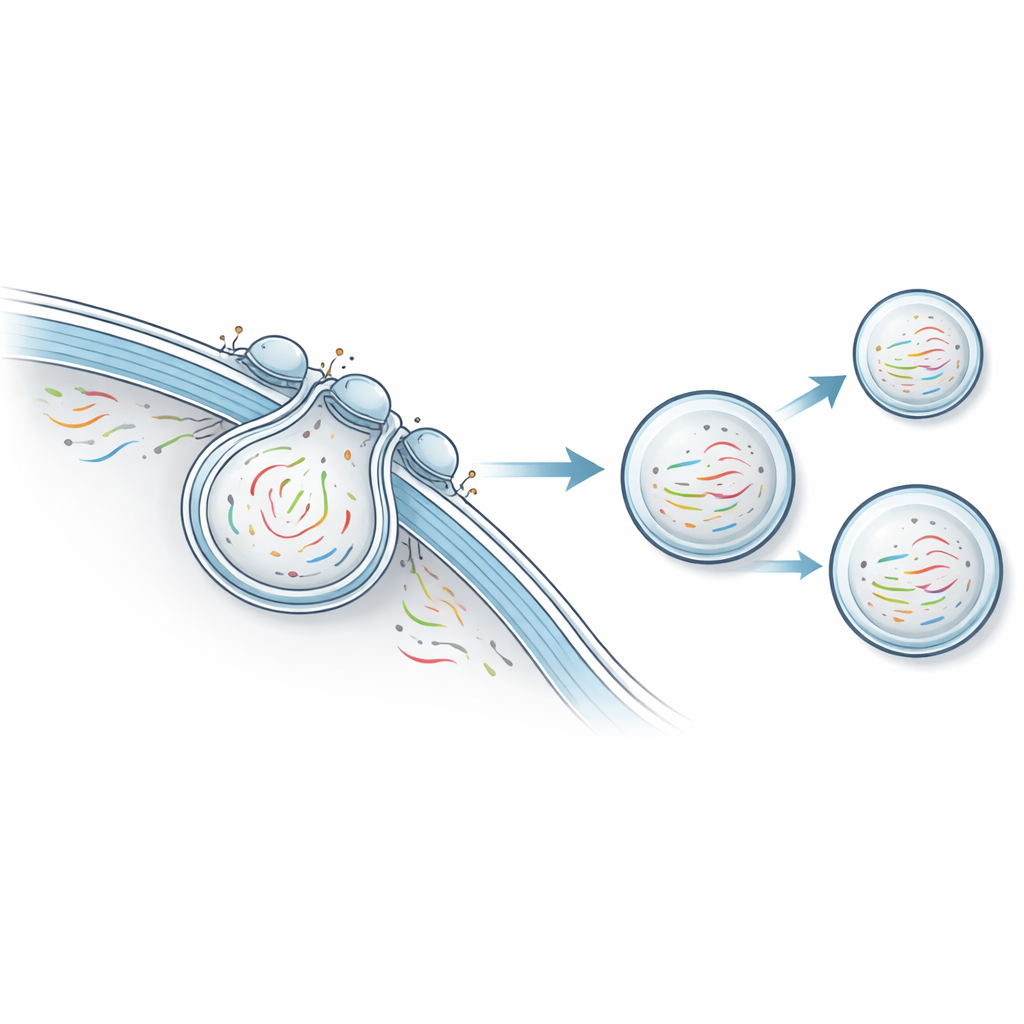
Att skicka meddelanden mellan celler
Utöver passiv övervakning kan NTVE-vesiklar också göras om till leveransfordon. Teamet visade att vesiklar kunde lastas med budbärar-RNA eller genredigerande proteinkomplex och riktas mot specifika ”mottagar”-celler med hjälp av viruskapselproteiner som målinriktningsanordningar. I medodlade celler gjorde detta det möjligt för en population att skicka vesiklar som slog på genetiska brytare eller skrev om DNA i en annan population, och skapade en programmerbar kanal för cell-till-cell-kommunikation som bygger på samma vesikelplattform som används för RNA-avläsning.
Varför detta är viktigt för framtida forskning
För icke-specialister är huvudidén att NTVE låter forskare upprepade gånger ta ”flytande biopsier” av levande celler i en odling, läsa deras genaktivitet dag efter dag utan att offra cellerna. Detta övervinner en viktig begränsning i standard RNA-profilering, där varje tidpunkt kräver ett nytt parti celler och döljer hur individuella celler utvecklas. Med NTVE kan varje kultur — eller till och med varje organoid — fungera som sin egen baslinje, vilket ökar känsligheten för att upptäcka subtila förändringar och gör långtidsstudier av utveckling, sjukdomsmodeller och läkemedelssvar mer precisa. Även om metoden för närvarande fokuserar på cytoplasmatiska budbärar-RNA och ännu inte kan tilldela vesikel-RNA till enskilda celler, erbjuder den redan ett tillgängligt och mångsidigt sätt att se cellernas molekylära liv veckla ut i realtid.
Citering: Armbrust, N., Grosshauser, M., Geilenkeuser, J. et al. Non-destructive transcriptomics via vesicular export. Nat Commun 17, 3812 (2026). https://doi.org/10.1038/s41467-026-72072-w
Nyckelord: RNA-export, levande cell-transkriptomik, extracellulära vesiklar, stamcellsdifferentiering, genuttrycks-dynamik