Clear Sky Science · zh
MeCP2基因剂量依赖的神经发育受限缺陷通过细胞命运决定双价基因的异常激活产生
为何此基因与大脑健康相关
MECP2基因广为人知:其蛋白质不足会导致雷特综合征,而过量则引起MeCP2重复综合征。两种疾病都会带来严重问题,如智力障碍、癫痫和运动障碍。本研究提出了一个看似简单但对未来基因疗法影响深远的问题:额外的MeCP2是否总是有害,还是其出现的时机和细胞类型决定了大脑是否受损或得以幸免?
当额外的MeCP2过早出现
研究者比较了在未成熟的“神经祖细胞”与成熟神经元中过量表达MeCP2会产生何种不同后果,采用了小鼠和人类细胞。神经祖细胞是发育中大脑中可分裂的细胞,后来会产生神经元。当团队在这些祖细胞中提升MeCP2时,细胞的基因活动发生了显著改变:数千个基因表达升高或降低,并明显偏向激活那些推动细胞分化为神经元的基因。在培养皿和发育中的小鼠大脑中,MeCP2过量的祖细胞减慢了增殖并更早、更迅速地转变为神经元,从而改变了大脑发育的步调。
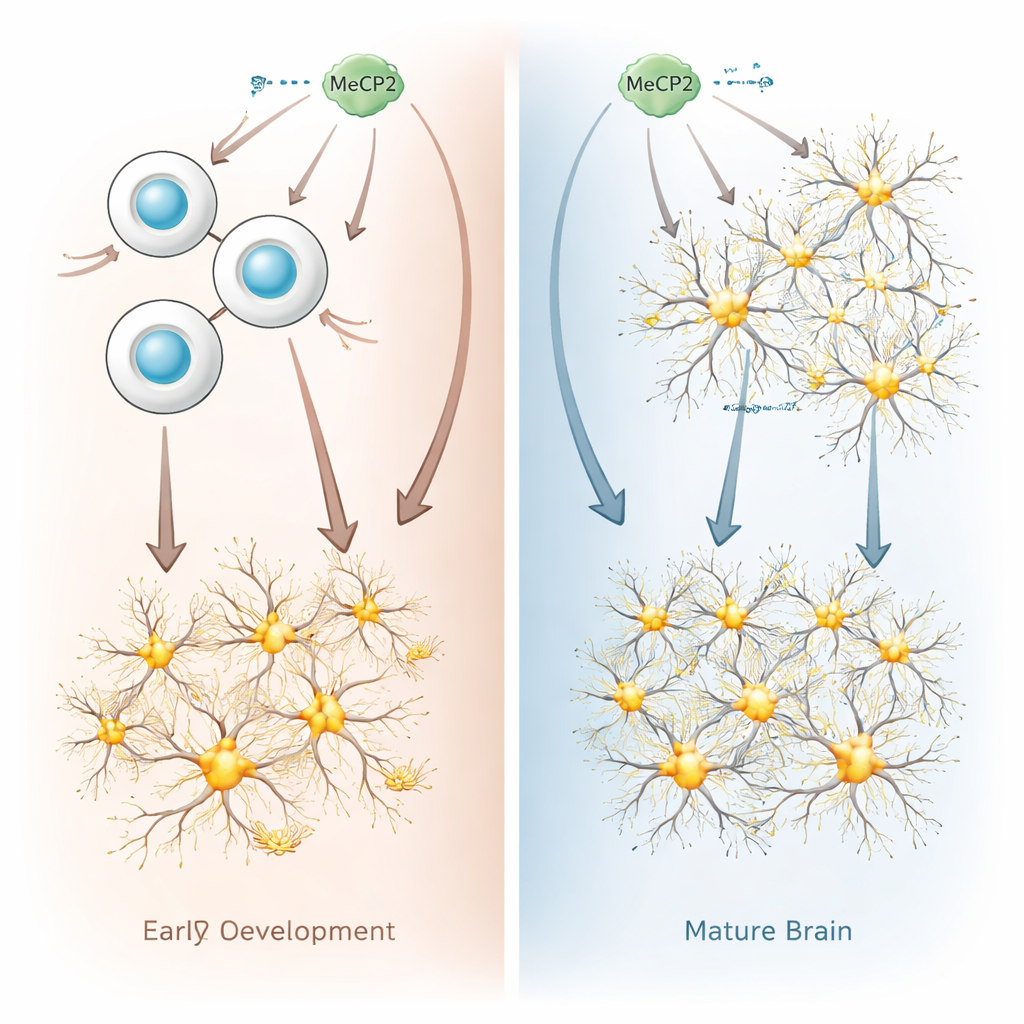
为何成熟神经元对额外MeCP2无动于衷
形成鲜明对比的是,当相同量的MeCP2被加入到成熟神经元时,影响出人意料地轻微。仅有几百个基因的活性发生变化,而且多数变化很小。研究者也几乎未发现这些神经元中总体DNA包装发生改变的证据。在活体小鼠中,于胚胎期祖细胞中提高MeCP2会产生具有更强兴奋性电信号的成年神经元,这与重复综合征模型中的观察一致。但直接在成年大脑中提升MeCP2并未改变神经元的电活动。综上,这些结果表明成熟神经元对MeCP2增加的耐受性远高于发育中的祖细胞。
MeCP2如何选择其在DNA上的位置
为了解为何细胞类型差异如此显著,团队精确绘制了正常和额外MeCP2分子在DNA上的结合位点。在祖细胞和神经元中,MeCP2都倾向于定位于富含“CpG岛”的DNA片段,位于基因起始位点附近——这些区域有助于控制基因的开启或关闭。正常与过量的蛋白质基本选择了相同的一组靶点,尤其是那些参与构建和精修神经回路的基因。关键区别在于这些位点的占据程度。在天然MeCP2本就丰富的神经元中,这些位点几乎被饱和,留给额外蛋白的空间很小,额外蛋白结合较弱并更快被降解。而在MeCP2水平通常较低的祖细胞中,加入的蛋白质可以在这些调控区更强且更广泛地结合。
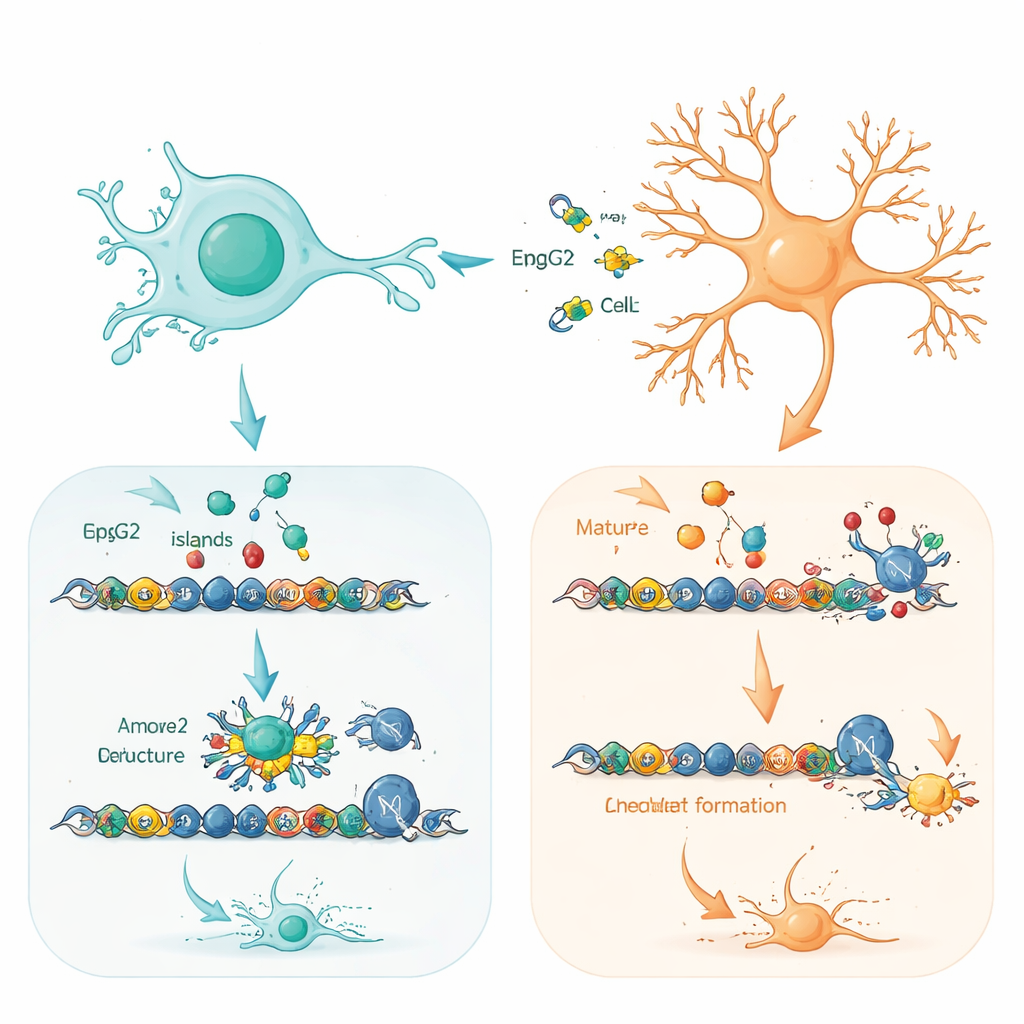
在幼年脑细胞中为命运决定基因“预设”
一个特别显著的发现是,许多在祖细胞中受影响最严重的基因处于“待激活”状态:它们在调控区同时带有激活和抑制的化学标记,随发育推进随时可被打开。这类双价基因常常控制关于何种类型神经元被制造以及何时被制造的关键决策。作者显示,过量的MeCP2有助于将一个强大的DNA包装机器——SWI/SNF复合体——招募到这些待激活位点。这种联手使得激活的天平倾斜,过早解锁整套神经分化程序。支持这一图景的还有对更广泛DNA包装景观的细微变化:与细胞周期控制和神经元成熟相关的区域在MeCP2过量的祖细胞中变得略微更开放。
这对基因疗法与脑部疾病意味着什么
对于担心基于MeCP2的基因疗法可能产生过量并损害大脑的家庭和临床医生,这项工作提供了谨慎的宽慰。研究表明,在成熟神经元中适度增加MeCP2——即便是3到4倍——出人意料地能被很好地耐受,因为结合位点已被占据且多余的蛋白会迅速被清除。真正的危险似乎出现在发育早期,当MeCP2在命运仍待决定且高度敏感的祖细胞中被提升。在这种情况下,额外的MeCP2可能过早激活发育程序,改变神经元生成的方式和时间,最终改变大脑连线,可能促成MECP2重复综合征中看到的癫痫和其他症状。更广泛地说,这些发现强调了一个可能为许多染色质调控因子所共有的原则:基因剂量本身并非固有有毒,其影响关键上取决于发育时期以及不平衡发生的细胞类型。
引用: Luoni, M., Kubacki, M., Giannelli, S.G. et al. MeCP2 gene dosage-dependent neurodevelopmentally restricted defects arise by aberrant activation of cell fate-determining bivalent genes. Nat Commun 17, 3225 (2026). https://doi.org/10.1038/s41467-026-71432-w
关键词: MeCP2, 神经发育, 基因剂量, 表观遗传学, 基因疗法