Clear Sky Science · es
Defectos restringidos al neurodesarrollo dependientes de la dosis del gen MeCP2 surgen por la activación aberrante de genes bivalentes que determinan el destino celular
Por qué este gen importa para la salud cerebral
El gen MECP2 es conocido porque la falta de su proteína causa el síndrome de Rett, mientras que su exceso conduce al síndrome de duplicación de MECP2. Ambas condiciones provocan problemas graves como discapacidad intelectual, convulsiones y trastornos del movimiento. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones para futuras terapias génicas: ¿es siempre peligroso tener MeCP2 de más, o el momento y el tipo celular en que aparece determinan si el cerebro resulta dañado o protegido?
Cuando el exceso de MeCP2 aparece demasiado pronto
Los investigadores compararon lo que ocurre cuando MeCP2 se sobreproduce en células inmaduras «progenitoras neurales» frente a neuronas ya formadas, usando células tanto de ratón como humanas. Las progenitores neurales son las células en división del cerebro en desarrollo que más tarde darán lugar a neuronas. Cuando el equipo aumentó MeCP2 en estas progenitoras, la actividad genética de las células cambió de forma drástica: miles de genes se activaron o reprimieron, con un marcado sesgo hacia la activación de genes que impulsan a las células a convertirse en neuronas. En cultivos y en cerebros de ratón en desarrollo, las progenitoras con exceso de MeCP2 dejaron de dividirse tanto y se convirtieron en neuronas antes y más rápidamente de lo normal, desplazando el ritmo del desarrollo cerebral.
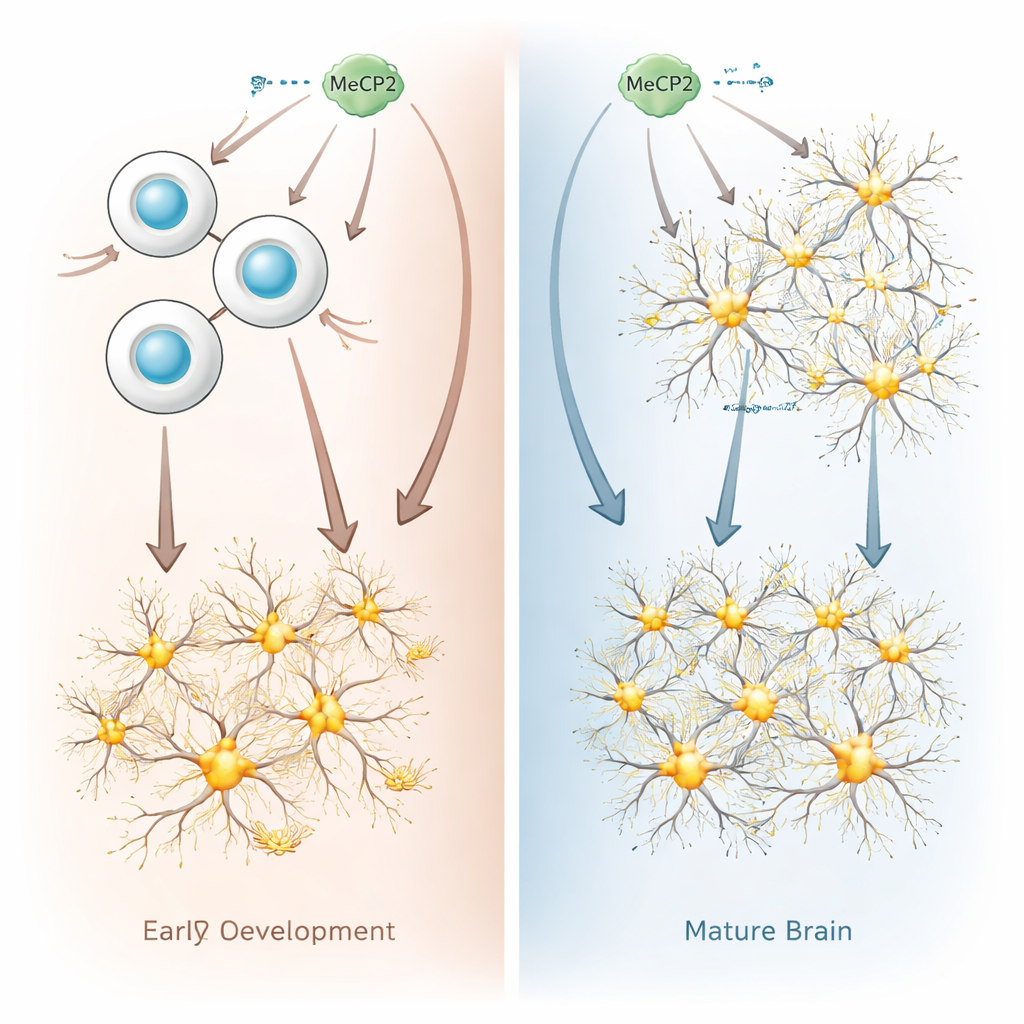
Por qué las neuronas maduras toleran el exceso de MeCP2
En marcado contraste, cuando la misma cantidad de MeCP2 se añadió a neuronas maduras, los efectos fueron sorprendentemente leves. Solo unos pocos centenares de genes cambiaron su actividad, y la mayoría de esos cambios fue pequeña. Los investigadores también hallaron poca evidencia de que el empaquetamiento global del ADN en estas neuronas resultara alterado. En ratones vivos, aumentar MeCP2 en progenitores embrionarios produjo neuronas adultas con señales excitatorias más fuertes, reflejando lo observado en modelos del síndrome de duplicación. Pero aumentar MeCP2 directamente en el cerebro adulto no cambió el comportamiento eléctrico de las neuronas. En conjunto, estos resultados muestran que las neuronas maduras son mucho más tolerantes a un incremento de MeCP2 que las progenitoras en desarrollo.
Cómo MeCP2 elige sus sitios en el ADN
Para entender por qué el tipo celular importa tanto, el equipo cartografió exactamente dónde se sitúan tanto las moléculas normales como las excedentes de MeCP2 en el ADN. En progenitoras y en neuronas, MeCP2 se localizó en tramos de ADN ricos en «islas CpG» cerca de los inicios de los genes, regiones que ayudan a controlar si los genes están activos o inactivos. La proteína normal y la extra eligieron esencialmente el mismo conjunto de blancos, especialmente genes implicados en construir y refinar los circuitos neuronales. La diferencia clave fue la intensidad de ocupación de esos sitios. En las neuronas, donde MeCP2 ya es abundantemente natural, estos sitios estaban casi saturados, dejando poco espacio para la proteína adicional, que se unió débilmente y se degradó con más rapidez. En las progenitoras, donde los niveles de MeCP2 son normalmente bajos, la proteína añadida pudo unirse con mucha más fuerza y de forma más amplia a estas regiones regulatorias.
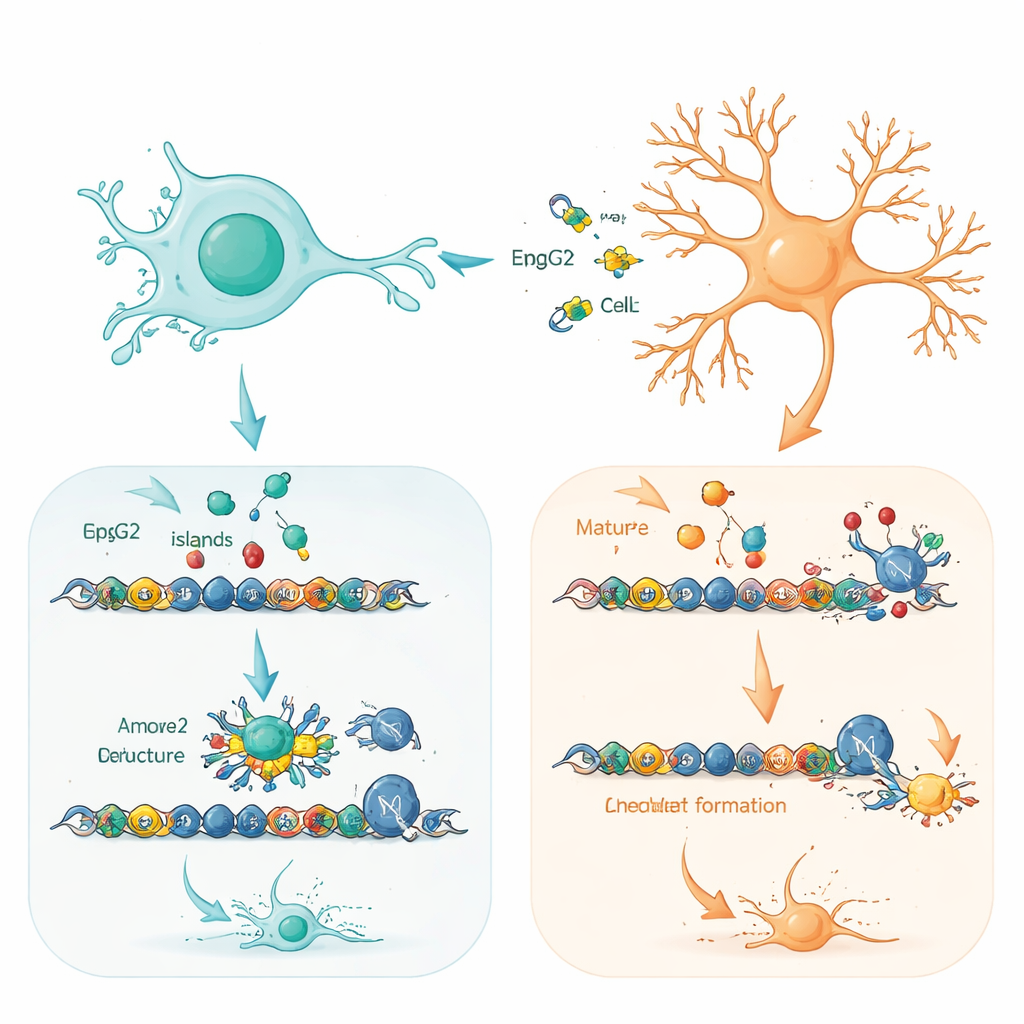
Preparando genes que deciden el destino en células cerebrales jóvenes
Un hallazgo particularmente llamativo fue que muchos de los genes más afectados en progenitoras se hallan en un estado «preparado»: portan marcas químicas tanto activadoras como represoras en sus regiones regulatorias y están listos para activarse a medida que avanza el desarrollo. Estos genes bivalentes con frecuencia controlan decisiones clave sobre qué tipos de neuronas se generan y cuándo. Los autores muestran que el exceso de MeCP2 ayuda a reclutar una poderosa máquina de empaquetamiento del ADN, el complejo SWI/SNF, a estos sitios preparados. Esta colaboración inclina la balanza hacia la activación, desbloqueando programas enteros de diferenciación neuronal antes de tiempo. Cambios sutiles en el panorama más amplio del empaquetamiento del ADN respaldaron esta imagen: regiones vinculadas al control del ciclo celular y a la maduración neuronal se volvieron algo más accesibles en progenitoras con exceso de MeCP2.
Qué implica esto para la terapia génica y los trastornos cerebrales
Para familias y clínicos preocupados de que las terapias génicas basadas en MeCP2 puedan excederse y dañar el cerebro, este trabajo ofrece una tranquilidad cautelosa. El estudio sugiere que aumentos moderados de MeCP2 en neuronas maduras—incluso de tres a cuatro veces—son sorprendentemente bien tolerados, porque los sitios de unión ya están ocupados y la proteína sobrante se elimina rápidamente. El verdadero peligro aparece cuando MeCP2 se eleva temprano en el desarrollo, en progenitoras cuyas genes que deciden el destino aún están en estado preparado y son altamente sensibles. En ese contexto, el exceso de MeCP2 puede activar prematuramente programas de desarrollo, alterar cómo y cuándo se producen las neuronas y, en última instancia, cambiar el cableado cerebral de formas que podrían contribuir a la epilepsia y otros síntomas observados en el síndrome de duplicación de MECP2. Más ampliamente, los hallazgos subrayan un principio probablemente compartido por muchos reguladores de la cromatina: la dosificación génica no es intrínsecamente tóxica, pero su impacto depende de manera crucial de cuándo en el desarrollo y en qué tipo celular ocurre el desequilibrio.
Cita: Luoni, M., Kubacki, M., Giannelli, S.G. et al. MeCP2 gene dosage-dependent neurodevelopmentally restricted defects arise by aberrant activation of cell fate-determining bivalent genes. Nat Commun 17, 3225 (2026). https://doi.org/10.1038/s41467-026-71432-w
Palabras clave: MeCP2, neurodesarrollo, dosificación génica, epigenética, terapia génica