Clear Sky Science · pl
Wady zależne od dawki genu MeCP2, ograniczone do rozwoju nerwowego, wynikają z nieprawidłowej aktywacji genów dwuwartościowych decydujących o losie komórkowym
Dlaczego ten gen ma znaczenie dla zdrowia mózgu
Gen MECP2 jest znany, ponieważ zbyt mała ilość jego białka powoduje zespół Retta, podczas gdy jego nadmiar prowadzi do zespołu duplikacji MECP2. Oba schorzenia przynoszą poważne problemy, takie jak upośledzenie intelektualne, napady drgawkowe i zaburzenia ruchowe. W tym badaniu postawiono pozornie proste pytanie o dalekosiężnych implikacjach dla przyszłych terapii genowych: czy dodatkowe MeCP2 jest zawsze szkodliwe, czy też to moment pojawienia się i typ komórki decydują, czy mózg zostanie uszkodzony czy oszczędzony?
Gdy nadmiar MeCP2 pojawia się zbyt wcześnie
Naukowcy porównali, co się dzieje, gdy MeCP2 jest nadprodukowane w niedojrzałych komórkach „progenitorowych nerwowych” versus w w pełni ukształtowanych neuronach, używając zarówno mysich, jak i ludzkich komórek. Progenitory nerwowe to dzielące się komórki rozwijającego się mózgu, które później dają początek neuronom. Gdy zespół zwiększył ilość MeCP2 w tych progenitorach, aktywność genów w komórkach zmieniła się dramatycznie: tysiące genów stało się bardziej lub mniej aktywnych, z wyraźnym przesunięciem w kierunku uruchamiania genów, które popychają komórki ku losowi neuronowemu. W hodowlach i w rozwijających się mózgach myszy progenitory z nadmiarem MeCP2 mniej się dzieliły i szybciej oraz wcześniej różnicowały się w neurony niż normalnie, zmieniając tempo rozwoju mózgu.
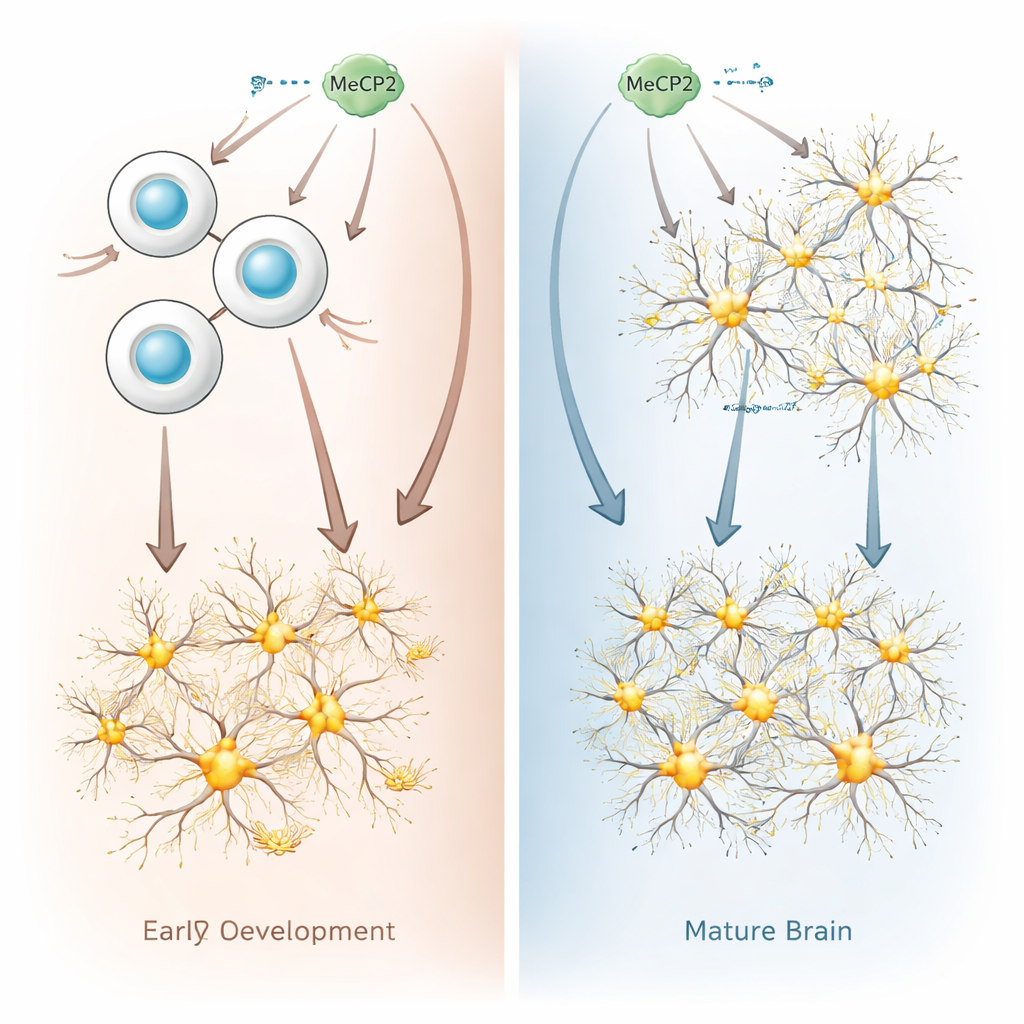
Dlaczego dojrzałe neurony znoszą nadmiar MeCP2
W ostrym kontraście, gdy tę samą ilość MeCP2 dodano do dojrzałych neuronów, efekty były zaskakująco łagodne. Tylko kilkaset genów zmieniło swoją aktywność, a większość tych zmian była niewielka. Naukowcy znaleźli też niewiele dowodów na to, że ogólne upakowanie DNA w tych neuronach zostało zmienione. U żywych myszy zwiększenie MeCP2 w embrionalnych progenitorach dało dorosłe neurony o silniejszych sygnałach pobudzających, co przypomina obserwacje w modelach zespołu duplikacji. Z kolei podniesienie poziomu MeCP2 bezpośrednio w mózgu dorosłych zwierząt nie zmieniło zachowania elektrycznego neuronów. Razem te wyniki pokazują, że dojrzałe neurony są znacznie bardziej tolerancyjne na zwiększenie MeCP2 niż rozwijające się progenitory.
Jak MeCP2 wybiera miejsca na DNA
Aby zrozumieć, dlaczego typ komórki ma tak duże znaczenie, zespół zmapował dokładnie, gdzie zarówno normalne, jak i dodatkowe cząsteczki MeCP2 wiążą się z DNA. Zarówno w progenitorach, jak i neuronach MeCP2 lokalizował się w obrębie odcinków DNA bogatych w „wyspy CpG” w pobliżu miejsc startu genów — regionów pomagających kontrolować, czy geny są włączone czy wyłączone. Normalne i dodatkowe białko wybierały zasadniczo ten sam zestaw celów, szczególnie geny zaangażowane w budowę i dopracowywanie obwodów nerwowych. Kluczowa różnica polegała na tym, jak mocno te miejsca były zajęte. W neuronach, gdzie MeCP2 jest już naturalnie obfite, te miejsca były niemal nasycone, pozostawiając niewiele przestrzeni dla dodatkowego białka, które wiązało się słabiej i było szybciej degradowane. W progenitorach, gdzie poziomy MeCP2 są normalnie niskie, dodane białko mogło wiązać się znacznie silniej i szerzej w tych regulatorowych regionach.
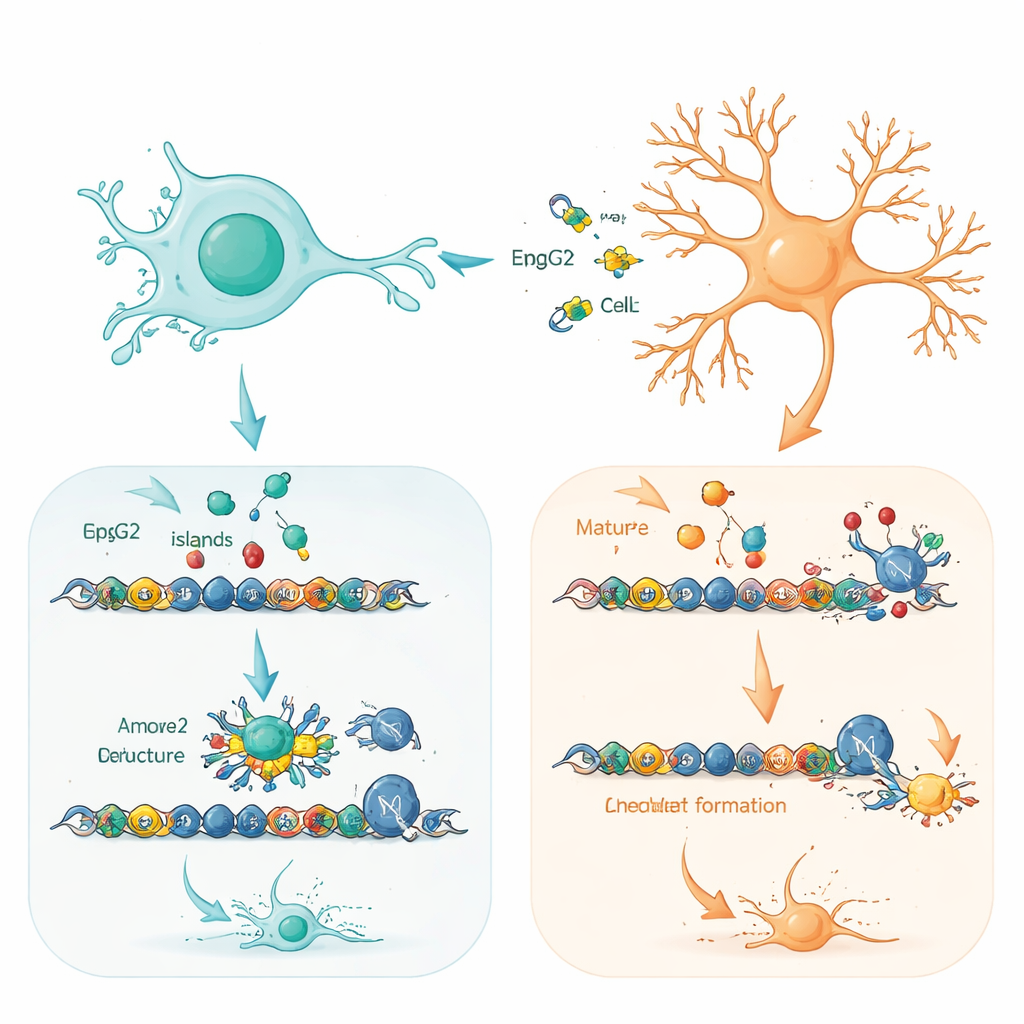
Priming genów decydujących o losie w młodych komórkach mózgu
Szczególnie uderzającym odkryciem było to, że wiele genów najsilniej dotkniętych w progenitorach znajduje się w stanie „gotowości”: niosą one zarówno aktywujące, jak i wyciszające modyfikacje chemiczne w swoich regionach regulatorowych i są gotowe do włączenia w miarę postępu rozwoju. Te geny dwuwartościowe często kontrolują kluczowe decyzje dotyczące tego, jakie typy neuronów powstają i kiedy. Autorzy pokazują, że nadmiar MeCP2 pomaga rekrutować potężną maszynę do
Cytowanie: Luoni, M., Kubacki, M., Giannelli, S.G. et al. MeCP2 gene dosage-dependent neurodevelopmentally restricted defects arise by aberrant activation of cell fate-determining bivalent genes. Nat Commun 17, 3225 (2026). https://doi.org/10.1038/s41467-026-71432-w
Słowa kluczowe: MeCP2, rozwój nerwowy, dawka genu, epigenetyka, terapia genowa