Clear Sky Science · nl
Dosering van het MeCP2-gen veroorzaakt neurodevelopmentaal beperkte defecten door abnormale activering van bivalente genen die celdeterminatie bepalen
Waarom dit gen belangrijk is voor de gezondheid van de hersenen
Het MECP2-gen is bekend omdat een tekort aan het bijbehorende eiwit het Rett-syndroom veroorzaakt, terwijl een teveel leidt tot MECP2-duplicatiesyndroom. Beide aandoeningen geven ernstige problemen zoals verstandelijke beperking, epileptische aanvallen en bewegingsstoornissen. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties voor toekomstige gentherapieën: is extra MeCP2 altijd schadelijk, of bepalen het tijdstip en het celtype waarin het voorkomt of de hersenen worden geschaad of gespaard?
Wanneer extra MeCP2 te vroeg verschijnt
De onderzoekers vergeleken wat er gebeurt als MeCP2 in overmaat wordt geproduceerd in onrijpe “neuronale voorlopercellen” versus in volledig ontwikkelde neuronen, met zowel muis- als menselijke cellen. Neuronale voorlopercellen zijn de delende cellen in de zich ontwikkelende hersenen die later neuronen zullen vormen. Toen het team MeCP2 in deze voorlopercellen verhoogde, veranderde de genactiviteit ingrijpend: duizenden genen werden sterker of zwakker geactiveerd, met een duidelijke neiging om genen aan te zetten die cellen naar een neuronaal lot duwen. In kweek en in zich ontwikkelende muizenhersenen deelden voorlopercellen met teveel MeCP2 minder en differentieerden ze eerder en sneller naar neuronen dan normaal, waardoor het tempo van de hersenontwikkeling verschoof.
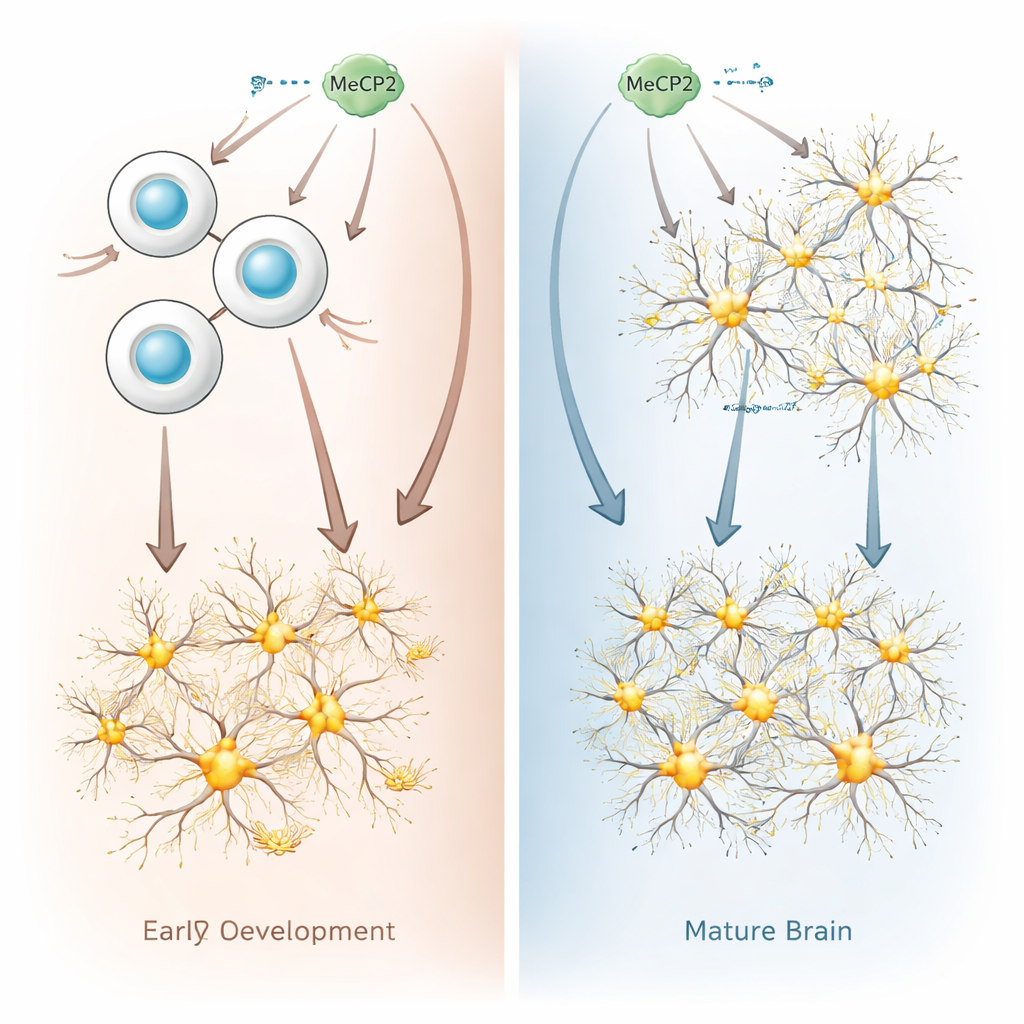
Waarom rijpe neuronen extra MeCP2 van zich af lijken te schudden
In scherp contrast daarmee waren de effecten verrassend mild wanneer dezelfde hoeveelheid MeCP2 aan rijpe neuronen werd toegevoegd. Slechts enkele honderden genen veranderden in activiteit, en de meeste veranderingen waren klein. De onderzoekers vonden ook weinig bewijs dat de algehele verpakking van DNA in deze neuronen werd veranderd. In levenende muizen zorgde het verhogen van MeCP2 in embryonale voorlopercellen voor volwassen neuronen met sterkere exciterende elektrische signalen, overeenkomstig met wat wordt gezien in modellen van duplicatiesyndroom. Het direct verhogen van MeCP2 in de volwassen hersenen veranderde echter niet het elektrische gedrag van neuronen. Samen laten deze resultaten zien dat rijpe neuronen veel toleranter zijn voor verhoogd MeCP2 dan zich ontwikkelende voorlopercellen.
Hoe MeCP2 zijn plekken op DNA kiest
Om te begrijpen waarom het celtype zo belangrijk is, bracht het team precies in kaart waar zowel normaal als extra MeCP2 zich op het DNA bevindt. In zowel voorlopercellen als neuronen zocht MeCP2 naar stukken DNA rijk aan “CpG-eilanden” nabij genstarters—regio’s die helpen bepalen of genen aan of uit staan. Het normale en het extra eiwit kozen in wezen dezelfde set doelen, vooral genen die betrokken zijn bij het bouwen en verfijnen van neurale netwerken. Het belangrijke verschil was hoeveel van die plaatsen bezet waren. In neuronen, waar MeCP2 van nature al overvloedig aanwezig is, waren deze plekken bijna verzadigd, waardoor er weinig ruimte overbleef voor het extra eiwit, dat zwakker bond en sneller werd afgebroken. In voorlopercellen, waar MeCP2-niveaus normaal laag zijn, kon het toegevoegde eiwit veel sterker en ruimer binden over deze regulatorische regio’s.
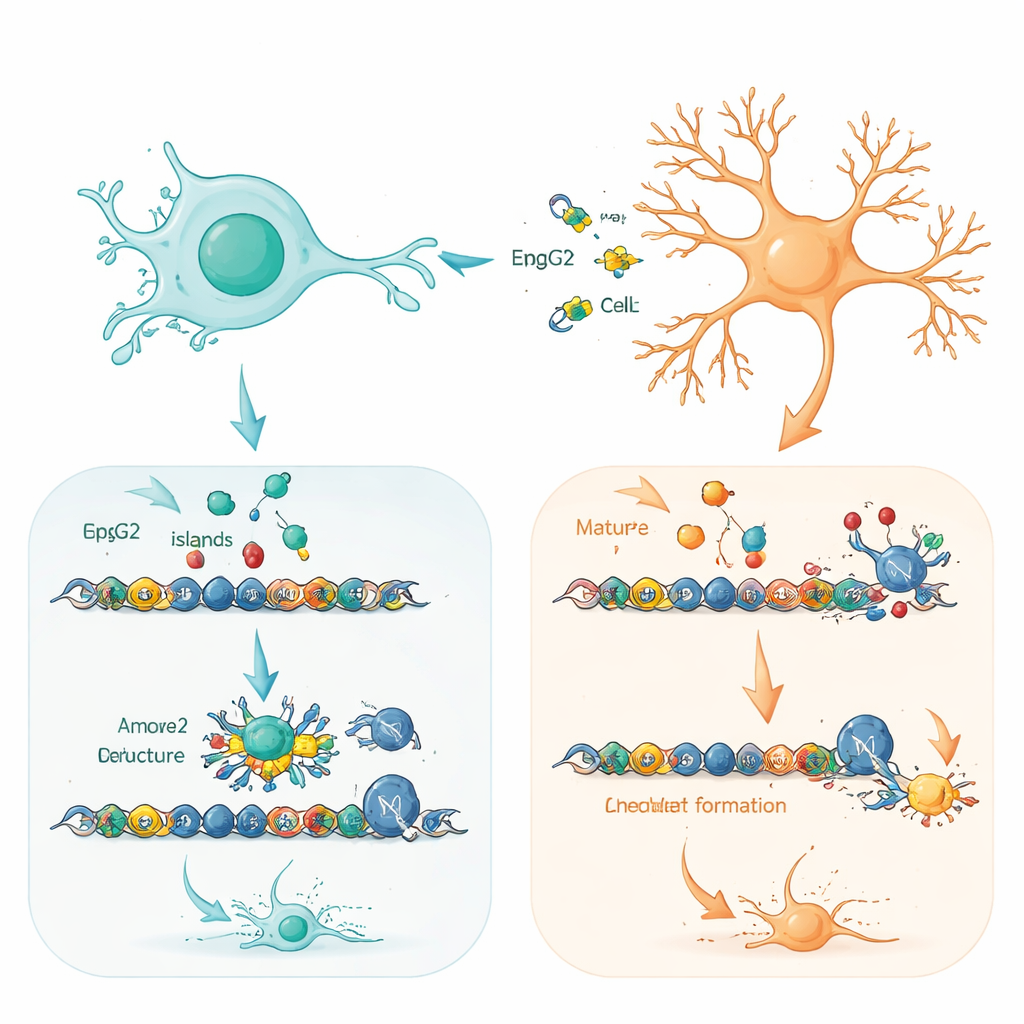
Het primen van fate-bepalende genen in jonge hersencellen
Een opvallende bevinding was dat veel van de genen die het meest werden beïnvloed in voorlopercellen in een “gepoosde” toestand verkeren: ze dragen zowel activerende als stillegende chemische merken op hun regulatorische regio’s en staan klaar om aangezet te worden naarmate de ontwikkeling vordert. Deze bivalente genen regelen vaak cruciale beslissingen over welke typen neuronen worden gemaakt en wanneer. De auteurs tonen aan dat teveel MeCP2 helpt bij het rekruteren van een krachtig DNA-verpakkingscomplex, het SWI/SNF-complex, naar deze gepoosde sites. Deze samenwerking kantelt de balans richting activatie, waardoor volledige programma’s van neuronale differentiatie eerder dan bedoeld worden ontgrendeld. Subtiele verschuivingen in het bredere DNA-verpakkingslandschap ondersteunen dit beeld: regio’s die verband houden met celdelingscontrole en neuronale rijping werden iets opener in voorlopercellen met teveel MeCP2.
Wat dit betekent voor gentherapie en hersenaandoeningen
Voor gezinnen en clinici die vrezen dat MeCP2-gebaseerde gentherapieën te veel kunnen doen en de hersenen kunnen schaden, biedt dit werk voorzichtige geruststelling. De studie suggereert dat matige verhogingen van MeCP2 in rijpe neuronen—zelfs drie- tot viermaal—verrassend goed worden verdragen, omdat bindingsplaatsen al bezet zijn en overtollig eiwit snel wordt verwijderd. Het echte gevaar lijkt te liggen wanneer MeCP2 vroeg in de ontwikkeling wordt verhoogd, in voorlopercellen wiens fate-bepalende genen nog gepoosd en zeer gevoelig zijn. In die situatie kan extra MeCP2 ontwikkelingsprogramma’s voortijdig activeren, veranderen hoe en wanneer neuronen worden geproduceerd en uiteindelijk de bedrading van de hersenen op manieren veranderen die kunnen bijdragen aan epilepsie en andere symptomen die worden gezien bij MECP2-duplicatiesyndroom. Breder benadrukken de bevindingen een principe dat waarschijnlijk geldt voor veel chromatineregulatoren: geendosering is niet per definitie toxisch, maar het effect hangt cruciaal af van wanneer in de ontwikkeling, en in welk celtype, de onbalans optreedt.
Bronvermelding: Luoni, M., Kubacki, M., Giannelli, S.G. et al. MeCP2 gene dosage-dependent neurodevelopmentally restricted defects arise by aberrant activation of cell fate-determining bivalent genes. Nat Commun 17, 3225 (2026). https://doi.org/10.1038/s41467-026-71432-w
Trefwoorden: MeCP2, neuroontwikkeling, geendosering, epigenetica, gentherapie