Clear Sky Science · it
Difetti neuroevolutivi limitati nel tempo dipendenti dal dosaggio del gene MeCP2 derivano dall'attivazione aberrante di geni bivalenti determinanti il destino cellulare
Perché questo gene è importante per la salute del cervello
Il gene MECP2 è noto perché la sua carenza di proteina provoca la sindrome di Rett, mentre il suo eccesso porta alla sindrome da duplicazione di MECP2. Entrambe le condizioni comportano gravi problemi come disabilità intellettiva, crisi epilettiche e disturbi del movimento. Questo studio pone una domanda apparentemente semplice ma di grande importanza per le future terapie geniche: un eccesso di MeCP2 è sempre pericoloso, o è il momento e il tipo cellulare in cui compare a determinare se il cervello viene danneggiato o risparmiato?
Quando l’eccesso di MeCP2 compare troppo presto
I ricercatori hanno confrontato cosa succede quando MeCP2 è sovraespresso in cellule immature «progenitrici neurali» rispetto a neuroni completamente formati, usando sia cellule murine sia umane. Le progenitrici neurali sono le cellule in divisione nel cervello in sviluppo che poi daranno origine ai neuroni. Quando il gruppo ha aumentato MeCP2 in queste progenitrici, l’attività genetica delle cellule è cambiata drasticamente: migliaia di geni sono diventati più o meno attivi, con una netta tendenza all’attivazione di geni che spingono le cellule a diventare neuroni. in coltura e nei cervelli in sviluppo di topi, le progenitrici con MeCP2 in eccesso hanno ridotto la proliferazione e si sono convertite in neuroni prima e più rapidamente del normale, accelerando il ritmo dello sviluppo cerebrale.
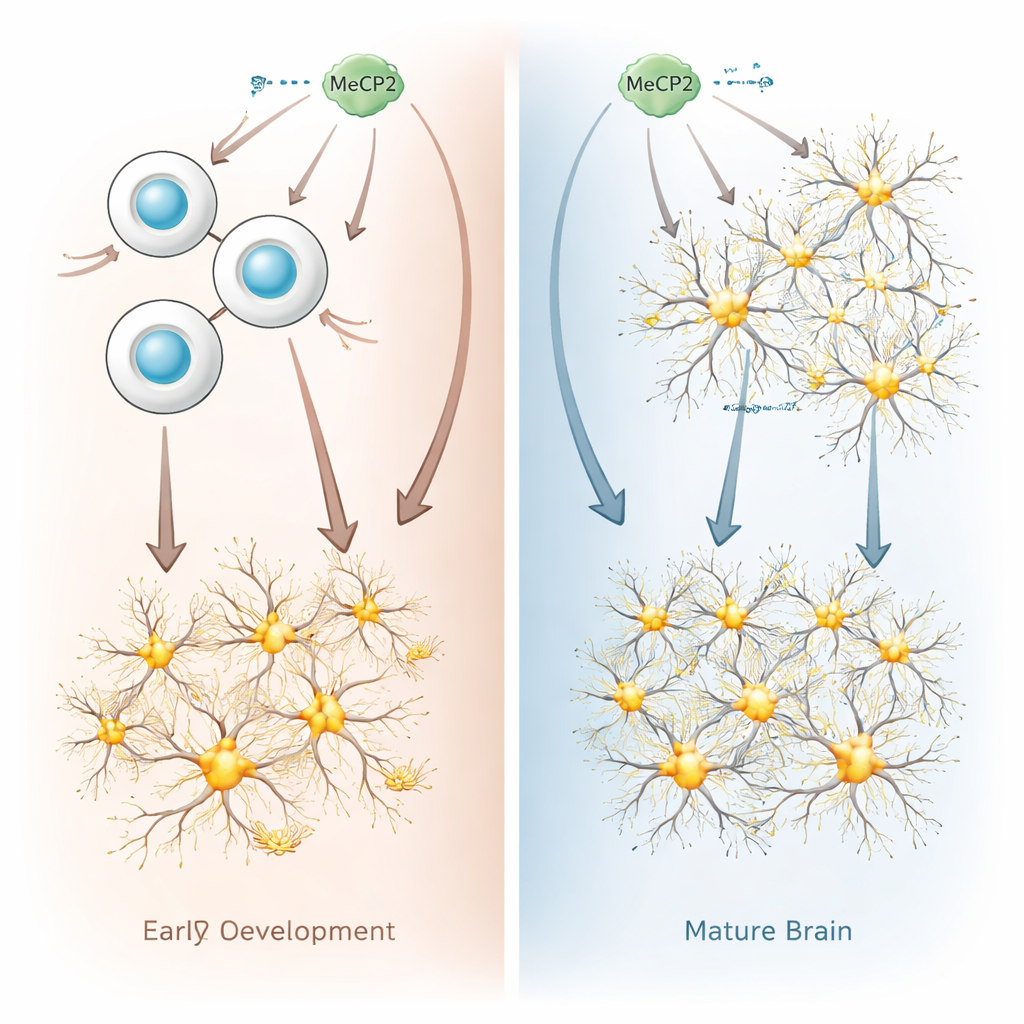
Perché i neuroni maturi ignorano in gran parte l’eccesso di MeCP2
Al contrario netto, quando la stessa quantità di MeCP2 è stata aggiunta a neuroni maturi, gli effetti sono stati sorprendentemente lievi. Solo alcune centinaia di geni hanno cambiato la loro attività, e la maggior parte di questi cambiamenti è risultata modesta. I ricercatori hanno inoltre trovato poche evidenze che il confezionamento complessivo del DNA in questi neuroni fosse alterato. Nei topi viventi, aumentare MeCP2 nelle progenitrici embrionali ha prodotto neuroni adulti con segnali elettrici eccitatori più forti, rispecchiando quanto osservato nei modelli della sindrome da duplicazione. Ma aumentare MeCP2 direttamente nel cervello adulto non ha cambiato il comportamento elettrico dei neuroni. Nel loro complesso, questi risultati mostrano che i neuroni maturi tollerano molto meglio l’aumento di MeCP2 rispetto alle progenitrici in sviluppo.
Come MeCP2 sceglie i suoi siti sul DNA
Per capire perché il tipo cellulare è così importante, il gruppo ha mappato esattamente dove sia MeCP2 normale sia quello in eccesso si legano sul DNA. Sia nelle progenitrici sia nei neuroni, MeCP2 ha preso di mira tratti di DNA ricchi di «isole CpG» vicino agli inizi dei geni—regioni che aiutano a controllare se i geni sono attivi o spenti. La proteina normale e quella in eccesso hanno scelto essenzialmente lo stesso insieme di bersagli, in particolare geni coinvolti nella costruzione e nel perfezionamento dei circuiti neuronali. La differenza chiave era quanto intensamente quei siti fossero occupati. Nei neuroni, dove MeCP2 è già naturalmente abbondante, questi siti erano quasi saturi, lasciando poco spazio per la proteina in eccesso, che si legava debolmente ed era degradata più rapidamente. Nelle progenitrici, dove i livelli di MeCP2 sono normalmente bassi, la proteina aggiunta poteva legarsi molto più fortemente e diffusamente a queste regioni regolatorie.
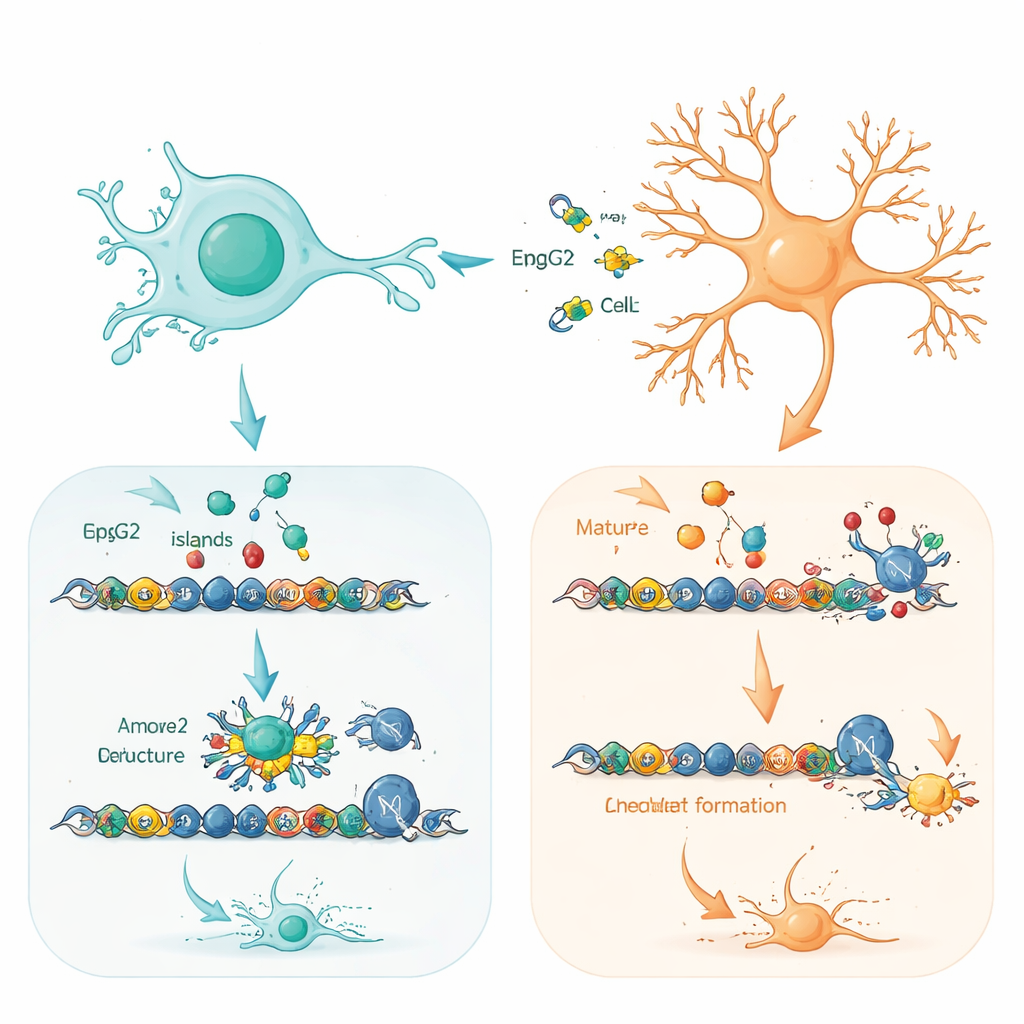
Priming dei geni determinanti il destino nelle cellule cerebrali giovani
Un risultato particolarmente notevole è che molti dei geni più colpiti nelle progenitrici si trovano in uno stato «pronto»: portano sia marchi chimici attivanti sia silenzianti sulle loro regioni regolatorie e sono pronti a essere accesi con l’avanzare dello sviluppo. Questi geni bivalenti spesso controllano decisioni chiave su quali tipi di neuroni vengano prodotti e quando. Gli autori mostrano che l’eccesso di MeCP2 favorisce il reclutamento di una potente macchina di impacchettamento del DNA, il complesso SWI/SNF, in questi siti pronti. Questa collaborazione tende l’equilibrio verso l’attivazione, sbloccando interi programmi di differenziazione neuronale prima del dovuto. Mutamenti sottili nel più ampio paesaggio del confezionamento del DNA confermano questo quadro: regioni legate al controllo del ciclo cellulare e alla maturazione neuronale diventano leggermente più aperte nelle progenitrici con MeCP2 in eccesso.
Cosa significa per la terapia genica e i disturbi cerebrali
Per le famiglie e i clinici preoccupati che le terapie geniche basate su MeCP2 possano eccedere e danneggiare il cervello, questo lavoro offre una rassicurazione cauta. Lo studio suggerisce che aumenti moderati di MeCP2 nei neuroni maturi—anche di tre‑quattro volte—sono sorprendentemente ben tollerati, perché i siti di legame sono già occupati e la proteina in eccesso viene rapidamente eliminata. Il vero pericolo sembra emergere quando MeCP2 è elevato precocemente nello sviluppo, nelle progenitrici le cui regioni regolatorie dei geni determinanti il destino sono ancora pronte e altamente sensibili. In quel contesto, l’eccesso di MeCP2 può attivare prematuramente programmi di sviluppo, alterare come e quando i neuroni vengono prodotti e, in ultima analisi, modificare i cablaggi cerebrali in modi che possono contribuire all’epilessia e ad altri sintomi osservati nella sindrome da duplicazione di MECP2. Più in generale, i risultati evidenziano un principio probabilmente condiviso da molti regolatori della cromatina: il dosaggio genico non è intrinsecamente tossico, ma il suo impatto dipende in modo cruciale da quando nello sviluppo e in quale tipo cellulare si verifica lo squilibrio.
Citazione: Luoni, M., Kubacki, M., Giannelli, S.G. et al. MeCP2 gene dosage-dependent neurodevelopmentally restricted defects arise by aberrant activation of cell fate-determining bivalent genes. Nat Commun 17, 3225 (2026). https://doi.org/10.1038/s41467-026-71432-w
Parole chiave: MeCP2, neurosviluppo, dosaggio genico, epigenetica, terapia genica