Clear Sky Science · pt
Defeitos restritos ao desenvolvimento neurológico dependentes da dosagem do gene MeCP2 surgem por ativação aberrante de genes bivalentes que determinam destino celular
Por que este gene é importante para a saúde do cérebro
O gene MECP2 é conhecido porque a falta de sua proteína causa a síndrome de Rett, enquanto o excesso leva à síndrome de duplicação de MECP2. Ambas as condições provocam problemas sérios, como deficiência intelectual, convulsões e transtornos motores. Este estudo aborda uma pergunta aparentemente simples, com grandes implicações para futuras terapias gênicas: o excesso de MeCP2 é sempre perigoso, ou o momento e o tipo de célula em que ele aparece determinam se o cérebro será prejudicado ou poupado?
Quando o excesso de MeCP2 aparece cedo demais
Os pesquisadores compararam o que acontece quando o MeCP2 é superexpresso em células imaturas “progenitoras neurais” versus em neurônios totalmente formados, usando células de camundongo e humanas. Progenitores neurais são as células que se dividem no cérebro em desenvolvimento e que mais tarde darão origem aos neurônios. Quando a equipe aumentou o MeCP2 nesses progenitores, a atividade gênica das células mudou dramaticamente: milhares de genes ficaram mais ou menos ativos, com forte tendência a ativar genes que impulsionam as células a se tornarem neurônios. Em cultura e em cérebros de camundongo em desenvolvimento, progenitores com excesso de MeCP2 diminuíram sua divisão e se converteram em neurônios mais cedo e mais rapidamente que o normal, alterando o ritmo do desenvolvimento cerebral.
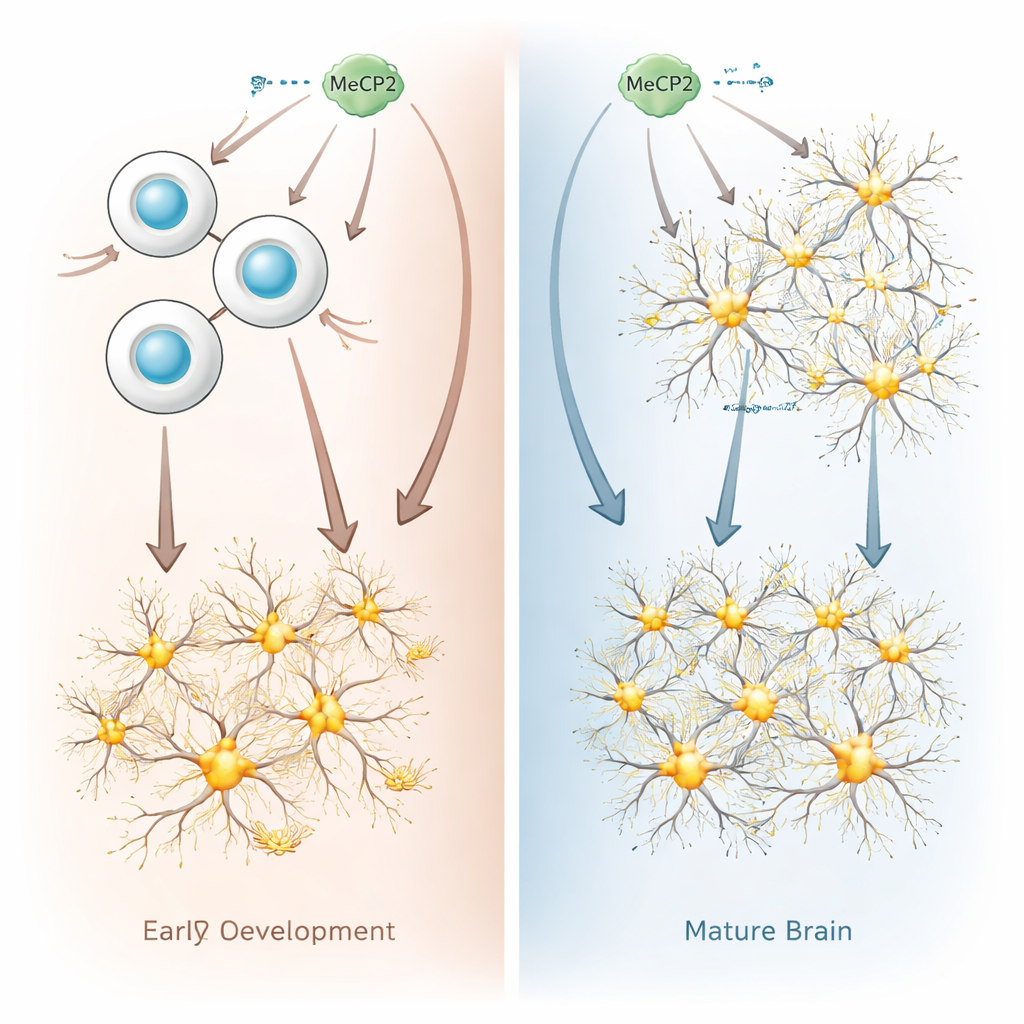
Por que neurônios maduros toleram melhor o excesso de MeCP2
Em nítido contraste, quando a mesma quantidade de MeCP2 foi adicionada a neurônios maduros, os efeitos foram surpreendentemente suaves. Apenas algumas centenas de genes alteraram sua atividade, e a maioria dessas mudanças foi pequena. Os pesquisadores também encontraram pouca evidência de alteração na organização global do DNA nesses neurônios. Em camundongos vivos, aumentar MeCP2 em progenitores embrionários gerou neurônios adultos com sinais excitatórios elétricos mais fortes, ecoando o observado em modelos da síndrome de duplicação. Mas aumentar MeCP2 diretamente no cérebro adulto não alterou o comportamento elétrico dos neurônios. Em conjunto, esses resultados mostram que neurônios maduros toleram muito melhor níveis aumentados de MeCP2 do que progenitores em desenvolvimento.
Como o MeCP2 escolhe seus locais no DNA
Para entender por que o tipo celular importa tanto, a equipe mapeou exatamente onde tanto o MeCP2 normal quanto o excedente se posicionam no DNA. Em progenitores e neurônios, o MeCP2 se concentrou em trechos de DNA ricos em “ilhas CpG” perto de inícios de genes — regiões que ajudam a controlar se os genes estão ligados ou desligados. A proteína normal e a em excesso escolheram essencialmente o mesmo conjunto de alvos, especialmente genes envolvidos na construção e refinamento de circuitos neurais. A diferença chave foi a intensidade de ocupação desses sítios. Em neurônios, onde o MeCP2 já é naturalmente abundante, esses locais estavam quase saturados, deixando pouco espaço para a proteína extra, que se ligava fracamente e era degradada mais rapidamente. Em progenitores, onde os níveis de MeCP2 são normalmente baixos, a proteína adicionada podia se ligar muito mais forte e amplamente nessas regiões regulatórias.
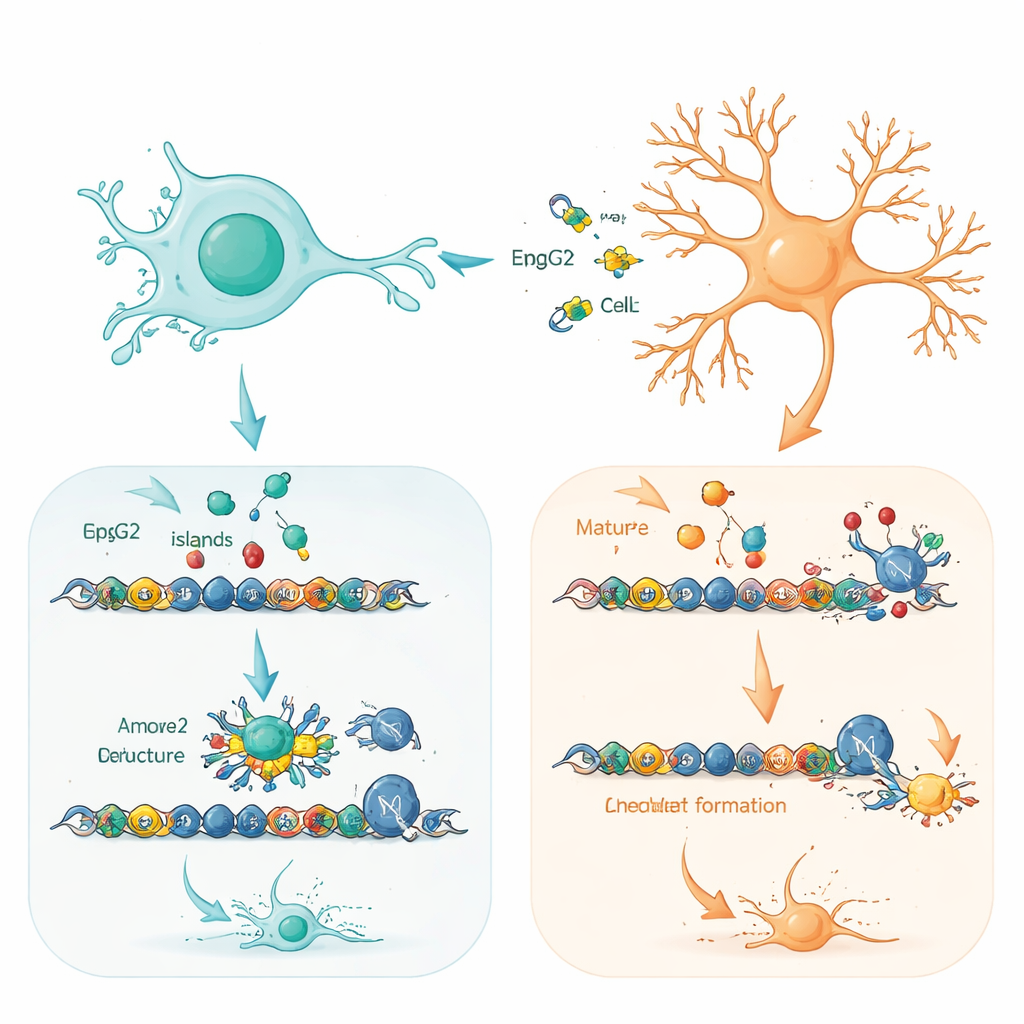
Priming de genes determinantes de destino em células cerebrais jovens
Uma descoberta particularmente notável foi que muitos dos genes mais afetados em progenitores estão em um estado “pronto”: carregam marcas químicas ativadoras e silenciadoras em suas regiões regulatórias e estão prontos para serem ativados conforme o desenvolvimento progride. Esses genes bivalentes frequentemente controlam decisões-chave sobre quais tipos de neurônios são feitos e quando. Os autores mostram que o excesso de MeCP2 ajuda a recrutar uma poderosa máquina de empacotamento do DNA, o complexo SWI/SNF, para esses sítios prontos. Essa parceria inclina a balança para a ativação, desbloqueando programas inteiros de diferenciação neuronal mais cedo do que deveriam. Mudanças sutis no panorama mais amplo do empacotamento do DNA corroboraram essa imagem: regiões ligadas ao controle do ciclo celular e à maturação neuronal tornaram-se levemente mais abertas em progenitores com excesso de MeCP2.
O que isso significa para terapia gênica e distúrbios cerebrais
Para famílias e clínicos preocupados de que terapias gênicas baseadas em MeCP2 possam exceder a dose e prejudicar o cérebro, este trabalho oferece uma cautelosa tranquilidade. O estudo sugere que aumentos moderados de MeCP2 em neurônios maduros — mesmo de três a quatro vezes — são surpreendentemente bem tolerados, porque os sítios de ligação já estão ocupados e o excesso de proteína é rapidamente eliminado. O perigo real parece ocorrer quando o MeCP2 é elevado cedo no desenvolvimento, em células progenitoras cujos genes determinantes de destino ainda estão prontos e altamente sensíveis. Nesse contexto, o excesso de MeCP2 pode ativar prematuramente programas de desenvolvimento, alterar como e quando os neurônios são produzidos e, em última instância, modificar a fiação cerebral de maneiras que podem contribuir para epilepsia e outros sintomas observados na síndrome de duplicação de MECP2. Mais amplamente, os achados destacam um princípio provavelmente compartilhado por muitos reguladores da cromatina: a dosagem gênica não é inerentemente tóxica, mas seu impacto depende crucialmente de quando, durante o desenvolvimento, e em qual tipo celular, o desequilíbrio ocorre.
Citação: Luoni, M., Kubacki, M., Giannelli, S.G. et al. MeCP2 gene dosage-dependent neurodevelopmentally restricted defects arise by aberrant activation of cell fate-determining bivalent genes. Nat Commun 17, 3225 (2026). https://doi.org/10.1038/s41467-026-71432-w
Palavras-chave: MeCP2, neurodesenvolvimento, dosagem gênica, epigenética, terapia gênica