Clear Sky Science · zh
Dbf4依赖性激酶微调Ino80在染色体复制起点的功能
这对我们的DNA为何重要
每次细胞分裂时,都必须完整且尽量无差错地复制其全部DNA。复制过程中的失误会破坏基因组稳定性,并与癌症密切相关。本研究揭示了一种关键细胞周期酶不仅能开启DNA复制机器,还能整理局部DNA的包装,以便复制平稳启动并在压力下重启。 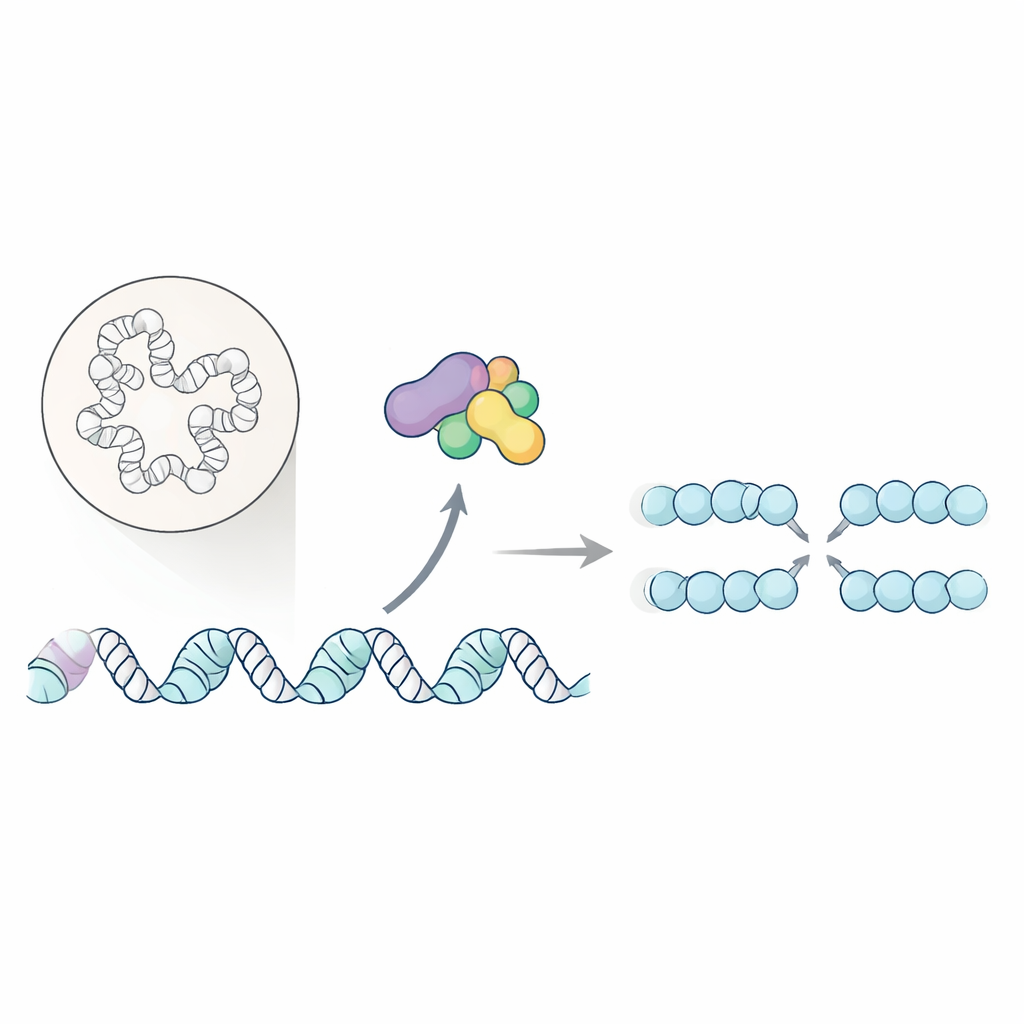
启动DNA复制的交通信号灯
细胞依赖染色体上专门的“起点”来开始DNA复制。一对众所周知的酶——Dbf4依赖性激酶(DDK)——通过修饰核心解旋酶来帮助启动该过程。迄今为止,DDK的直接靶点知之甚少,其作用仍有许多未解之处。作者着手在全局范围内描绘哪些核内蛋白依赖DDK进行磷酸化——一种常作为蛋白功能开/关信号的化学修饰。
扫描细胞核以寻找DDK的隐蔽伙伴
为此,研究者以出芽酵母为模型,结合两种互补策略在活细胞中降低DDK活性:其催化亚基的温敏突变体和一种诱导复制应激的药物,后者间接阻断DDK作用。随后他们分离细胞核并用质谱对成千上万的磷酸化肽段进行目录化,比较DDK活跃与抑制状态的样本。通过聚焦在两种抑制设置中都降低的位点,他们建立了约400个DDK依赖靶点的高置信清单。其中许多蛋白与染色质结合——染色质是组织基因组的DNA-蛋白质材料——暗示DDK在塑造复制发生的物理环境方面具有更广泛的作用。
由小蛋白尾巴调谐的重塑机器
强烈的命中目标之一是Arp8,它属于名为INO80的大型染色质重塑复合体。已知INO80能重新定位核小体(DNA绕组蛋白形成的珠状结构),并在复制起点周围将它们排列成有规律的阵列。团队用生化方法证明DDK直接磷酸化Arp8非结构化尾部的两个特定丝氨酸残基。当他们将这些丝氨酸替换为不能被磷酸化的丙氨酸时,INO80的总体组成保持不变,但其内部架构发生改变:交联实验显示复合体关键模块之间的接触减弱。从功能上看,突变的INO80消耗ATP的速率明显降低,移动核小体的能力大幅减弱,尽管它仍能结合DNA和核小体,有时甚至比正常情况下结合更紧密。
从局部间距到整体复制成功
为了将这些分子缺陷与染色体行为联系起来,作者在体外用含有数百个复制起点的酵母DNA片段库重建了染色质。在存在正常INO80和起始识别复合体(ORC)的条件下,他们观察到每个起点两侧形成整齐的核小体相位阵列,并在中间留有核小体空缺的间隙。相比之下,Arp8突变体产生的阵列不那么精确,核小体间的连接距离发生变化。使用完全重构的复制体系,他们发现由突变INO80组装的染色质在起点的起始效率较弱,尽管已经开始的单个复制片段延伸看起来相似。在携带相同Arp8突变的活体酵母中,细胞周期阻滞后进入DNA合成被延迟,自发重组事件增多,且细胞对羟基脲(一种耗尽DNA合成原料并阻滞复制的药物)特别敏感。然而整体基因表达,包括细胞周期和复制相关基因,大体保持不变,这表明主要问题在于起点处的染色质构架,而不是复制因子的数量变化。 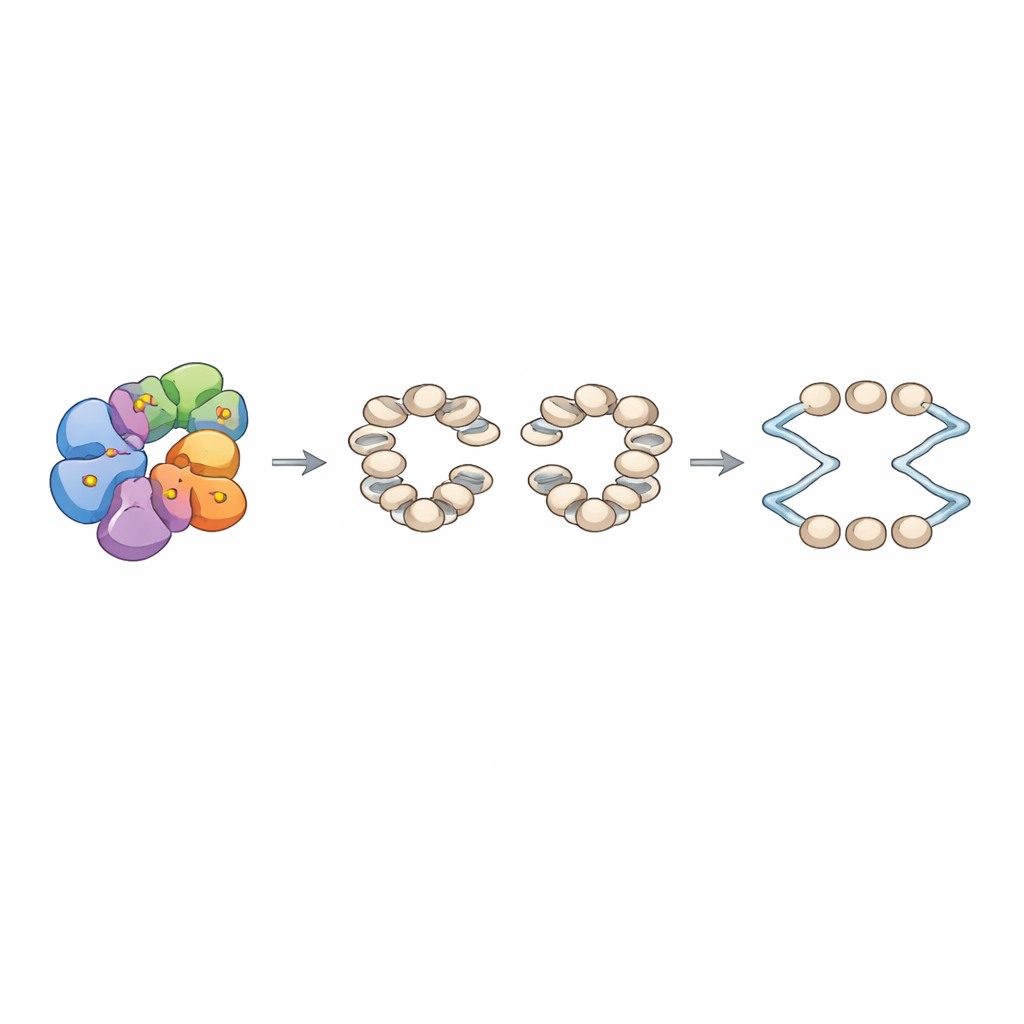
细致的DNA包装如何保护我们的基因组
综上所述,这项工作表明DDK不仅仅是开启核心复制机械的开关。通过磷酸化Arp8,DDK微调INO80重塑酶,使复制起点周围的核小体间距恰到好处。这种有序的包装似乎是高效起始和在压力下安全重启停滞复制叉的门控机制。从实际角度看,研究显示DNA的缠绕和排列方式不仅是复制必须克服的障碍——它本身是被调控的主动特征,有助于决定复制何时何地开始,并对维持基因组稳定性具有直接影响。
引用: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
关键词: DNA复制, 染色质重塑, 细胞周期激酶, 基因组稳定性, 酵母模型