Clear Sky Science · fr
La kinase dépendante de Dbf4 ajuste finement la fonction d’Ino80 aux origines de réplication chromosomique
Pourquoi cela compte pour notre ADN
Chaque fois qu’une cellule se divise, elle doit copier l’intégralité de son ADN sans erreurs majeures. Les défaillances de cette étape de copie peuvent déstabiliser le génome et sont étroitement liées au cancer. Cette étude montre comment une enzyme clé du cycle cellulaire non seulement active la machinerie de réplication, mais organise aussi l’emballage local de l’ADN afin que la réplication puisse démarrer correctement et redémarrer en cas de stress. 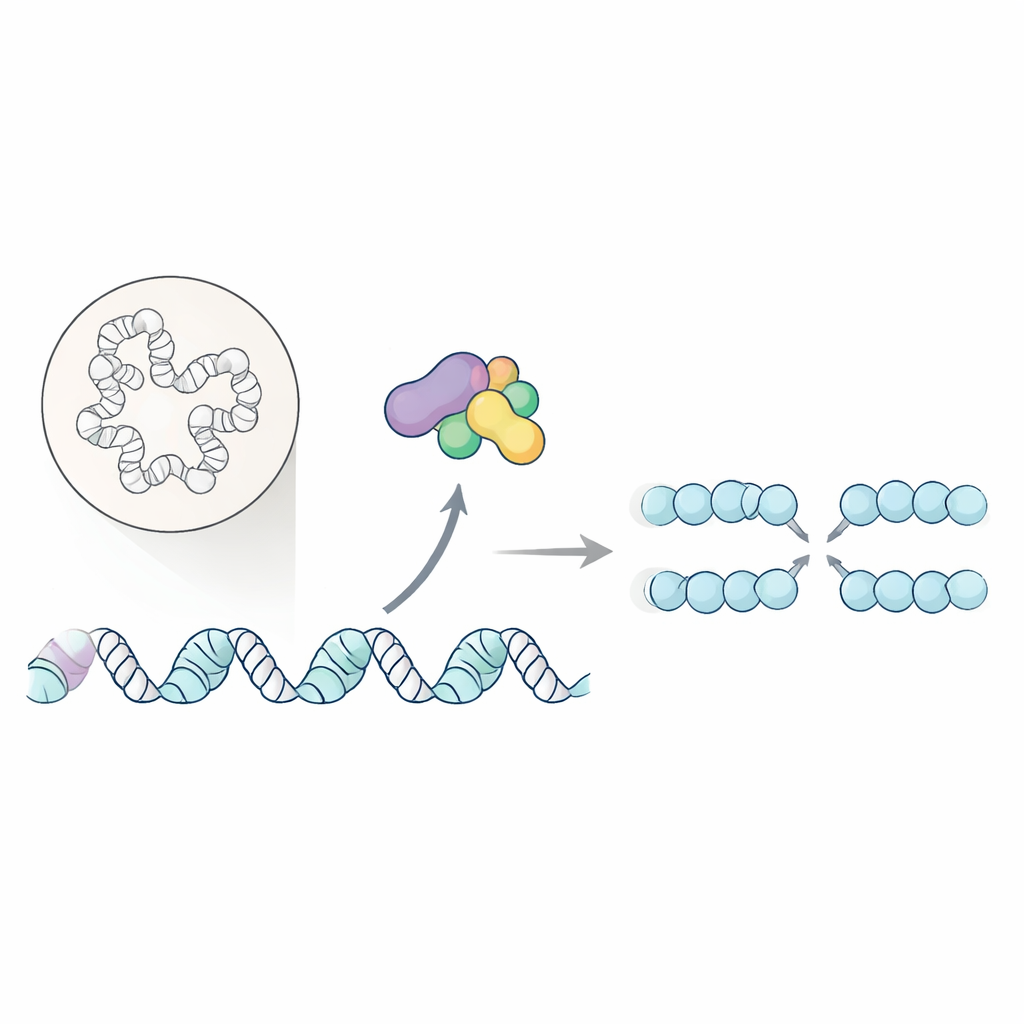
Un feu tricolore pour lancer la copie de l’ADN
Les cellules s’appuient sur des « origines » spécialisées le long de leurs chromosomes où commence la réplication de l’ADN. Une paire d’enzymes bien connue, la kinase dépendante de Dbf4 (DDK), aide à déclencher ce processus en modifiant la machine centrale d’ouverture de l’ADN, l’hélicase. Jusqu’ici, seules quelques cibles directes de la DDK étaient connues, ce qui laissait une grande part d’ombre sur son rôle. Les auteurs ont entrepris de cartographier, à grande échelle, quelles protéines nucléaires dépendent de la DDK pour leur phosphorylation — une marque chimique qui sert souvent d’interrupteur marche/arrêt pour la fonction des protéines.
À la recherche des partenaires cachés de la DDK dans le noyau
Pour cela, les chercheurs ont utilisé la levure bourgeonnante comme modèle et combiné deux stratégies complémentaires pour réduire l’activité de la DDK in vivo : un mutant thermosensible de sa sous-unité catalytique et un stress de réplication induit par médicament qui bloque indirectement l’action de la DDK. Ils ont ensuite isolé les noyaux et utilisé la spectrométrie de masse pour recenser des milliers de fragments protéiques phosphorylés, comparant des échantillons avec DDK active ou inhibée. En se concentrant sur les sites diminuant dans les deux protocoles d’inhibition, ils ont établi une liste à haute confiance d’environ 400 cibles dépendantes de la DDK. Beaucoup de ces protéines sont liées à la chromatine, le matériau ADN–protéine qui organise le génome, ce qui suggère que la DDK joue un rôle plus large dans la configuration physique où la réplication a lieu.
Une machine de remodelage réglée par une petite queue protéique
Parmi les cibles les plus fortes figure Arp8, une composante d’une grande machinerie de remodelage de la chromatine appelée le complexe INO80. On sait qu’INO80 repositionne les nucléosomes — structures en perles formées par l’ADN enroulé autour d’histones — et qu’il les arrange en réseaux réguliers autour des origines de réplication. L’équipe a montré biochimiquement que la DDK phosphoryle directement deux sérines spécifiques dans une queue non structurée d’Arp8. Lorsqu’ils ont remplacé ces sérines par des alanines, qui ne peuvent pas être phosphorylées, la composition globale d’INO80 est restée intacte, mais son architecture interne a changé : des expériences de réticulation ont révélé des contacts affaiblis entre des modules clés du complexe. Sur le plan fonctionnel, l’INO80 mutant consommait beaucoup plus lentement l’ATP et était nettement moins efficace pour faire glisser les nucléosomes, même s’il pouvait toujours se lier à l’ADN et aux nucléosomes, parfois même plus fortement que la normale.
Du réglage local de l’espacement au succès global de la réplication
Pour relier ces défauts moléculaires au comportement chromosomique, les auteurs ont reconstitué la chromatine in vitro sur une bibliothèque de fragments d’ADN de levure contenant des centaines d’origines de réplication. Avec l’INO80 normal et le complexe de reconnaissance des origines présents, ils ont observé des réseaux de nucléosomes bien phasés encadrant une zone sans nucléosome à chaque origine. En revanche, l’Arp8 mutant produisait des réseaux moins précis avec des distances de liaison entre nucléosomes altérées. En utilisant un système de réplication entièrement reconstitué, ils ont trouvé que la chromatine assemblée avec l’INO80 mutant favorisait une initiation plus faible aux origines, même si la croissance des fourches de réplication individuelles qui démarraient avait un aspect similaire. Dans des levures vivantes portant les mêmes mutations d’Arp8, l’entrée en synthèse de l’ADN après un arrêt du cycle cellulaire était retardée, les événements de recombinaison spontanée augmentaient et les cellules étaient particulièrement sensibles à l’hydroxyurée, un médicament qui épuise les précurseurs de l’ADN et bloque la réplication. Pourtant, l’expression génique globale, y compris celle des gènes du cycle cellulaire et de la réplication, restait largement inchangée, ce qui indique que le problème principal réside dans l’architecture de la chromatine aux origines plutôt que dans la quantité de facteurs de réplication produits. 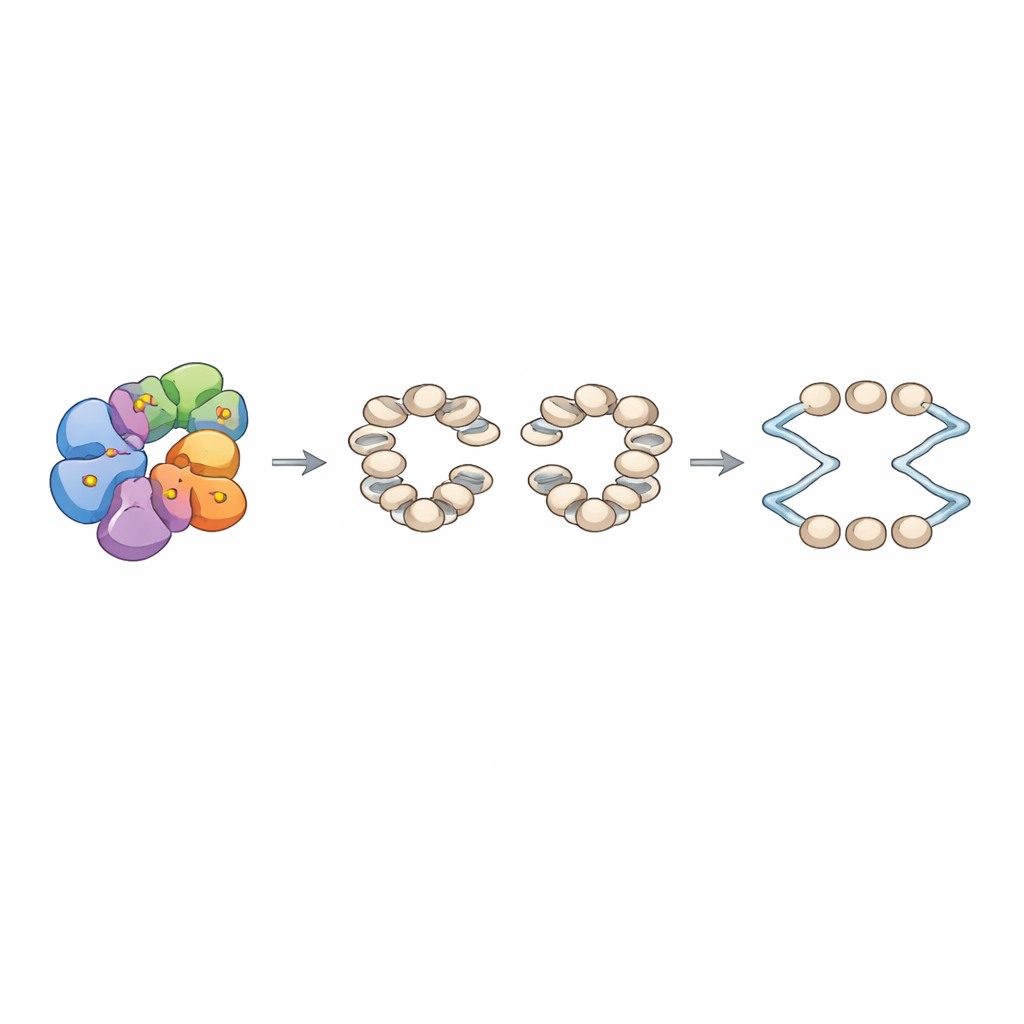
Comment un emballage soigneux de l’ADN protège nos génomes
Pris ensemble, ces travaux révèlent que la DDK fait plus que simplement activer la machinerie de réplication centrale. En phosphorylant Arp8, elle règle finement le remodeler INO80 afin que les nucléosomes autour des origines de réplication soient espacés de manière optimale. Cet empaquetage ordonné semble jouer le rôle de gardien pour un déclenchement efficace des origines et pour le redémarrage sûr des fourches de réplication bloquées sous stress. Sur le plan pratique, l’étude montre que la façon dont l’ADN est enroulé et organisé n’est pas seulement un obstacle que la réplication doit surmonter : c’est une caractéristique active et régulée qui contribue à déterminer quand et où la réplication commence, avec des implications directes pour le maintien de la stabilité du génome.
Citation: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
Mots-clés: Réplication de l’ADN, remodelage de la chromatine, kinase du cycle cellulaire, stabilité du génome, modèle de levure