Clear Sky Science · pl
Kinaza zależna od Dbf4 dopracowuje funkcję Ino80 przy początkach replikacji chromosomów
Dlaczego to ma znaczenie dla naszego DNA
Za każdym razem, gdy komórka się dzieli, musi skopiować całe swoje DNA bez poważnych błędów. Niepowodzenia w tym etapie kopiowania mogą destabilizować genom i są silnie powiązane z rakiem. W tym badaniu odkryto, jak kluczowy enzym cyklu komórkowego nie tylko uruchamia maszynerię do kopiowania DNA, ale też porządkuje lokalne upakowanie DNA, tak aby replikacja mogła się zacząć płynnie i wznowić pod stresem. 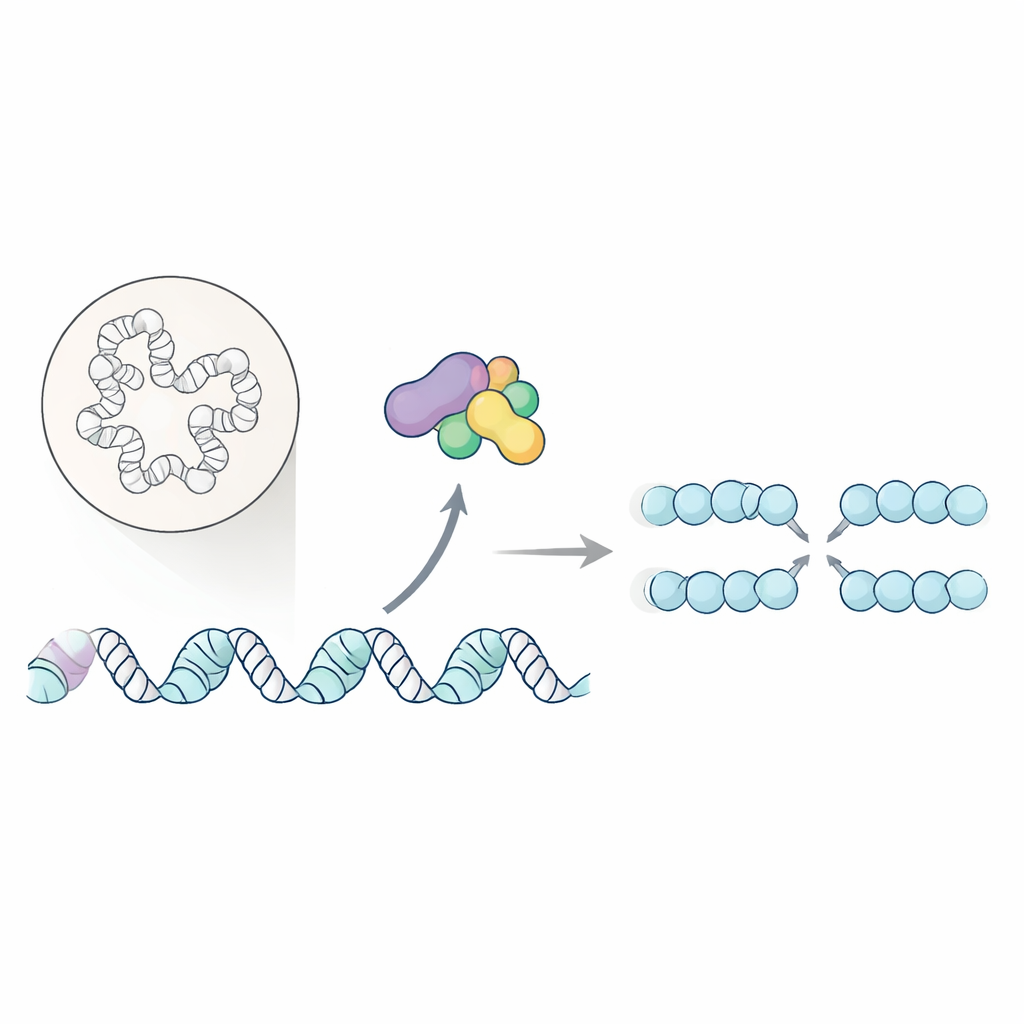
Światło drogowe dla rozpoczynania kopiowania DNA
Komórki polegają na wyspecjalizowanych „originach” wzdłuż chromosomów, w których rozpoczyna się replikacja DNA. Znana para enzymów, kinaza zależna od Dbf4 (DDK), pomaga uruchomić ten proces poprzez modyfikację rdzeniowej maszyny rozplatającej DNA — helikazy. Dotąd znanych było tylko kilka bezpośrednich celów DDK, co pozostawiałoby wiele aspektów jej roli niejasnymi. Autorzy postanowili zmapować na skalę globalną, które białka jądrowe zależą od DDK w zakresie fosforylacji — chemicznego znacznika, który często służy jako przełącznik on/off funkcji białka.
Przeszukiwanie jądra w poszukiwaniu ukrytych partnerów DDK
Aby to osiągnąć, badacze użyli drożdży pączkujących jako modelu i połączyli dwie komplementarne strategie osłabienia aktywności DDK in vivo: mutant wrażliwy na temperaturę podjednostki katalitycznej oraz stres replikacyjny indukowany lekiem, który pośrednio blokuje działanie DDK. Następnie izolowali jądra i użyli spektrometrii mas do skatalogowania tysięcy zfosforylowanych fragmentów białek, porównując próbki z aktywnym i zahamowanym DDK. Skupiając się na miejscach, których poziom fosforylacji obniżał się w obu schematach inaktywacji, zbudowali listę wysokiego zaufania obejmującą około 400 celów zależnych od DDK. Wiele z tych białek było związanych z chromatyną — materiałem DNA–białko organizującym genom — co sugeruje, że DDK ma szerszą rolę w kształtowaniu fizycznego krajobrazu, w którym zachodzi replikacja.
Maszyna remodelująca dostrojona przez mały ogon białkowy
Wśród najsilniejszych trafień znalazł się Arp8, część dużego kompleksu remodelującego chromatynę nazwanego kompleksem INO80. INO80 jest znane z przesuwania nukleosomów — struktur przypominających paciorki DNA owiniętego wokół białek histonowych — oraz z układania ich w regularne szeregi wokół originów replikacyjnych. Zespół wykazał biochemicznie, że DDK bezpośrednio fosforyluje dwa konkretne seryny w nieuporządkowanym końcu Arp8. Gdy zastąpili te seryny alaninami, które nie mogą być fosforylowane, ogólny skład INO80 pozostał niezmieniony, ale jego wewnętrzna architektura uległa zmianie: eksperymenty z krzyżowaniem wykazały osłabione kontakty między kluczowymi modułami kompleksu. Funkcjonalnie zmutowany INO80 używał ATP znacznie wolniej i był wyraźnie gorszy w przesuwaniu nukleosomów, choć wciąż mógł wiązać DNA i nukleosomy, czasami nawet mocniej niż normalnie.
Od lokalnego rozmieszczenia do globalnego sukcesu replikacji
Aby powiązać te molekularne defekty z zachowaniem chromosomów, autorzy odtworzyli chromatynę in vitro na bibliotece fragmentów DNA drożdży zawierających setki originów replikacyjnych. Przy obecnym normalnym INO80 i kompleksie rozpoznającym origin obserwowali schludnie sfazowane szeregi nukleosomów otaczające wolną od nukleosomu przerwę przy każdym originie. W przeciwieństwie do tego, mutacja Arp8 dawała mniej precyzyjne szeregi z zmienionymi odległościami łącznikowymi między nukleosomami. Korzystając z w pełni zrekonstytuowanego układu replikacyjnego, stwierdzili, że chromatyna zmontowana z mutantowym INO80 wspierała słabsze inicjacje przy originach, choć rozrost poszczególnych pasm replikacyjnych, które się rozpoczęły, wyglądał podobnie. W żywych drożdżach noszących te same mutacje Arp8, wejście w syntezę DNA po zatrzymaniu cyklu komórkowego było opóźnione, zwiększyła się liczba spontanicznych zdarzeń rekombinacyjnych, a komórki były szczególnie wrażliwe na hydroksyureę — lek wyczerpujący prekursory DNA i zatrzymujący replikację. Jednak globalna ekspresja genów, w tym genów cyklu komórkowego i replikacji, pozostała w dużej mierze niezmieniona, co wskazuje, że główny problem leży w architekturze chromatyny przy originach, a nie w tym, ile czynników replikacji jest wytwarzanych.
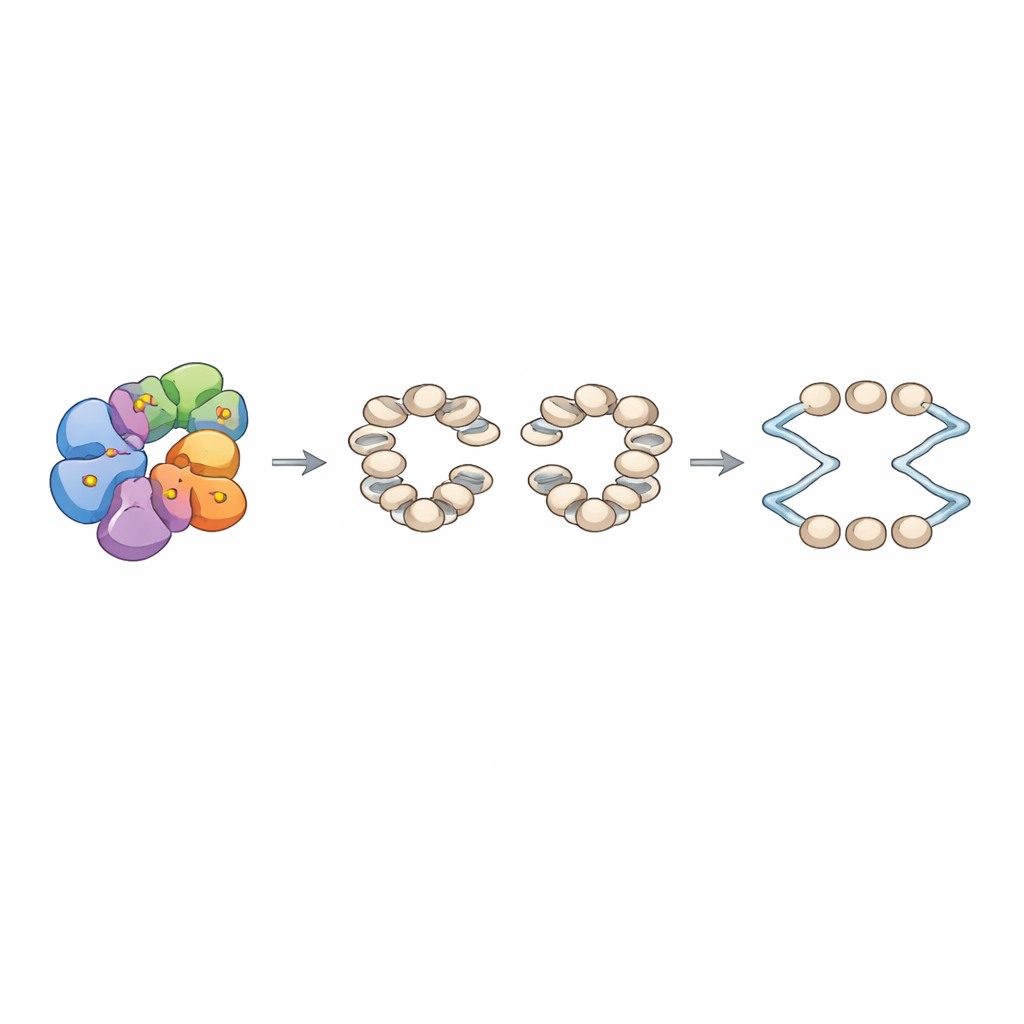
Jak staranne upakowanie DNA chroni nasze genomy
Podsumowując, praca pokazuje, że DDK robi więcej niż tylko włącza podstawową maszynerię replikacyjną. Poprzez fosforylację Arp8 dostraja remodeler INO80 tak, aby nukleosomy wokół originów były ustawione w odpowiednich odstępach. To uporządkowane upakowanie wydaje się pełnić rolę strażnika efektywnego zapalania originów i bezpiecznego wznawiania zatrzymanych wideł replikacyjnych pod stresem. W praktycznym wymiarze badanie dowodzi, że sposób, w jaki DNA jest owinięte i uporządkowane, nie jest jedynie przeszkodą, którą replikacja musi pokonać — jest aktywną, regulowaną cechą, która pomaga określić kiedy i gdzie replikacja się zaczyna, z bezpośrednimi konsekwencjami dla utrzymania stabilności genomu.
Cytowanie: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
Słowa kluczowe: Replikacja DNA, remodeling chromatyny, kinaza cyklu komórkowego, stabilność genomu, model drożdżowy