Clear Sky Science · de
Dbf4‑abhängige Kinase optimiert die Ino80‑Funktion an Replikationsursprüngen der Chromosomen
Warum das für unsere DNA wichtig ist
Jedes Mal, wenn eine Zelle sich teilt, muss sie ihre gesamte DNA ohne gravierende Fehler kopieren. Versagen in diesem Kopierschritt kann das Genom destabilisieren und steht in enger Verbindung mit Krebs. Diese Studie zeigt, wie ein zentrales Enzym des Zellzyklus nicht nur die Replikationsmaschinerie einschaltet, sondern zugleich die lokale Verpackung der DNA so zurechtstutzt, dass die Replikation reibungslos starten und sich unter Stress wieder aufnehmen lässt. 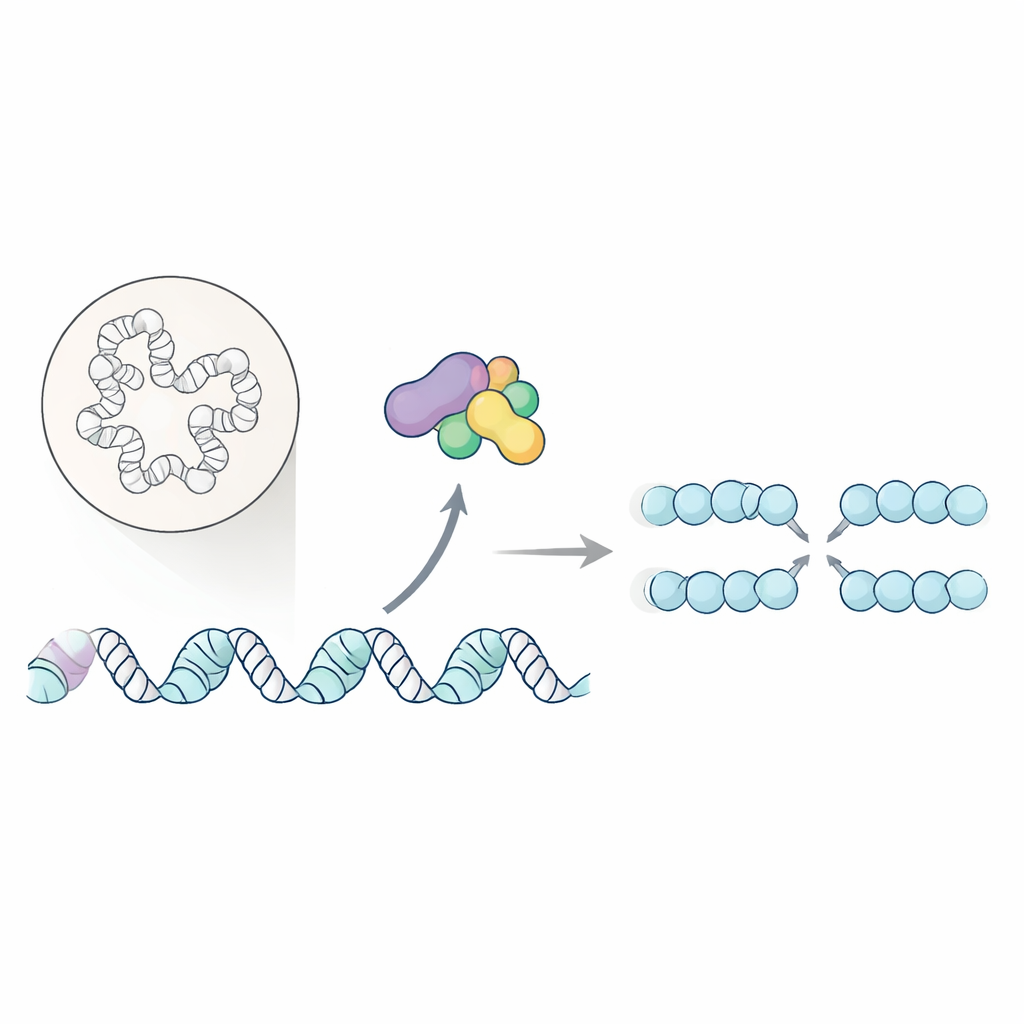
Ein Ampelsystem für den Start der DNA‑Kopie
Zellen verlassen sich auf spezialisierte „Ursprünge“ entlang ihrer Chromosomen, an denen die DNA‑Replikation beginnt. Ein bekanntes Enzympaar, die Dbf4‑abhängige Kinase (DDK), hilft beim Start, indem es die zentrale DNA‑Aufwickelmaschine, die Helikase, modifiziert. Bislang waren nur wenige direkte Ziele von DDK bekannt, sodass ein Großteil seiner Rolle unklar blieb. Die Autoren wollten daher auf globaler Ebene kartieren, welche nukleären Proteine von DDK‑abhängiger Phosphorylierung abhängig sind — ein chemischer Markierungsmechanismus, der oft als Ein/Aus‑Schalter für Proteinfunktionen fungiert.
Das Nukleus‑Scannen nach DDKs verborgenen Partnern
Dazu verwendeten die Forscher die Brotbackhefe als Modell und kombinierten zwei komplementäre Strategien, um die DDK‑Aktivität in lebenden Zellen zu drosseln: einen temperatursensitiven Mutanten seiner katalytischen Untereinheit und einen medikamentös induzierten Replikationsstress, der DDK indirekt blockiert. Anschließend isolierten sie Zellkerne und nutzten Massenspektrometrie, um Tausende phosphorylierter Peptide zu katalogisieren und Proben mit aktiver gegenüber gehemmter DDK zu vergleichen. Indem sie sich auf Positionen konzentrierten, die in beiden Hemmungsbedingungen abnahmen, erstellten sie eine Liste mit hoher Zuverlässigkeit von etwa 400 DDK‑abhängigen Zielen. Viele dieser Proteine sind an Chromatin gebunden, dem DNA‑Protein‑Material, das das Genom organisiert, was darauf hindeutet, dass DDK eine weiterreichende Rolle bei der Gestaltung der physischen Landschaft hat, in der die Replikation stattfindet.
Eine Remodeler‑Maschine, abgestimmt durch einen kurzen Protein‑Schwanz
Unter den stärksten Treffern fand sich Arp8, ein Bestandteil einer großen Chromatin‑Remodelling‑Maschine namens INO80‑Komplex. INO80 ist dafür bekannt, Nukleosomen — die kugeligen Strukturen, in denen DNA um Histone gewickelt ist — neu anzuordnen und sie rund um Replikationsursprünge in regelmäßigen Arrays zu positionieren. Das Team zeigte biochemisch, dass DDK zwei spezifische Serine in einem ungeordneten C‑Terminalen Schwanz von Arp8 direkt phosphoryliert. Wenn diese Serine durch Alanine ersetzt wurden, die nicht phosphoryliert werden können, blieb die Gesamtzusammensetzung des INO80‑Komplexes erhalten, aber seine interne Architektur veränderte sich: Crosslinking‑Experimente zeigten geschwächte Kontakte zwischen wichtigen Modulen des Komplexes. Funktionell verbrauchte der mutierte INO80 ATP deutlich langsamer und war erheblich schlechter im Verschieben von Nukleosomen, obwohl er weiterhin DNA und Nukleosomen binden konnte — in manchen Fällen sogar fester als normal.
Von lokaler Abstandsregelung zum globalen Replikationserfolg
Um diese molekularen Defekte mit dem Chromosomenverhalten zu verknüpfen, rekonstruierten die Autoren Chromatin in vitro auf einer Bibliothek von Hefe‑DNA‑Fragmenten, die Hunderte von Replikationsursprüngen enthielten. Mit wildtypischem INO80 und dem Origin Recognition Complex beobachteten sie ordentlich phasierte Nukleosom‑Arrays, die an jedem Ursprung eine Nukleosomfreie Lücke flankierten. Im Gegensatz dazu erzeugte der Arp8‑Mutant weniger präzise Arrays mit veränderten Verbindungsabständen zwischen den Nukleosomen. In einem vollständig rekonstruierten Replikationssystem zeigte sich, dass Chromatin, das mit mutiertem INO80 assembliert wurde, eine schwächere Initiation an Ursprüngen unterstützte, obwohl das Wachstum einzelner Replikationsstränge, die einmal begonnen hatten, ähnlich war. In lebenden Hefezellen mit denselben Arp8‑Mutationen verzögerte sich der Eintritt in die DNA‑Synthese nach Zellzyklus‑Arrest, spontane Rekombinationsereignisse nahmen zu, und die Zellen waren besonders empfindlich gegenüber Hydroxyurea, einem Wirkstoff, der die DNA‑Bausteine erschöpft und die Replikation zum Stillstand bringt. Die globale Genexpression, einschließlich jener von Zellzyklus‑ und Replikationsgenen, blieb jedoch weitgehend unverändert, was dafür spricht, dass das Hauptproblem in der Chromatin‑Architektur an den Ursprüngen liegt und nicht in der Menge an produzierten Replikationsfaktoren. 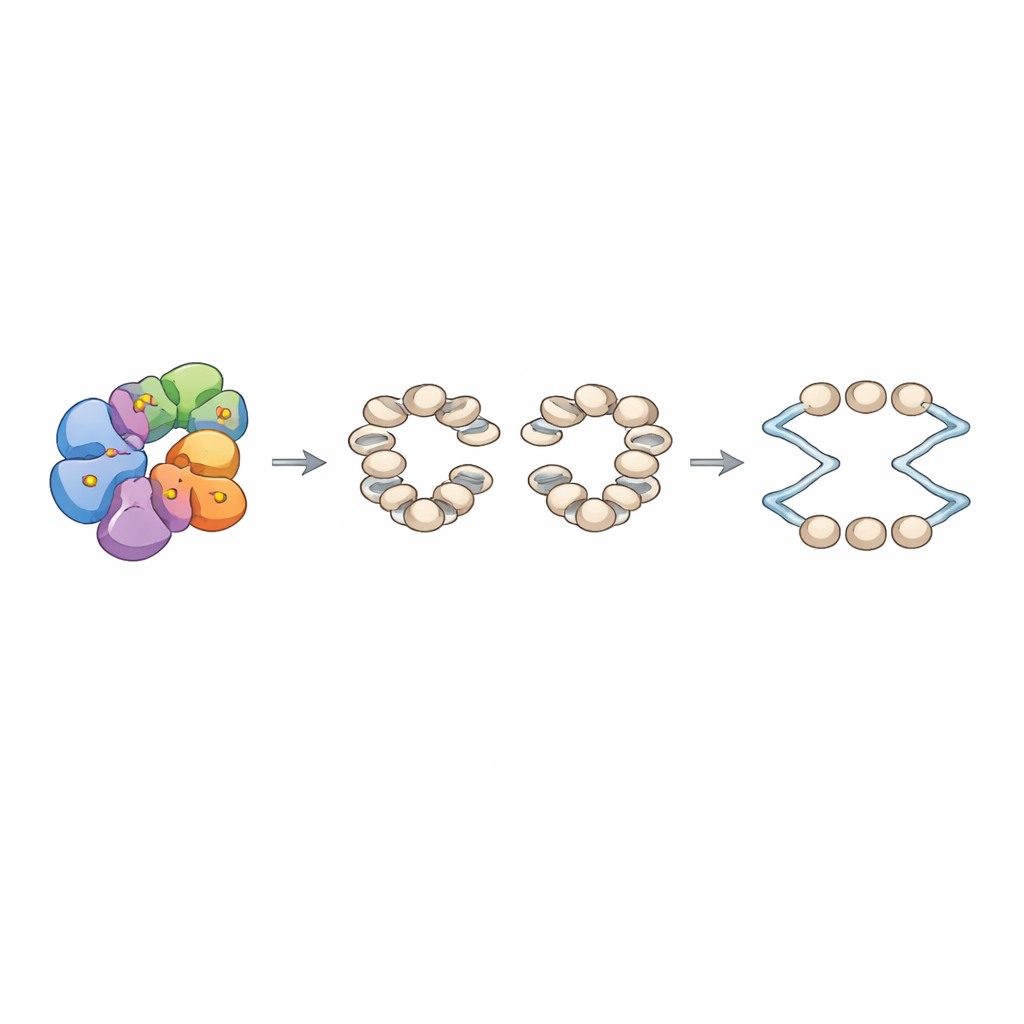
Wie sorgfältige DNA‑Verpackung unsere Genome schützt
In der Summe zeigen die Ergebnisse, dass DDK mehr tut, als nur den Schalter an der Kernreplikationsmaschine umzulegen. Durch die Phosphorylierung von Arp8 stimmt es den INO80‑Remodeler so ab, dass die Nukleosomen um Replikationsursprünge genau richtig verteilt sind. Diese geordnete Verpackung wirkt offenbar als Gatekeeper für effizientes Origin‑Firing und für das sichere Wiederanlaufen gestoppter Replikationsgabeln unter Stress. Praktisch bedeutet das: Die Art und Weise, wie DNA gewickelt und angeordnet ist, ist nicht bloß ein Hindernis, das die Replikation überwinden muss — sie ist ein aktives, reguliertes Merkmal, das mitbestimmt, wann und wo Replikation beginnt, und das direkte Folgen für die Erhaltung der Genomstabilität hat.
Zitation: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
Schlüsselwörter: DNA‑Replikation, Chromatin‑Remodelling, Zellzyklus‑Kinase, Genomstabilität, Hefe‑Modell