Clear Sky Science · pt
A quinase dependente de Dbf4 ajusta finamente a função do Ino80 nas origens de replicação cromossômica
Por que isso importa para o nosso DNA
Cada vez que uma célula se divide, ela precisa copiar todo o seu DNA sem cometer erros graves. Falhas nessa etapa de cópia podem desestabilizar o genoma e estão fortemente associadas ao câncer. Este estudo revela como uma enzima-chave do ciclo celular não apenas ativa a máquina de replicação do DNA, mas também organiza o empacotamento local do DNA para que a replicação possa começar sem problemas e recomeçar sob estresse. 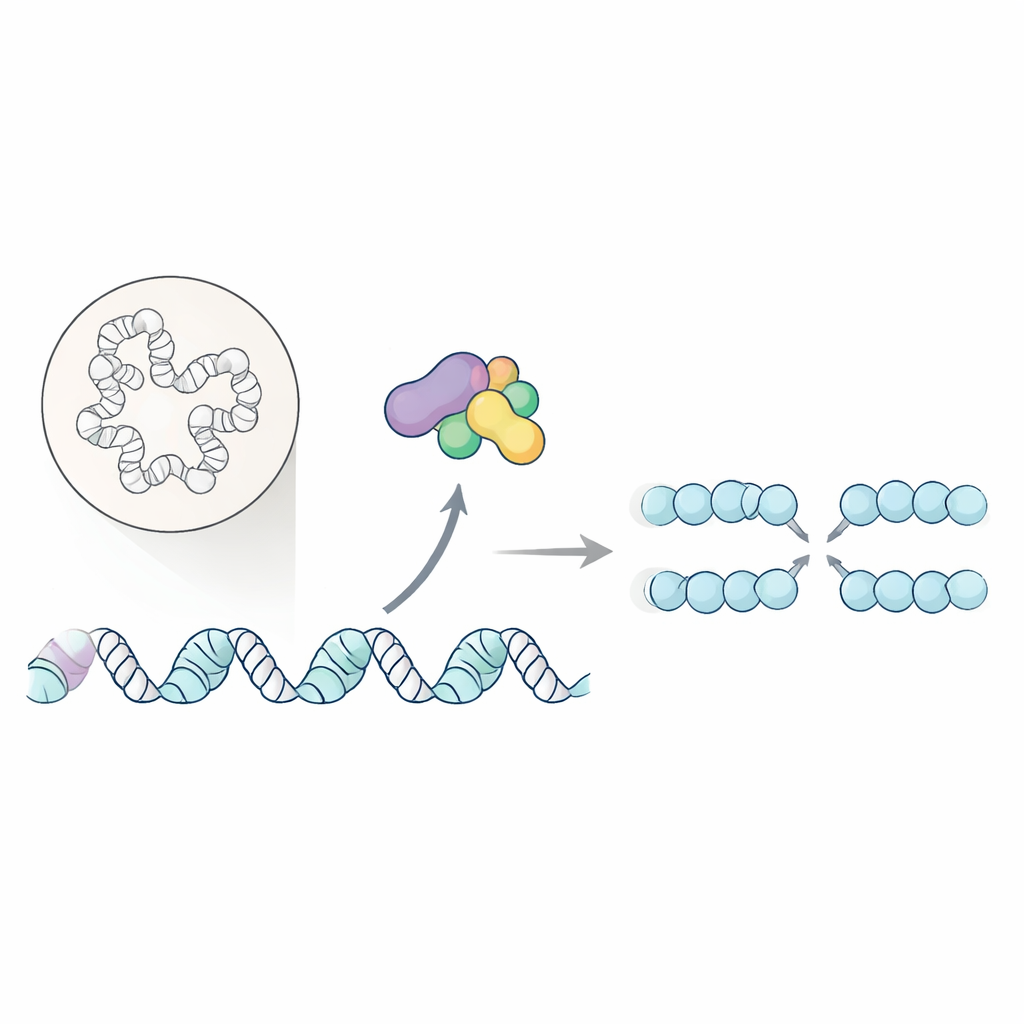
Um semáforo para iniciar a cópia do DNA
As células dependem de “origens” especializadas ao longo dos cromossomos onde a replicação do DNA se inicia. Um par de enzimas bem conhecido, a quinase dependente de Dbf4 (DDK), ajuda a iniciar esse processo modificando a máquina central de desenrolamento do DNA, a helicase. Até agora, poucos alvos diretos da DDK eram conhecidos, deixando grande parte de seu papel obscuro. Os autores partiram para mapear, em escala global, quais proteínas nucleares dependem da DDK para fosforilação — uma marca química que frequentemente funciona como um interruptor liga/desliga da função proteica.
Varrendo o núcleo em busca dos parceiros ocultos da DDK
Para isso, os pesquisadores usaram a levedura de gema como modelo e combinaram duas estratégias complementares para reduzir a atividade da DDK em células vivas: um mutante sensível à temperatura da subunidade catalítica e um estresse de replicação induzido por droga que bloqueia indiretamente a ação da DDK. Em seguida, isolaram núcleos e usaram espectrometria de massa para catalogar milhares de fragmentos proteicos fosforilados, comparando amostras com DDK ativa versus inibida. Ao focar em sítios que diminuíram em ambos os esquemas de inibição, construíram uma lista de alta confiança com cerca de 400 alvos dependentes de DDK. Muitas dessas proteínas estão ligadas à cromatina, o material DNA–proteína que organiza o genoma, sugerindo que a DDK tem um papel mais amplo na modelagem da paisagem física onde a replicação ocorre.
Uma máquina de remodelamento ajustada por uma pequena cauda proteica
Entre os alvos mais fortes estava Arp8, parte de uma grande máquina de remodelamento da cromatina chamada complexo INO80. O INO80 é conhecido por reposicionar nucleossomos — estruturas em forma de contas com DNA enrolado ao redor de histonas — e organizá-los em arranjos regulares ao redor das origens de replicação. A equipe mostrou bioquimicamente que a DDK fosforila diretamente dois serinos específicos em uma cauda não estruturada de Arp8. Quando esses serinos foram substituídos por alaninas, que não podem ser fosforiladas, a composição geral do INO80 permaneceu intacta, mas sua arquitetura interna mudou: experimentos de reticulação revelaram contatos enfraquecidos entre módulos-chave do complexo. Funcionalmente, o INO80 mutante consumiu ATP muito mais devagar e foi marcadamente pior em deslizar nucleossomos para novas posições, embora ainda pudesse se ligar ao DNA e aos nucleossomos, às vezes até com maior afinidade que o normal.
Do espaçamento local ao sucesso global da replicação
Para conectar esses defeitos moleculares ao comportamento dos cromossomos, os autores remontaram cromatina in vitro sobre uma biblioteca de fragmentos de DNA de levedura contendo centenas de origens de replicação. Com INO80 normal e o complexo de reconhecimento de origem presentes, observaram arrays de nucleossomos bem faseados ao flanco de uma lacuna livre de nucleossomos em cada origem. Em contraste, o mutante Arp8 produziu arrays menos precisos com distâncias de enlace alteradas entre nucleossomos. Usando um sistema de replicação totalmente reconstituído, descobriram que a cromatina montada com INO80 mutante suportava início mais fraco nas origens, embora o crescimento de tratos de replicação individuais que se iniciaram parecesse semelhante. Em leveduras vivas carregando as mesmas mutações em Arp8, a entrada na síntese de DNA após parada do ciclo celular foi atrasada, os eventos de recombinação espontânea aumentaram e as células ficaram especialmente sensíveis à hidroxiureia, uma droga que esgota os blocos de construção do DNA e interrompe a replicação. Ainda assim, a expressão gênica global, incluindo a de genes do ciclo celular e da replicação, permaneceu em grande parte inalterada, o que indica que o problema principal está na arquitetura da cromatina nas origens, e não na quantidade de fatores de replicação produzidos.
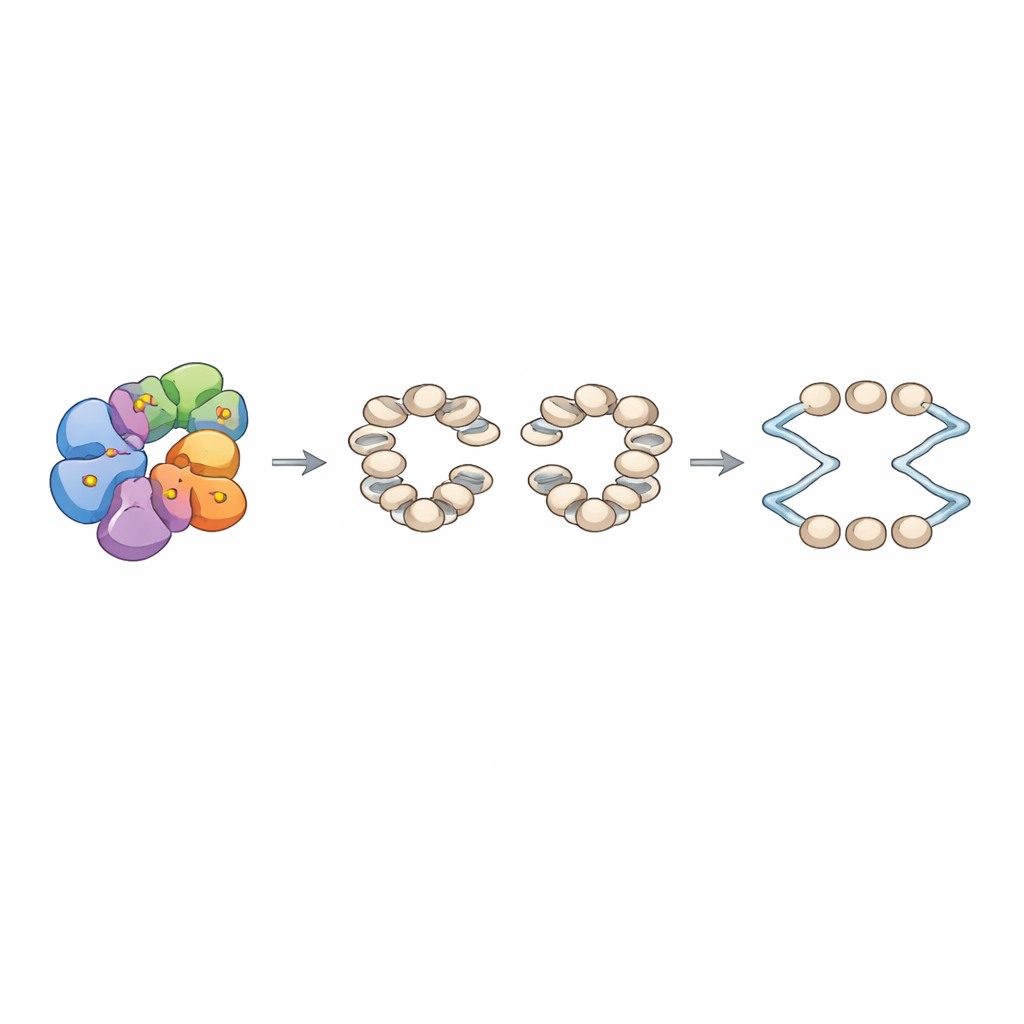
Como o empacotamento cuidadoso do DNA protege nossos genomas
Em conjunto, o trabalho revela que a DDK faz mais do que acionar a máquina central de replicação. Ao fosforilar Arp8, ela ajusta finamente o remodelador INO80 para que os nucleossomos ao redor das origens de replicação fiquem espaçados de maneira adequada. Esse empacotamento ordenado parece funcionar como um guardião para a ativação eficiente das origens e para o reinício seguro de forquilhas de replicação paradas sob estresse. Em termos práticos, o estudo mostra que a forma como o DNA é enrolado e organizado não é apenas um obstáculo a ser superado pela replicação — é uma característica ativa e regulada que ajuda a determinar quando e onde a replicação começa, com implicações diretas para a manutenção da estabilidade do genoma.
Citação: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
Palavras-chave: Replicação do DNA, remodelamento da cromatina, quinase do ciclo celular, estabilidade do genoma, modelo de levedura