Clear Sky Science · sv
Dbf4-beroende kinas finjusterar Ino80:s funktion vid kromosomers replikationsorigin
Varför detta är viktigt för vårt DNA
Vid varje celldelning måste hela cellens DNA kopieras utan större fel. Misslyckanden i detta kopieringssteg kan destabilisera genomet och är starkt kopplade till cancer. Denna studie avslöjar hur ett nyckelenzym i cellcykeln inte bara sätter igång själva replikationsmaskineriet, utan också städar upp den lokala paketeringen av DNA så att replikationen kan starta smidigt och återstarta under stress. 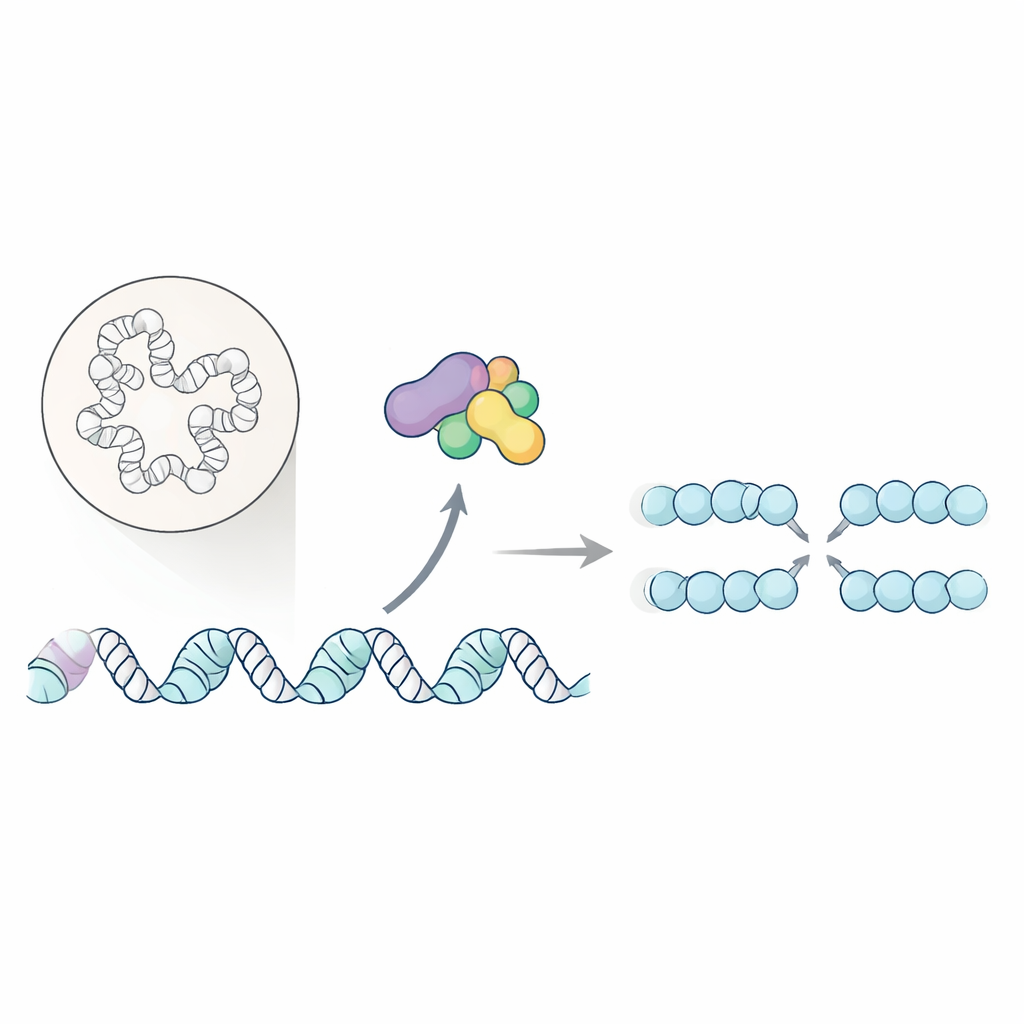
Ett trafikljus för att starta DNA-kopiering
Cellernas replikation börjar vid specialiserade "origin" längs kromosomerna. Ett välkänt enzympar kallat Dbf4-beroende kinas (DDK) hjälper till att starta processen genom att modifiera den centrala DNA-uppvridande maskinen, helikasen. Hittills var bara några få direkta mål för DDK kända, vilket lämnat mycket av dess roll mystisk. Författarna satte därför ut för att kartlägga, i stor skala, vilka nukleära proteiner som är beroende av DDK för fosforylering — en kemisk märkning som ofta fungerar som en på/av-brytare för proteiners funktion.
Skanning av nukleus för DDK:s dolda partners
För att göra detta använde forskarna knoppjäst som modell och kombinerade två kompletterande strategier för att dämpa DDK-aktivitet i levande celler: en temperaturkänslig mutant av dess katalytiska subenhet och en läkemedelsinducerad replikationsstress som indirekt blockerar DDK:s verkan. De isolerade sedan kärnor och använde masspektrometri för att katalogisera tusentals fosforylerade proteinklyvningar, och jämförde prover med aktiv respektive hämmad DDK. Genom att fokusera på platser som minskade i båda hämningsuppläggen byggde de en lista med hög konfidens på cirka 400 DDK-beroende mål. Många av dessa proteiner är bundna till kromatin, det DNA–proteinmaterial som organiserar genomet, vilket antyder att DDK har en bredare roll i att forma det fysiska landskapet där replikation sker.
En omformningsmaskin finjusterad av en liten proteintail
Bland de starkaste träffarna fanns Arp8, en del av en stor kromatinomformningsmaskin kallad INO80-komplexet. INO80 är känt för att omplacera nukleosomer — pärl-liknande strukturer där DNA är lindat runt histonproteiner — och att ordna dem i regelbundna rader runt replikationsorigin. Gruppen visade biokemiskt att DDK direkt fosforylerar två specifika seriner i en ostrukturerad tail hos Arp8. När de ersatte dessa seriner med alaniner, som inte kan fosforyleras, förblev INO80:s övergripande sammansättning intakt, men dess interna arkitektur ändrades: korsbindningsexperiment visade försvagade kontakter mellan nyckelmoduler i komplexet. Funktionellt förbrukade den mutanta INO80 ATP mycket långsammare och var märkbart sämre på att skjuta nukleosomer till nya positioner, även om den fortfarande kunde binda DNA och nukleosomer, ibland till och med starkare än normalt.
Från lokal avståndsättning till global replikationsframgång
För att koppla dessa molekylära defekter till kromosombeteende återuppbyggde författarna kromatin in vitro på ett bibliotek av jäst-DNA-fragment som innehöll hundratals replikationsorigin. Med normal INO80 och origin recognition complex närvarande observerade de prydligt fasade nukleosomrader som flankade ett nukleosomfritt gap vid varje origin. I kontrast producerade Arp8-mutanten mindre precisa rader med förändrade länkavstånd mellan nukleosomer. Med ett fullständigt rekonstituerat replikationssystem fann de att kromatin monterat med mutant INO80 stödde svagare initiering vid origin, även om tillväxten av individuella replikationsspår som väl startade såg liknande ut. I levande jäst som bar samma Arp8-mutationer försenades insättningen i DNA-syntes efter cellcykelarrest, spontana rekombinationsevent ökade och cellerna var särskilt känsliga för hydroxyurea, ett läkemedel som tömmer DNA-byggstenar och stannar replikation. Samtidigt var den globala genuttrycksprofilen, inklusive gener för cellcykeln och replikation, till stor del oförändrad, vilket talar för att huvudproblemet ligger i kromatinarkitekturen vid origin snarare än i hur många replikationsfaktorer som bildas. 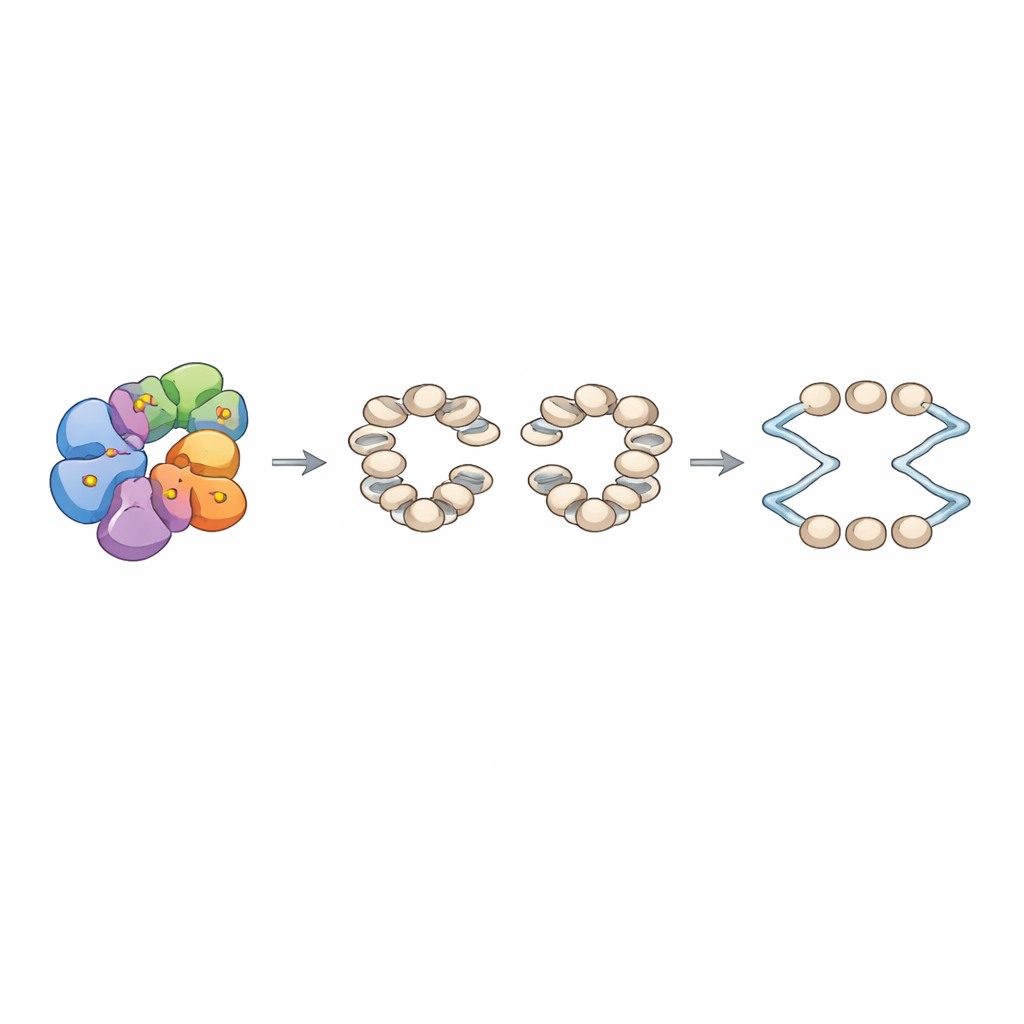
Hur noggrann DNA-packning skyddar våra genom
Sammantaget visar arbetet att DDK gör mer än att bara slå på kärnreplikationsmaskineriet. Genom att fosforylera Arp8 finjusterar det INO80-remodelern så att nukleosomer runt replikationsorigin får precis rätt avstånd. Denna ordnade packning verkar vara en grindvakt för effektiv origin-aktivering och för säker återstart av stillastående replikationsgafflar under stress. I praktiska termer visar studien att hur DNA är lindat och arrangerat inte bara är ett hinder som replikationen måste övervinna — det är en aktiv, reglerad egenskap som hjälper avgöra när och var replikation börjar, med direkt betydelse för att bevara genomstabiliteten.
Citering: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
Nyckelord: DNA-replikation, kromatinomformning, cellcykel-kinas, genomstabilitet, jästmodell