Clear Sky Science · ru
Киназа, зависящая от Dbf4, тонко настраивает функцию Ino80 на начальных участках репликации хромосом
Почему это важно для нашей ДНК
Каждый раз при делении клетки ей нужно точно скопировать всю ДНК без серьёзных ошибок. Сбои на этом этапе репликации могут дестабилизировать геном и тесно связаны с возникновением рака. В этом исследовании показано, как ключевой фермент клеточного цикла не только запускает аппарат копирования ДНК, но и упорядочивает локальную упаковку ДНК, чтобы репликация начиналась плавно и могла возобновляться при стрессовых условиях. 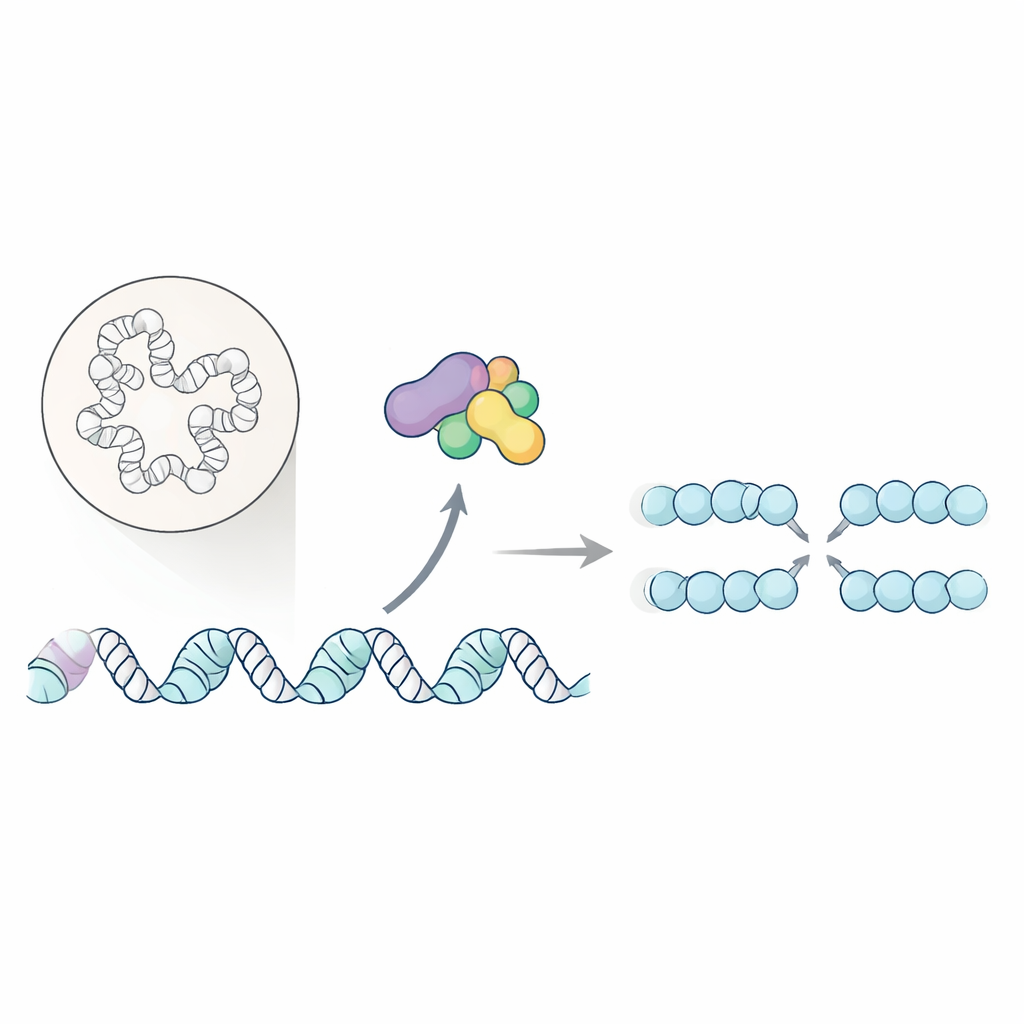
Светофор для запуска копирования ДНК
Клетки полагаются на специализированные «источники» вдоль хромосом, где начинается репликация ДНК. Хорошо известная пара ферментов под названием киназа, зависящая от Dbf4 (DDK), помогает запустить этот процесс, модифицируя основной аппарат разворачивания ДНК — геликазу. До сих пор было известно лишь несколько прямых мишеней DDK, и многие аспекты её роли оставались неясными. Авторы поставили цель глобально определить, какие ядерные белки зависят от DDK в плане фосфорилирования — химической метки, часто служащей переключателем активности белка.
Сканирование ядра в поисках скрытых партнёров DDK
Для этого исследователи использовали дрожжи Saccharomyces как модель и комбинировали две дополняющие друг друга стратегии для ослабления активности DDK в живых клетках: температурно-чувствительный мутант каталитической субъединицы и индуцируемый препаратом репликационный стресс, который косвенно блокирует действие DDK. Затем они выделили ядра и с помощью масс-спектрометрии каталогизировали тысячи фосфорилированных фрагментов белков, сравнивая образцы с активной и ингибированной DDK. Сосредоточившись на сайтах, уровень фосфорилирования которых снижался в обеих схемах ингибирования, они составили список с высоким уровнем достоверности примерно из 400 DDK-зависимых мишеней. Многие из этих белков связаны с хроматином — ДНК‑белковым материалом, который организует геном — что указывает на более широкую роль DDK в формировании физического ландшафта, где происходит репликация.
Механизм ремоделирования, настроенный маленьким хвостиком белка
Одной из самых сильных находок оказался Arp8, компонент большого комплекса ремоделирования хроматина INO80. Известно, что INO80 перемещает нуклеосомы — шарообразные структуры ДНК, обёрнутой вокруг гистонов — и выстраивает их в регулярные ряды вокруг источников репликации. Команда биохимически показала, что DDK напрямую фосфорилирует две конкретные серины в неструктурированном хвосте Arp8. Когда эти серины заменяли на аланин, который не может быть фосфорилирован, общий состав комплекса INO80 оставался целым, но его внутренняя архитектура менялась: эксперименты с кросс‑линкингом выявили ослабление контактов между ключевыми модулями комплекса. Функционально мутантный INO80 расходовал АТФ заметно медленнее и значительно хуже сдвигал нуклеосомы, хотя при этом он по‑прежнему мог связываться с ДНК и нуклеосомами, иногда даже прочнее, чем нормальный комплекс.
От локального размещения до глобального успеха репликации
Чтобы связать эти молекулярные дефекты с поведением хромосом, авторы воссоздали хроматин in vitro на библиотеке фрагментов дрожжевой ДНК с сотнями источников репликации. При наличии нормального INO80 и комплекса распознавания источников они наблюдали аккуратно упорядоченные ряды нуклеосом по обе стороны от участка без нуклеосомы у каждого источника. В отличие от этого, мутант Arp8 формировал менее точные массивы с изменёнными расстояниями между звеньями (linker) нуклеосом. В полностью реконституированной системе репликации хроматин, собранный с мутантным INO80, поддерживал более слабый старт на источниках, хотя рост отдельных репликационных «трактов», когда они запускались, выглядел похожим. В живых дрожжах с теми же мутациями Arp8 вход в синтез ДНК после остановки клеточного цикла задерживался, спонтанные события рекомбинации увеличивались, и клетки особенно чувствительны к гидроксиуре — веществу, истощающему строительные блоки ДНК и останавливающему репликацию. При этом глобальная экспрессия генов, включая гены клеточного цикла и репликации, в основном не изменялась, что указывает на то, что основная проблема — в архитектуре хроматина на источниках, а не в количестве синтезируемых факторов репликации. 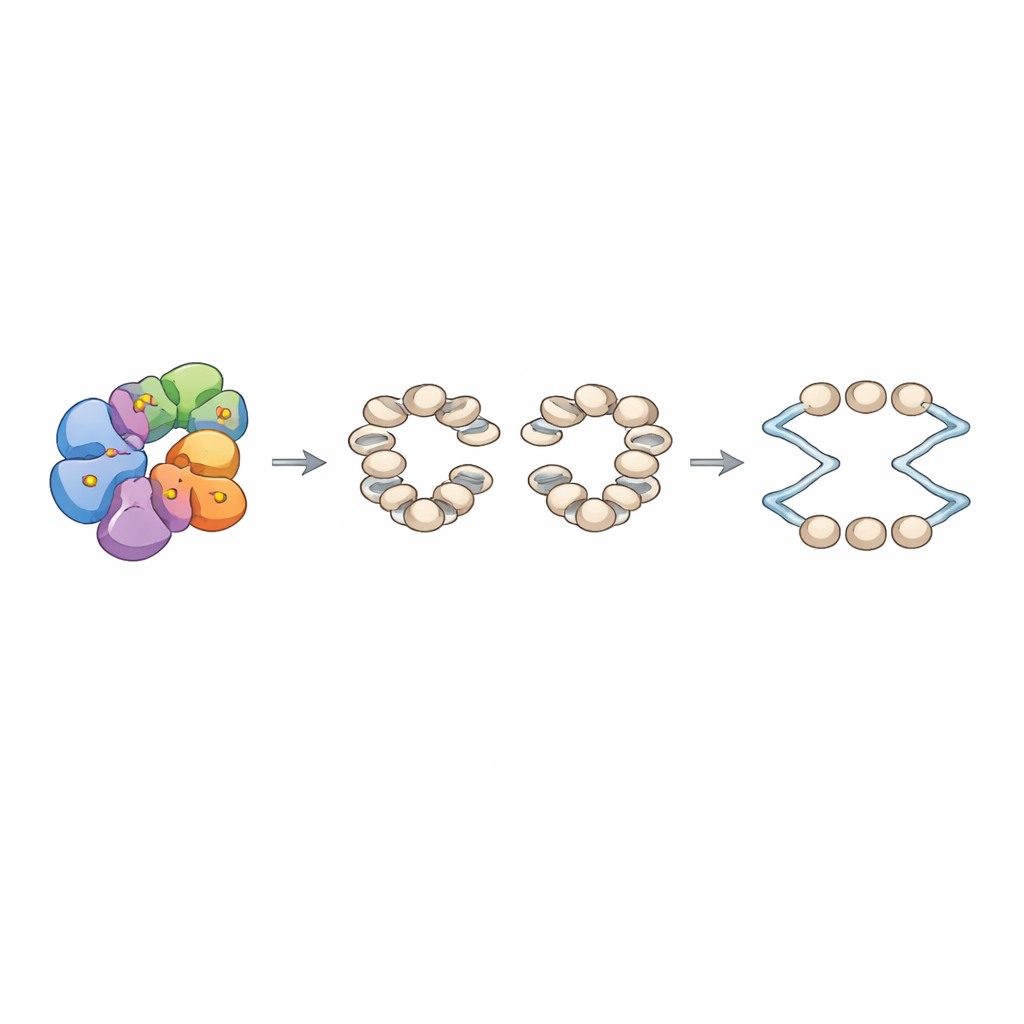
Как аккуратная упаковка ДНК защищает наши геномы
В сумме работа показывает, что DDK делает больше, чем просто включает основной аппарат репликации. Фосфорилируя Arp8, она тонко настраивает ремоделер INO80 так, чтобы нуклеосомы вокруг источников репликации располагались с нужным интервалом. Такое упорядоченное расположение, по-видимому, служит «пропускным контролем» для эффективного запуска источников и для безопасного возобновления застрявших репликационных вилок при стрессе. Практически это исследование демонстрирует, что способ, которым ДНК обёрнута и организована, — это не просто препятствие для репликации, которое нужно преодолеть, а активная, регулируемая черта, помогающая определить, когда и где начинается репликация, с прямыми последствиями для поддержания стабильности генома.
Цитирование: Bansal, P., Lahiri, S., Kumar, C.N. et al. Dbf4-dependent kinase finetunes Ino80 function at chromosome replication origins. Nat Commun 17, 3029 (2026). https://doi.org/10.1038/s41467-026-70698-4
Ключевые слова: репликация ДНК, ремоделирование хроматина, киназа клеточного цикла, стабильность генома, модель на дрожжах