Clear Sky Science · zh
磁控多功能光电导管用于体内化学成像与精确引导肿瘤治疗
更聪明的工具,用于发现与治疗隐匿肿瘤
癌症医生越来越依赖微创技术,通过将细小导管穿过血管或体腔到达难以接触的肿瘤。然而,当今的工具在精确操控、清晰识别肿瘤边界以及在不损伤健康组织的前提下递送治疗方面仍存在困难。本研究提出了一种新型微小磁控导管,旨在穿越复杂解剖结构、实时感知肿瘤的化学特征,并在所需位置提供定向治疗——目标是使癌症治疗更精确且对身体其他部分更温和。
为什么肿瘤边界如此难以看清
标准的癌症治疗仍然大量依赖活检、影像学检查、手术、化疗和放疗。尽管这些方法能挽救生命,但也存在盲点。单次活检样本可能错过分布不均或形状不规则的肿瘤区域,而从取样到治疗之间的漫长等待会延迟关键决策。外科医生往往难以直视肿瘤与正常组织的真实边界,这增加了留下残余癌细胞的风险。同时,全身性化疗和放疗是对整个机体施加治疗,因而会产生副作用,难以区分病变细胞与健康细胞。作者认为,需要一种能够在体内灵活移动、现场绘制肿瘤化学生态并仅在真正需要的位置集中施治的工具。
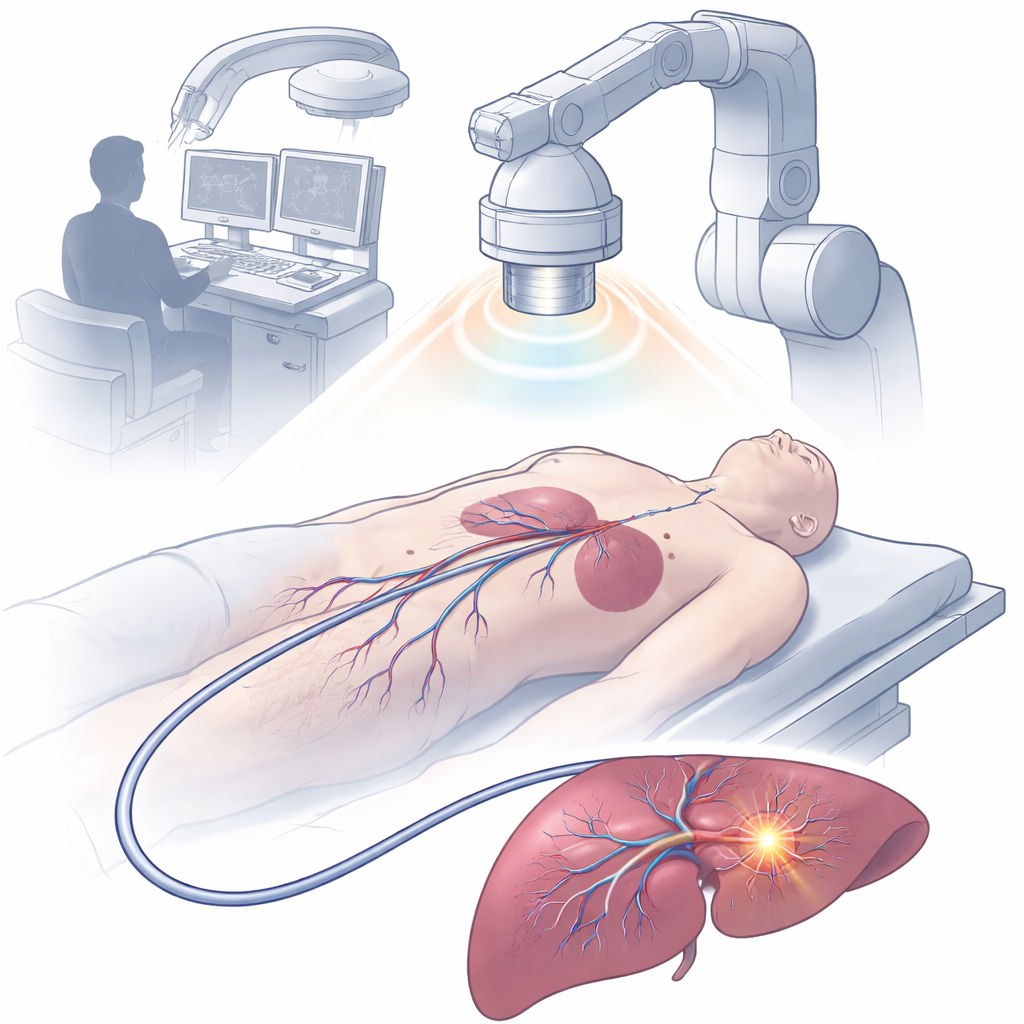
一款功能丰富的微小磁控导管
研究团队制造了一种直径2.5毫米的装置,称为磁驱动多功能光电导管(MDMOC)。借助先进的三维多轴打印,他们组装了一个柔性轴体,内含液态金属通道以实现电导、用于光传输的光纤、药物输送的空腔通道,以及用于操控与X光可视化的环形磁体。导管尖端覆以小型聚合物头,头部带有菱形孔隙,允许局部液体在受保护的传感电极周围流动。外层薄型水凝胶涂层使导管表面更光滑,减少与组织的摩擦,帮助其安全穿行血管与器官。尽管体积小,MDMOC可被外部磁场远程弯曲与定向,使其能够穿过急弯和复杂的血管分支。
实时读取肿瘤的化学指纹
这款导管的独特之处在于其内建的“化学之眼”。尖端装有四个微型电化学传感器,持续测量肿瘤与健康组织之间存在差异的关键标志物:酸度(pH)、过氧化氢、钾离子和与细胞应激及防御相关的谷胱甘肽。在实验室测试中,每个传感器即使在其他常见体内化合物存在时,也表现出高灵敏度、选择性和稳定性。在带肝肿瘤的兔子实验中,导管可被磁控通过腹部小开口引导至疑似病灶位置。通过在多个点采样,研究团队构建了详细的化学图谱,显示出肿瘤与正常组织交界处的陡峭梯度。将四个传感器的数据融合为单一“融合”图能将边界检测精度提高到亚毫米级,并与超声成像及组织学金标准结果高度一致。
从成像到靶向治疗
除了用于诊断,MDMOC还被设计为能执行治疗。通过其内部通道,它将低于全身给药量的高浓度光敏药物直接注入肿瘤,随后光纤发出红光以触发光动力治疗,使药物产生活性氧类物质来杀死周围的癌细胞。在肝癌小鼠模型中,这种局部化策略相比经皮给药或仅有照光的对照组,带来了更明显的肿瘤缩小、更小的终末肿瘤体积以及更多的癌细胞死亡,且没有显著体重下降或主要器官损伤。重要的是,同一导管在治疗前及治疗过程中也能测量肿瘤化学情况,从而在几分钟内实现快速的“感知—决策—治疗”闭环,而不是延续数日。
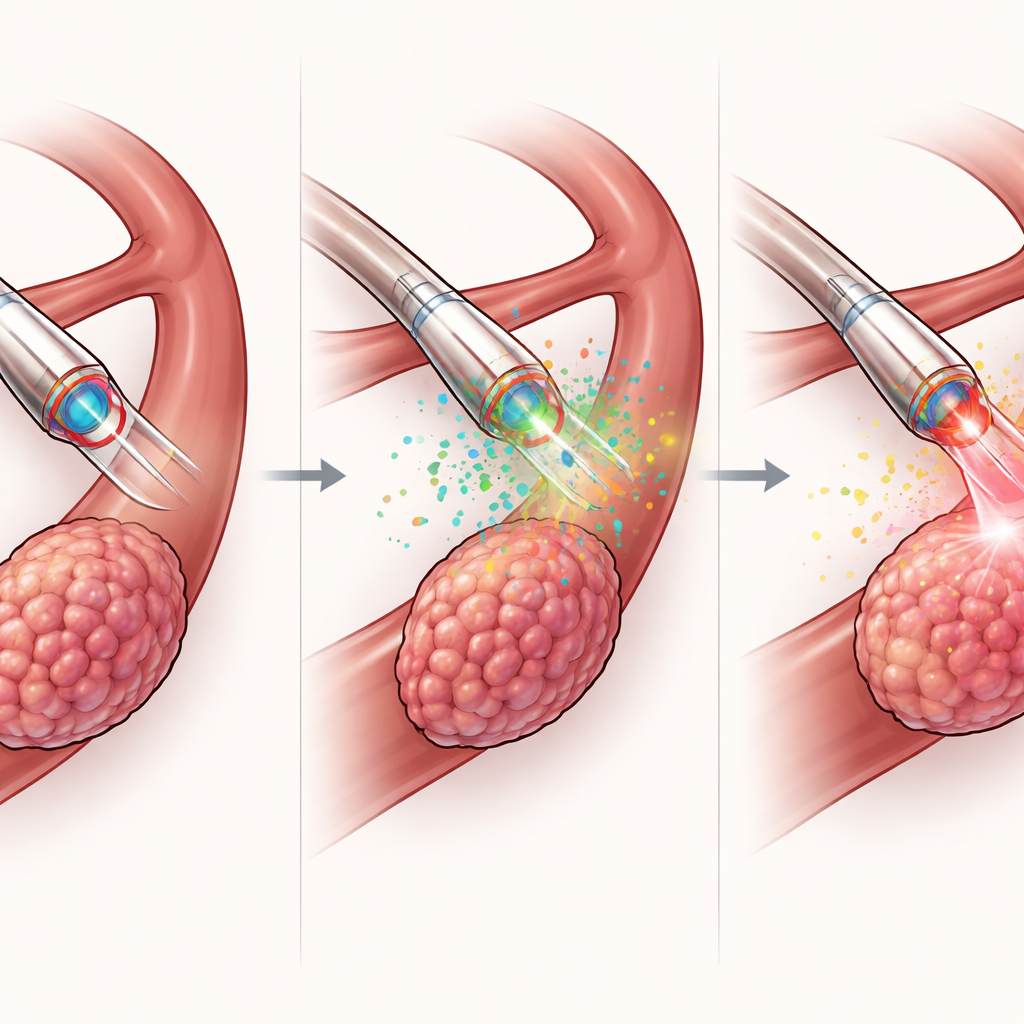
在更大、更接近真实的体内测试装置
为评估该技术向临床转化的前景,研究者在猪身上测试了更长版本的导管,猪的血管与器官更接近人类。在X光成像与磁控下,MDMOC从大静脉进入肝静脉和肾静脉的狭窄分支,能够通过传统导管难以应对的急弯。它能将造影剂精确输送到这些分支而不致渗漏,并且在腹腔镜引导下可穿刺肝表面和膀胱壁的特定位置进行体内传感与模拟治疗。即便在心跳导致的器官运动下,磁控导管仍能在目标位点保持稳定,显示出其在真实影像引导操作中的潜力。
这对未来癌症护理可能意味着什么
本质上,这项工作指向一类新的智能磁控导管,将导航、化学成像与定向治疗整合在一根细长工具中。通过实时读取肿瘤的化学生态并利用该信息将药物和光精准送达最有效的位置,MDMOC有望帮助外科医生更准确地界定肿瘤边界、保护健康组织并减少全身副作用。尽管在人体应用前仍需更多研究,特别是扩大可检测生物标志物的范围并将系统针对特定癌种进行定制,但这一概念展现了微创癌症治疗的新愿景——不只是由影像引导,而是由肿瘤自身的化学特征来引导。
引用: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
关键词: 磁控导管, 肿瘤微环境, 微创癌症治疗, 实时生物传感, 光动力治疗