Clear Sky Science · de
Magnetisch gesteuerter multifunktionaler optoelektronischer Katheter für in vivo-Chemiekartierung und präzise geführte Tumortherapie
Intelligentere Werkzeuge zum Auffinden und Behandeln verborgener Tumoren
Krebsärzte verlassen sich zunehmend auf minimalinvasive Verfahren, bei denen dünne Schläuche durch Blutgefäße oder Körperhöhlen geführt werden, um schwer zugängliche Tumoren zu erreichen. Die heutigen Instrumente tun sich jedoch oft schwer mit präziser Steuerung, klarer Abgrenzung der Tumorränder und der gezielten Behandlung ohne Schaden am gesunden Gewebe. Diese Studie stellt einen neuen Typ eines winzigen, magnetisch gesteuerten Katheters vor, der komplexe Anatomie durchfahren, die chemische Signatur des Tumors in Echtzeit erfassen und fokussierte Therapie genau dort liefern kann, wo sie gebraucht wird — mit dem Ziel, die Krebsbehandlung genauer und gleichzeitig schonender für den restlichen Körper zu machen.
Warum Tumorränder so schwer zu sehen sind
Die Standard-Krebsbehandlung stützt sich nach wie vor stark auf Biopsien, bildgebende Verfahren, Operationen, Chemotherapie und Strahlentherapie. Obwohl lebensrettend, haben diese Ansätze blinde Flecken. Eine einzelne Biopsieprobe kann Teile eines fleckigen, unregelmäßigen Tumors übersehen, und die lange Wartezeit zwischen Entnahme und Auswertung kann entscheidende Entscheidungen verzögern. Chirurgen sehen oft nicht die echte Grenze zwischen Krebs- und Normalgewebe, was das Risiko erhöht, verstreute Krebszellen zurückzulassen. Systemische Chemotherapie und Strahlung dagegen behandeln den ganzen Körper und verursachen Nebenwirkungen, weil sie kranke Zellen nicht leicht von gesunden unterscheiden können. Die Autoren argumentieren, dass ein Werkzeug nötig ist, das sich wendig im Körper bewegt, Tumorchemie vor Ort kartiert und Therapie nur dort konzentriert, wo sie wirklich erforderlich ist.
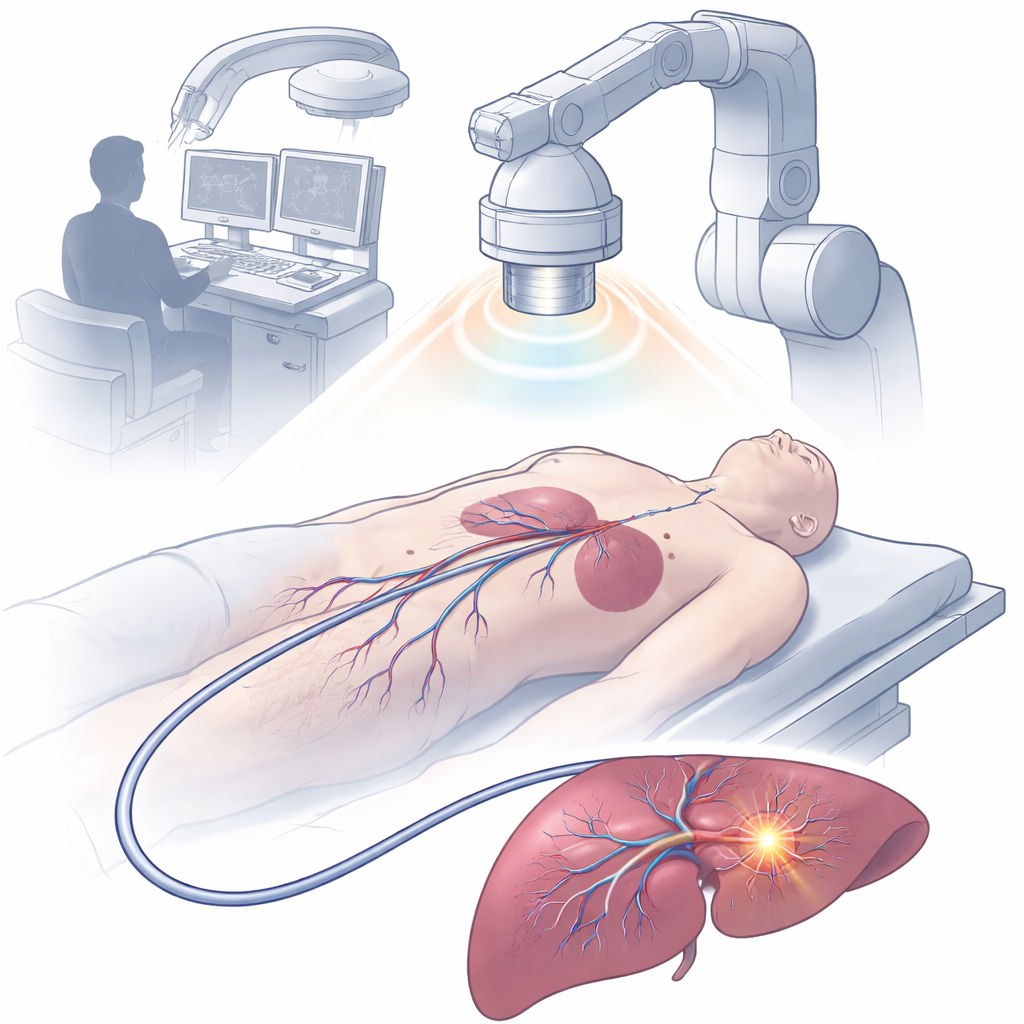
Ein winziger, magnetisch geführter Katheter voller Funktionen
Das Team entwickelte ein 2,5 Millimeter breites Gerät, genannt magnetisch angetriebener multifunktionaler optoelektronischer Katheter, kurz MDMOC. Mittels fortschrittlichem 3D-Multi-Achsen-Druck bauten sie eine flexible Schaftstruktur, die flüssigmetallgefüllte Kanäle für elektrische Leitung, eine Lichtfaser zur Lichtabgabe, Hohlwege für Medikamentengaben und ringförmige Magnete zur Steuerung und Röntgensichtbarkeit enthält. Die Spitze des Katheters ist mit einem kleinen Polymerkopf verschlossen, der von diamantförmigen Poren durchzogen ist, sodass lokale Flüssigkeiten an geschützten Messelektroden vorbeiströmen können. Eine dünne Hydrogelbeschichtung außen macht die Katheteroberfläche glatt, reduziert die Reibung zum Gewebe und erleichtert das sichere Gleiten durch Blutgefäße und Organe. Trotz seiner geringen Größe lässt sich der MDMOC per externem Magnetfeld ferngelenkt biegen und zielen, sodass er scharfe Kurven und komplexe vaskuläre Verzweigungen passieren kann.
Die chemische Signatur des Tumors in Echtzeit lesen
Was diesen Katheter besonders macht, sind seine eingebetteten „chemischen Augen“. Vier miniaturisierte elektrochemische Sensoren an der Spitze messen kontinuierlich Schlüsselmarker, die sich zwischen Tumoren und gesundem Gewebe unterscheiden: Säuregrad (pH), Wasserstoffperoxid, Kaliumionen und Glutathion, ein Molekül, das mit zellulärem Stress und Abwehr zusammenhängt. In Laborversuchen zeigten alle Sensoren hohe Empfindlichkeit, Selektivität und Stabilität, selbst in Gegenwart anderer üblicher Körperchemikalien. In Versuchen an Kaninchen mit Lebertumoren wurde der Katheter magnetisch durch eine kleine Bauchöffnung zu verdächtigen Läsionsstellen geführt. Durch Probenahmen an mehreren Punkten erstellte das Team detaillierte Chemiekarten, die scharfe Gradienten an der Tumor-Normal-Grenze offenbarten. Die Kombination der Daten aller vier Sensoren zu einer einzigen „Fusion“-Karte verbesserte die Randdetektion bis auf etwa submillimeter Genauigkeit und stimmte gut mit Ultraschallaufnahmen und gewebsdiagnostischen Goldstandards überein.
Von der Kartierung zur zielgerichteten Behandlung
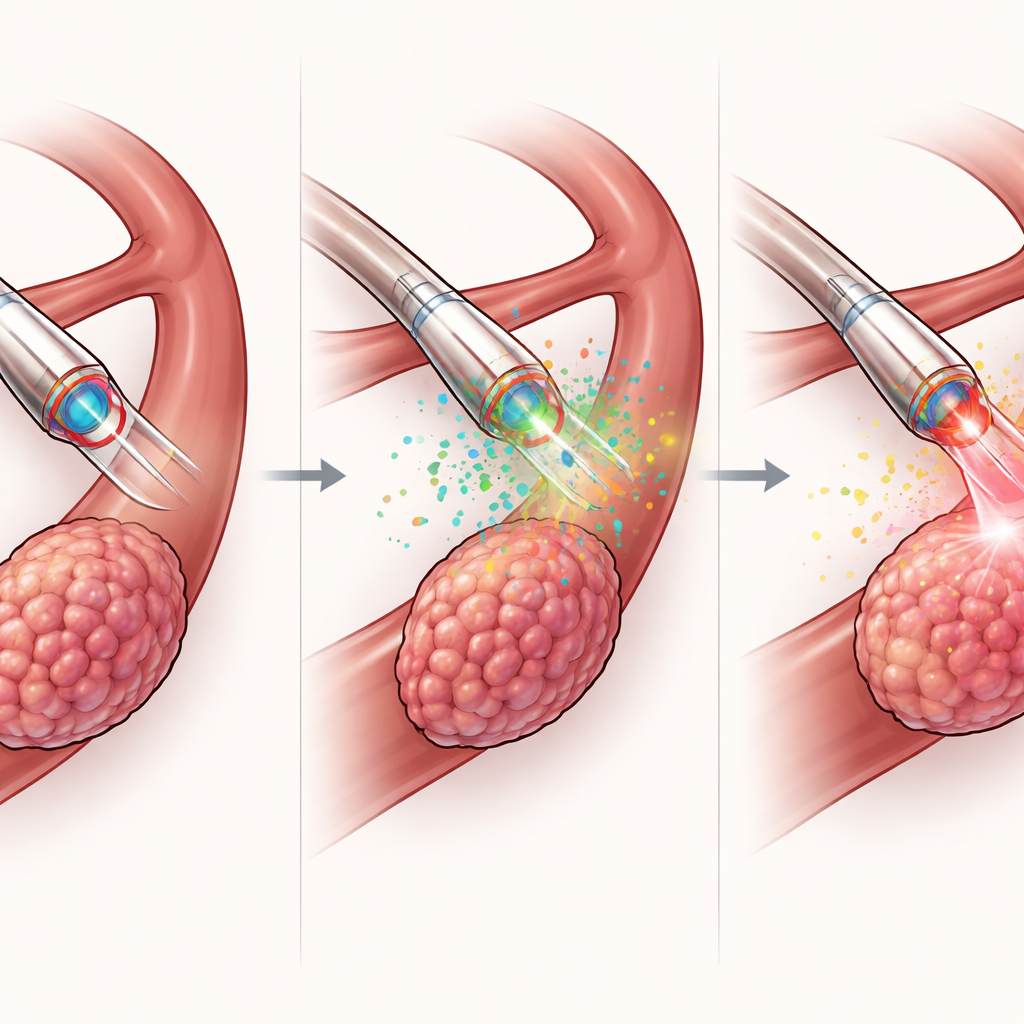
Über die Diagnose hinaus ist der MDMOC so ausgelegt, dass er auch therapeutisch wirkt. Über seinen internen Kanal liefert er eine konzentrierte Dosis eines lichtaktivierbaren Wirkstoffs direkt in den Tumor und verwendet dabei wesentlich weniger Wirkstoff als systemische Wege. Die Lichtfaser strahlt anschließend rotes Licht aus, um eine photodynamische Therapie auszulösen: Der Wirkstoff erzeugt reaktive Sauerstoffspezies, die in der Nähe liegende Krebszellen abtöten. In Mausmodellen von Leberkrebs führte dieser lokalisierte Ansatz zu stärkerer Tumorverkleinerung, kleineren Endtumorvolumina und mehr Tumorzellsterben als eine vergleichbare Behandlung durch die Haut oder Licht allein ohne Wirkstoff, und das alles ohne auffälligen Gewichtsverlust oder Schäden an wichtigen Organen. Wichtig ist, dass derselbe Katheter, der die Therapie steuert, auch die Tumorchemie vor und während der Behandlung misst und so eine schnelle „Erfassen–Entscheiden–Behandeln“-Schleife in Minuten statt Tagen ermöglicht.
Test des Geräts in größeren, realistischeren Körpern
Um zu prüfen, wie gut sich diese Technologie in die klinische Praxis übertragen lässt, testeten die Forscher eine längere Version des Katheters an Schweinen, deren Blutgefäße und Organe denen des Menschen näher kommen. Unter Röntgenbildgebung und magnetischer Steuerung navigierte der MDMOC von großen Venen in enge Abzweigungen der Leber- und Nierenvenen und meisterte scharfe Wendungen, die herkömmliche Katheter herausfordern würden. Er konnte Kontrastmittel präzise in diese Abzweigungen abgeben, ohne zu lecken, und unter laparoskopischer Kontrolle punktierte er spezifische Stellen auf der Leberoberfläche und der Blasenwand, um in situ zu messen und simulierte Behandlungen durchzuführen. Selbst bei Organbewegungen durch das schlagende Herz blieb der magnetisch geführte Katheter an den Zielstellen stabil, was sein Potenzial für reale, bildgestützte Eingriffe unterstreicht.
Was das für die künftige Krebsversorgung bedeuten könnte
Im Kern weist diese Arbeit auf eine neue Klasse intelligenter, magnetisch steuerbarer Katheter hin, die Navigation, Chemiekartierung und fokussierte Therapie in einem schlanken Instrument vereinen. Indem sie die chemische Landschaft des Tumors in Echtzeit lesen und diese Informationen nutzen, um Medikamente und Licht genau dorthin zu lenken, wo sie am effektivsten sind, könnte der MDMOC Chirurgen helfen, Tumorränder präziser zu definieren, gesundes Gewebe zu schonen und Nebenwirkungen am ganzen Körper zu verringern. Zwar sind vor dem Einsatz am Menschen weitere Studien nötig — insbesondere um die Bandbreite detektierbarer Biomarker zu erweitern und das System für spezifische Krebsarten anzupassen — doch das Konzept gewährt einen Ausblick auf minimalinvasive Krebstherapien, die nicht nur bild-, sondern auch chemiegesteuert sind.
Zitation: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
Schlüsselwörter: magnetisch geführter Katheter, Tumormikroumgebung, minimalinvasive Krebstherapie, Echtzeit-Biosensorik, photodynamische Therapie