Clear Sky Science · es
Catéter optoelectrónico multifuncional impulsado por imanes para el mapeo químico in vivo y terapia tumoral guiada con precisión
Herramientas más inteligentes para localizar y tratar tumores ocultos
Los oncólogos confían cada vez más en procedimientos mínimamente invasivos, introduciendo tubos delgados por vasos sanguíneos o cavidades corporales para alcanzar tumores de difícil acceso. Sin embargo, las herramientas actuales a menudo tienen dificultades para maniobrar con precisión, ver con claridad los bordes tumorales y aplicar tratamientos sin dañar el tejido sano. Esta investigación presenta un nuevo tipo de catéter diminuto guiado magnéticamente, diseñado para navegar por anatomías complejas, detectar en tiempo real la huella química del tumor y administrar terapia focalizada justo donde se necesita—con el objetivo de hacer el tratamiento del cáncer más preciso y menos agresivo para el resto del cuerpo.
Por qué es tan difícil ver los bordes del tumor
El cuidado estándar del cáncer sigue dependiendo en gran medida de biopsias, exploraciones, cirugía, quimioterapia y radiación. Aunque salvan vidas, estos enfoques tienen puntos ciegos. Una sola muestra de biopsia puede pasar por alto partes de un tumor parcheado e irregular, y la larga espera entre la toma de muestras y el tratamiento puede retrasar decisiones críticas. Los cirujanos a menudo no pueden ver la verdadera frontera entre el cáncer y el tejido normal, lo que eleva el riesgo de dejar células tumorales residuales. La quimioterapia y la radiación sistémicas, por su parte, exponen todo el cuerpo al tratamiento, provocando efectos secundarios porque no distinguen con facilidad entre células enfermas y sanas. Los autores sostienen que se necesita una herramienta capaz de moverse con agilidad dentro del cuerpo, mapear la química tumoral in situ y concentrar la terapia únicamente donde realmente se requiere.
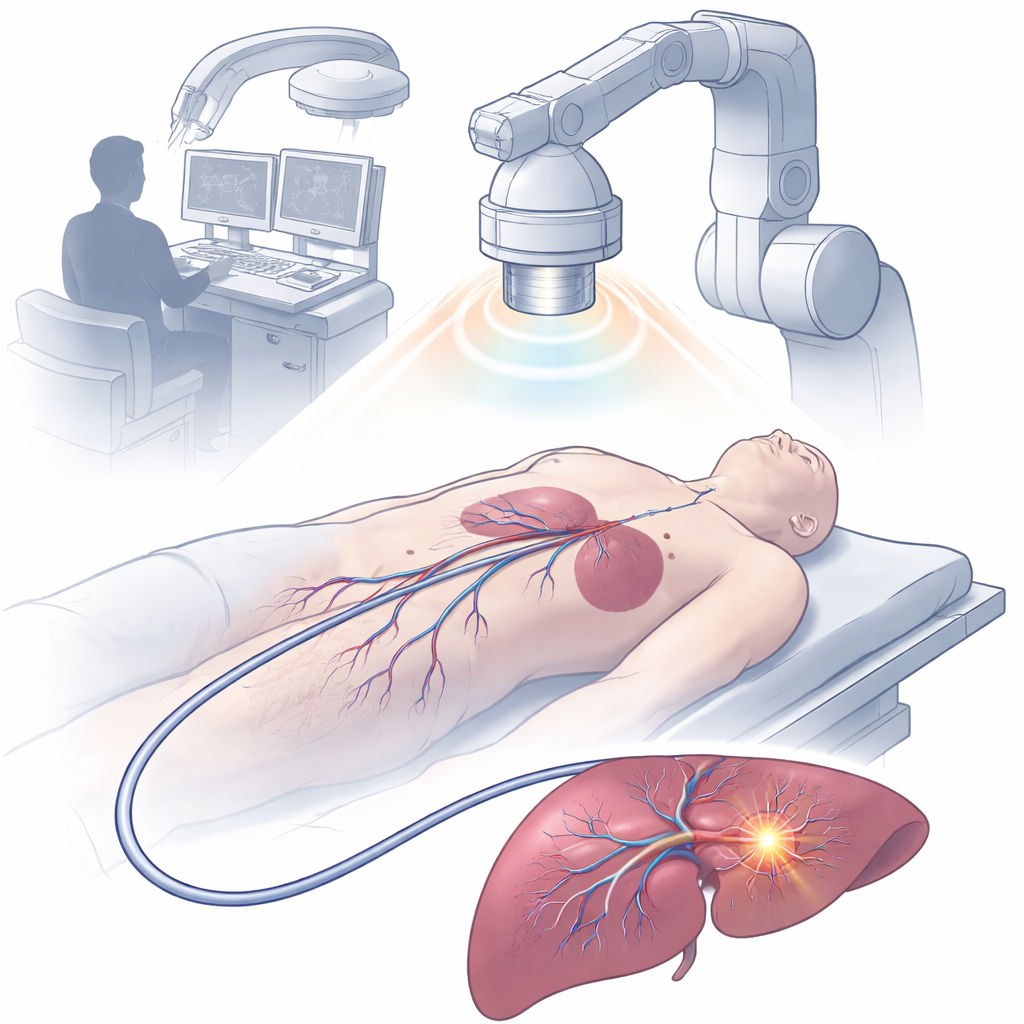
Un catéter diminuto guiado por imanes y lleno de funciones
El equipo construyó un dispositivo de 2,5 milímetros de diámetro llamado catéter optoelectrónico multifuncional impulsado por imanes, o MDMOC. Mediante impresión 3D multi-eje avanzada, ensamblaron un eje flexible que contiene canales de metal líquido para conducción eléctrica, una fibra óptica para la entrega de luz, conductos huecos para fármacos y anillos magnéticos para maniobra y visibilidad en rayos X. La punta del catéter está rematada con una pequeña cabeza polimérica perforada por poros en forma de diamante que permiten que los fluidos locales fluyan junto a electrodos de detección protegidos. Un recubrimiento delgado de hidrogel en el exterior hace la superficie resbaladiza, disminuyendo la fricción con los tejidos y ayudando a que se desplace con seguridad por vasos y órganos. A pesar de su pequeño tamaño, el MDMOC puede curvarse y apuntarse de forma remota mediante un campo magnético externo, permitiéndole sortear giros cerrados y ramas vasculares complejas.
Leer la firma química del tumor en tiempo real
Lo que distingue a este catéter son sus “ojos químicos” integrados. Cuatro sensores electroquímicos en miniatura en la punta miden continuamente marcadores clave que difieren entre tumores y tejidos sanos: acidez (pH), peróxido de hidrógeno, iones potasio y glutatión, una molécula vinculada al estrés y la defensa celular. En pruebas de laboratorio, cada sensor mostró alta sensibilidad, selectividad y estabilidad, incluso en presencia de otros químicos corporales comunes. En conejos con tumores hepáticos, el catéter se guió magnéticamente a través de una pequeña abertura abdominal hasta sitios de lesión sospechados. Al muestrear múltiples puntos, el equipo produjo mapas químicos detallados que revelaron gradientes pronunciados donde el tumor se encontraba con el tejido normal. La combinación de los datos de los cuatro sensores en un mapa de “fusión” mejoró la detección de límites hasta escalas submilimétricas aproximadas y coincidió bien con ecografías y la patología tisular, considerado el estándar de referencia.
Del mapeo al tratamiento dirigido
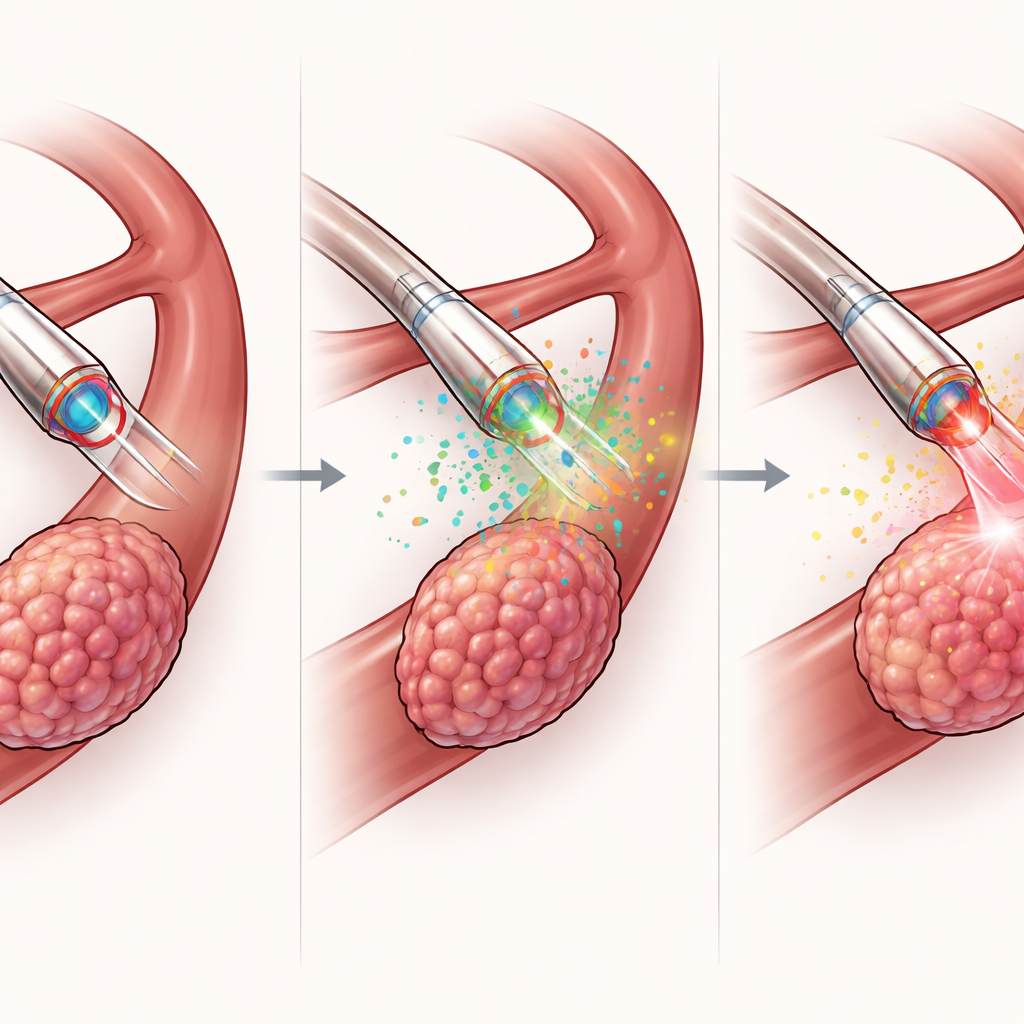
Más allá del diagnóstico, el MDMOC está diseñado para actuar. A través de su canal interno, administra una dosis concentrada de un fármaco activado por luz directamente en el tumor, usando mucho menos medicamento que las vías sistémicas. La fibra óptica luego emite luz roja para activar la terapia fotodinámica, haciendo que el fármaco genere especies reactivas de oxígeno que destruyen las células cancerosas cercanas. En modelos murinos de cáncer de hígado, este enfoque localizado produjo una mayor reducción tumoral, volúmenes tumorales finales menores y más muerte celular tumoral que un tratamiento comparable administrado a través de la piel o solo la luz sin fármaco, todo ello sin pérdida de peso apreciable ni daño a órganos principales. Importante: el mismo catéter que guía la terapia también mide la química tumoral antes y durante el tratamiento, permitiendo un ciclo rápido de “detectar–decidir–tratar” en minutos en lugar de días.
Probar el dispositivo en cuerpos más grandes y realistas
Para explorar cómo podría traducirse esta tecnología a la práctica clínica, los investigadores probaron una versión más larga del catéter en cerdos, cuyos vasos sanguíneos y órganos se asemejan más a los humanos. Bajo imágenes de rayos X y control magnético, el MDMOC navegó desde venas principales hacia ramas estrechas de las venas hepáticas y renales, tomando giros cerrados que desafiarían a los catéteres convencionales. Pudo administrar agentes de contraste con precisión en estas ramas sin fugas, y bajo guía laparoscópica perforó puntos específicos en la superficie hepática y la pared de la vejiga para realizar detección in situ y simulación de tratamiento. Incluso con el movimiento orgánico por el latido cardíaco, el catéter guiado magnéticamente se mantuvo estable en los sitios objetivo, subrayando su potencial para procedimientos guiados por imagen en el mundo real.
Qué podría significar esto para la atención del cáncer en el futuro
En esencia, este trabajo apunta a una nueva clase de catéteres inteligentes controlados magnéticamente que combinan navegación, mapeo químico y terapia focalizada en una sola y fina herramienta. Al leer el paisaje químico del tumor al vuelo y usar esa información para dirigir fármacos y luz exactamente donde son más eficaces, el MDMOC podría ayudar a los cirujanos a definir los márgenes tumorales con mayor precisión, preservar tejido sano y reducir efectos secundarios sistémicos. Aunque se necesitan más estudios antes del uso humano, en particular para ampliar el rango de biomarcadores detectables y adaptar el sistema a cánceres específicos, el concepto ofrece una visión de tratamientos mínimamente invasivos que no solo se guían por imágenes, sino por la propia química del tumor.
Cita: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
Palabras clave: catéter guiado magnéticamente, microambiente tumoral, terapia contra el cáncer mínimamente invasiva, biosensado en tiempo real, terapia fotodinámica