Clear Sky Science · ru
Магнитно управляемый многофункциональный оптоэлектронный катетер для in vivo химического картирования и точно направленной терапии опухолей
Более умные инструменты для поиска и лечения скрытых опухолей
Онкологи всё чаще полагаются на минимально инвазивные вмешательства, проводя тонкие трубки через сосуды или полости тела, чтобы добраться до труднодоступных опухолей. Однако современные инструменты нередко испытывают трудности с точным маневрированием, чётким определением краёв опухоли и доставкой лечения без вреда здоровой ткани. В этом исследовании предложен новый тип миниатюрного магнитно управляемого катетера, способного проходить сложную анатомию, в реальном времени выявлять химический след опухоли и доставлять сфокусированную терапию прямо в нужное место — цель состоит в том, чтобы сделать лечение рака более точным и щадящим для организма.
Почему так трудно увидеть границы опухоли
Стандартная онкологическая практика по-прежнему во многом опирается на биопсии, сканирование, хирургические вмешательства, химиотерапию и радиацию. Хоть эти подходы и спасают жизни, у них есть слепые зоны. Одна биопсийная проба может пропустить участки пятнистой, неправильной по форме опухоли, а длительная пауза между забором материала и лечением способна отсрочить важные решения. Хирурги часто не видят истинной границы между раковой и нормальной тканью, что повышает риск оставления отдельных раковых клеток. Системная химиотерапия и радиация, в свою очередь, воздействуют на весь организм, вызывая побочные эффекты, поскольку им трудно различить больные и здоровые клетки. Авторы утверждают, что необходим инструмент, который мог бы подвижно перемещаться внутри тела, картировать химию опухоли на месте и фокусировать терапию только там, где это действительно нужно.
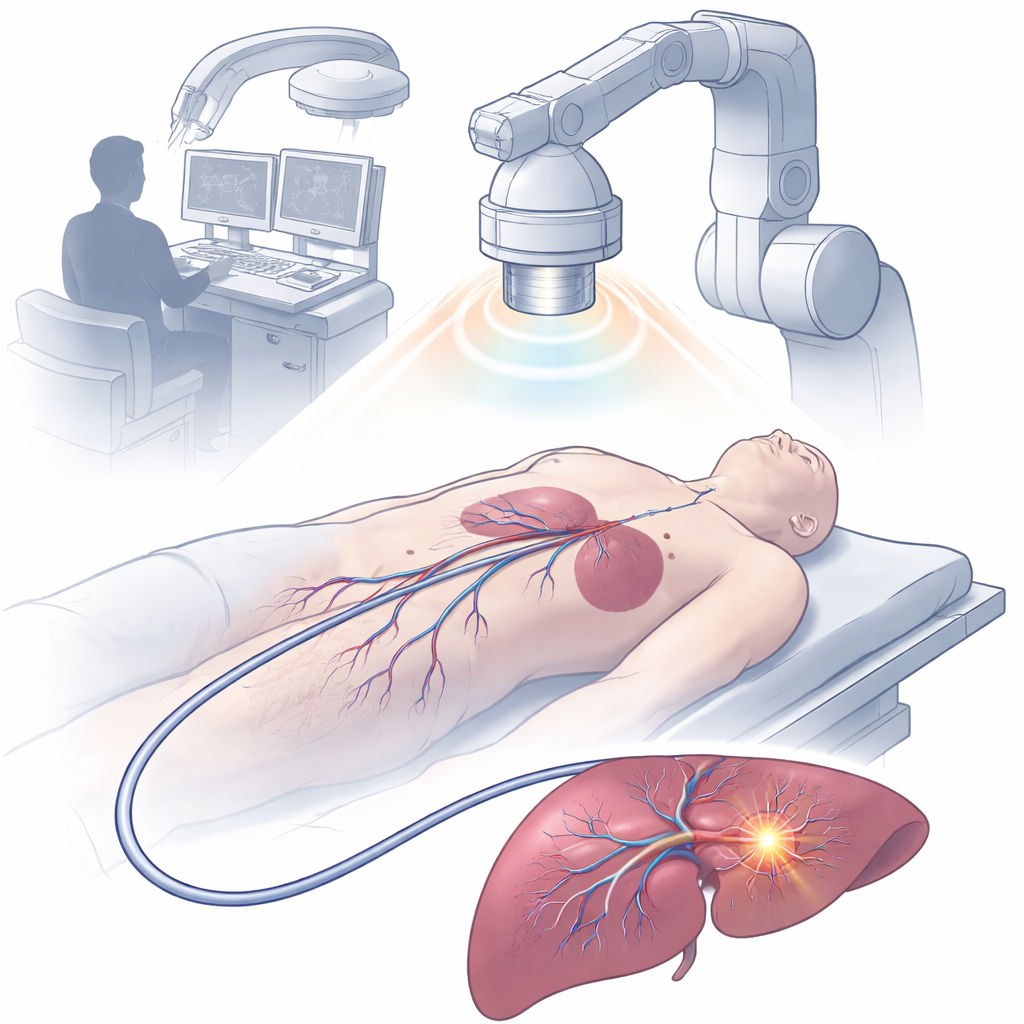
Миниатюрный магнитно управляемый катетер, насыщенный функциями
Команда создала устройство диаметром 2,5 миллиметра, названное магнитно управляемым многофункциональным оптоэлектронным катетером (MDMOC). С помощью передовой 3D многоосевой печати они собрали гибкий стержень, содержащий каналы с жидким металлом для электропроводки, оптическое волокно для подачи света, полые тракты для лекарств и кольцевые магниты для управления и видимости на рентгене. Наконечник катетера закрыт небольшим полимерным головным элементом с ромбовидными порами, через которые местные жидкости проходят мимо защищённых сенсорных электродов. Тонкое гидрогелевое покрытие снаружи делает поверхность катетера скользкой, снижая трение с тканями и помогая безопасно перемещаться по сосудам и органам. Несмотря на маленький размер, MDMOC можно дистанционно изгибать и наводить внешним магнитным полем, что позволяет ему огибать резкие повороты и ветвления сосудов.
Чтение химического «подписи» опухоли в реальном времени
Что отличает этот катетер, так это встроенные «химические глаза». Четыре миниатюрных электрохимических датчика на кончике непрерывно измеряют ключевые маркеры, отличающие опухоль от здоровых тканей: кислотность (pH), перекись водорода, ионы калия и глутатион — молекулу, связанную с клеточным стрессом и защитой. В лабораторных испытаниях каждый сенсор продемонстрировал высокую чувствительность, селективность и стабильность даже в присутствии других распространённых биохимических веществ. При использовании на кроликах с опухолями печени катетер магнитно направляли через небольшое брюшинное отверстие к предполагаемым очагам. При взятии проб в нескольких точках команда получила детализированные химические карты, выявившие резкие градиенты на стыке опухоли и нормальной ткани. Объединение данных всех четырёх сенсоров в единое «сливное» отображение улучшало обнаружение границы примерно до субмиллиметровых масштабов и хорошо согласовывалось с ультразвуковыми снимками и золотым стандартом тканевой патологии.
От картирования к таргетированной терапии
Помимо диагностики, MDMOC задуман как рабочий инструмент. По внутреннему каналу он доставляет концентрированную дозу светочувствительного препарата прямо в опухоль, используя значительно меньше лекарства, чем при системном введении. Оптическое волокно затем подаёт красный свет, инициируя фотодинамическую терапию: препарат генерирует активные формы кислорода, уничтожающие близлежащие раковые клетки. В мышиных моделях рака печени такой локализованный подход приводил к более выраженному сокращению опухоли, меньшим конечным объёмам и большему числу погибших раковых клеток по сравнению с сопоставимым лечением через кожу или только светом без препарата — и всё это без заметной потери веса или повреждения основных органов. Важно, что тот же катетер, который направляет терапию, также измеряет химию опухоли до и во время лечения, обеспечивая быстрый цикл «обнаружить—принять решение—лечить» за считанные минуты вместо дней.
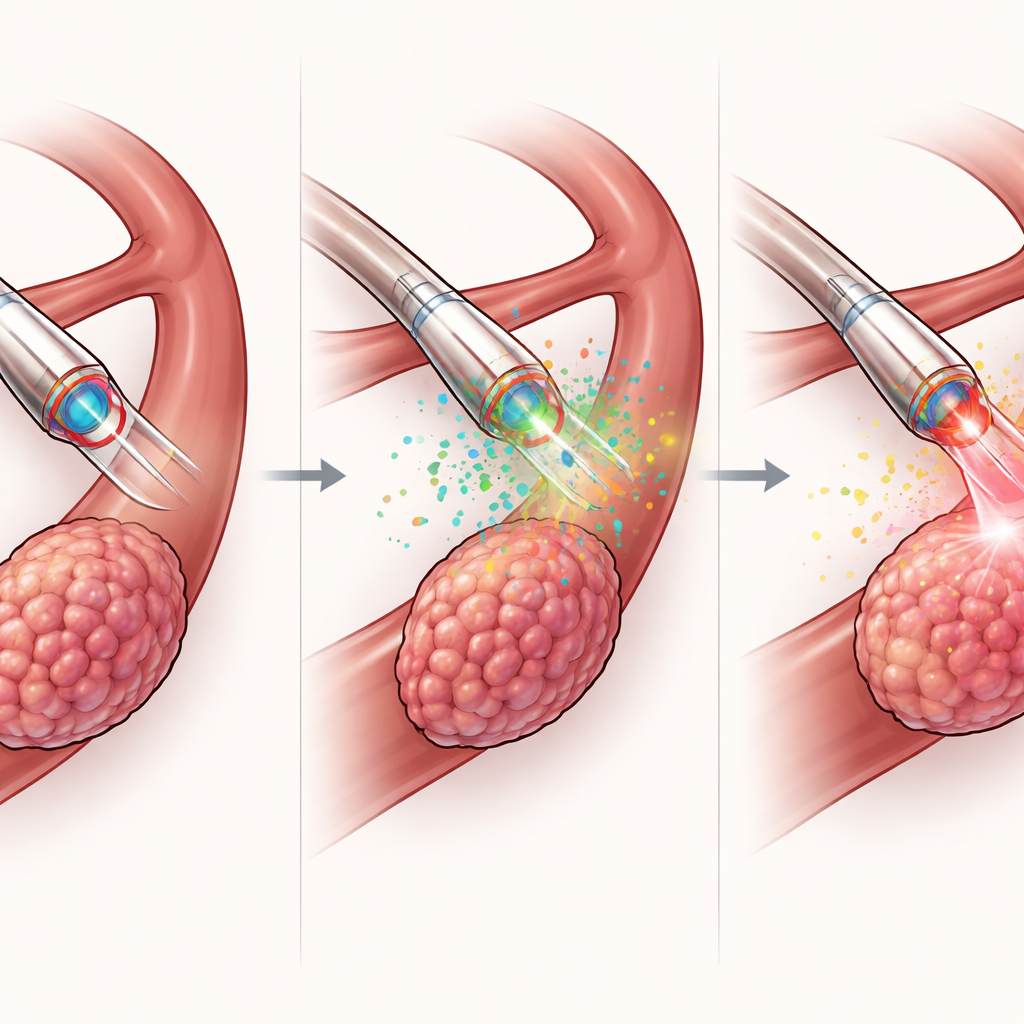
Испытания устройства в более крупных, реалистичных телах
Чтобы оценить возможную клиническую применимость, исследователи испытали удлинённую версию катетера на свиньях, сосуды и органы которых ближе по размерам к человеческим. Под рентгеновским контролем и магнитным управлением MDMOC прошёл от крупных вен в узкие ветви печёночных и почечных вен, совершая резкие повороты, которые стали бы проблемой для обычных катетеров. Он мог точно доставлять контрастные вещества в эти ветви без утечек, а под лапароскопическим контролем прокалывал выбранные участки на поверхности печени и стенке мочевого пузыря для in situ сенсинга и моделируемого лечения. Даже при движении органов из‑за сердечных сокращений магнитно управляемый катетер сохранял стабильность в целевых точках, что подчёркивает его потенциал для реальных процедур с визуальным наведением.
Что это может значить для будущей онкологической помощи
По сути, эта работа показывает путь к новому классу умных, магнитно управляемых катетеров, которые объединяют навигацию, химическое картирование и сфокусированную терапию в одном тонком инструменте. Считывая химический ландшафт опухоли на ходу и используя эти данные для точной доставки лекарств и света именно туда, где они наиболее эффективны, MDMOC может помочь хирургам точнее определять границы опухоли, щадить здоровые ткани и снижать системные побочные эффекты. Хотя перед применением у людей потребуются дополнительные исследования — в частности расширение набора детектируемых биомаркеров и адаптация системы под конкретные типы рака — концепция даёт представление о минимально инвазивных методах лечения, которые ориентируются не только на изображения, но и на саму химию опухоли.
Цитирование: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
Ключевые слова: магнитно управляемый катетер, микроокружение опухоли, малотравматичная противоопухолевая терапия, биосенсинг в реальном времени, фотодинамическая терапия