Clear Sky Science · nl
Magnetisch aangedreven multifunctionele opto-elektronische katheter voor in vivo chemische mapping en nauwkeurig geleide tumortherapie
Slimmere instrumenten om verborgen tumoren te vinden en te behandelen
Kankerdocenten vertrouwen steeds vaker op minimaal invasieve procedures, waarbij dunne buisjes door bloedvaten of lichaamsholtes worden geleid om moeilijk bereikbare tumoren te bereiken. De huidige instrumenten hebben echter vaak moeite met nauwkeurige besturing, het scherp in beeld brengen van tumorranden en het toedienen van behandeling zonder gezond weefsel te beschadigen. Dit onderzoek introduceert een nieuw type klein, magnetisch geleide katheter die is ontworpen om complexe anatomie te navigeren, het chemische profiel van de tumor in realtime te meten en gerichte therapie precies daar toe te dienen waar het nodig is — met als doel kankerbehandeling zowel nauwkeuriger als vriendelijker voor de rest van het lichaam te maken.
Waarom tumorranden zo moeilijk te zien zijn
De standaard kankerzorg steunt nog steeds sterk op biopsieën, scans, chirurgie, chemotherapie en bestraling. Hoewel levensreddend, hebben deze benaderingen blinde vlekken. Een enkele biopsie kan delen van een ongelijkmatige, onregelmatige tumor missen en de lange wachttijd tussen monstername en behandeling kan cruciale beslissingen vertragen. Chirurgen kunnen vaak de werkelijke grens tussen kankercellen en normaal weefsel niet zien, wat het risico vergroot dat achtergebleven kankercellen blijven bestaan. Systemische chemotherapie en bestraling behandelen het hele lichaam en veroorzaken bijwerkingen omdat zij zieke cellen niet gemakkelijk kunnen onderscheiden van gezonde. De auteurs stellen dat er een hulpmiddel nodig is dat zich wendbaar binnen het lichaam kan bewegen, tumorchimie ter plekke kan in kaart brengen en therapie alleen daar concentreert waar dat echt nodig is.
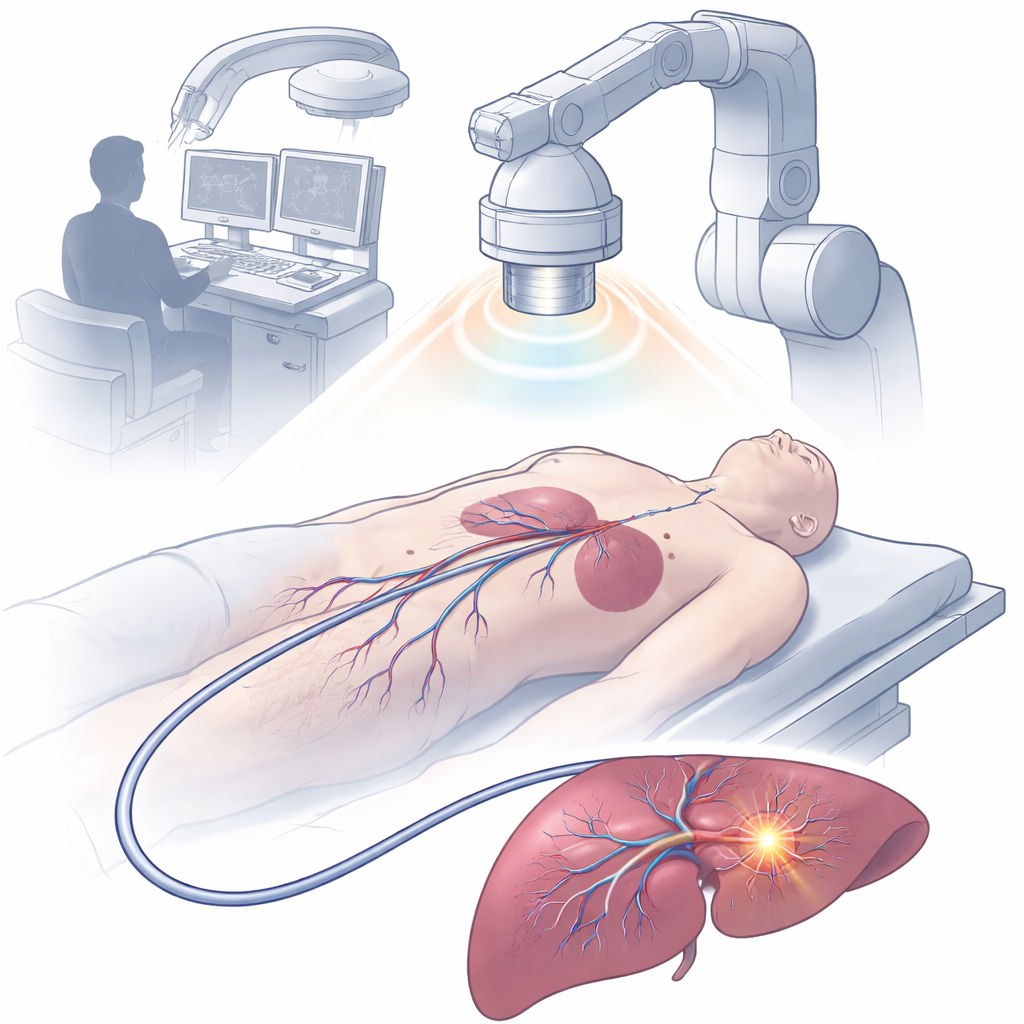
Een kleine magnetisch geleide katheter boordevol functies
Het team bouwde een apparaat met een diameter van 2,5 millimeter, een magnetisch aangedreven multifunctionele opto-elektronische katheter, of MDMOC. Met geavanceerd 3D multi-as printen monteerden ze een flexibele schacht die vloeibaar-metaalkanalen voor elektrische geleiding, een optische vezel voor lichtafgifte, holle kanalen voor medicatie en ringvormige magneten voor sturing en röntgendoorzicht bevat. De punt van de katheter is afgesloten met een klein polymeerhoofd met diamantvormige poriën die lokale vloeistoffen langs beschermde sensorelektroden laten stromen. Een dunne hydrogelcoating aan de buitenzijde maakt het katheteroppervlak glad, vermindert wrijving met weefsel en helpt veilig door bloedvaten en organen te bewegen. Ondanks zijn kleine formaat kan de MDMOC op afstand worden gebogen en gericht door een extern magnetisch veld, waardoor hij door scherpe bochten en complexe vaatvertakkingen kan kronkelen.
De chemische handtekening van de tumor in realtime lezen
Wat deze katheter onderscheidt, zijn de ingebouwde “chemische ogen.” Vier miniatuur elektrochemische sensoren aan de punt meten continu belangrijke merkers die verschillen tussen tumoren en gezond weefsel: zuurgraad (pH), waterstofperoxide, kaliumionen en glutathion, een molecule die verband houdt met cellulaire stress en verdediging. In laboratoriumtesten toonde elke sensor hoge gevoeligheid, selectiviteit en stabiliteit, zelfs in aanwezigheid van andere veelvoorkomende lichaamschemicals. Bij gebruik in konijnen met levertumoren werd de katheter magnetisch door een kleine buikopening naar vermoedelijke laesies geleid. Door op meerdere punten te bemonsteren produceerde het team gedetailleerde chemische kaarten die scherpe gradiënten onthulden waar tumor overging in normaal weefsel. Het combineren van gegevens van alle vier sensoren in één ‘fusie’-kaart verbeterde de grensdetectie tot ruwweg submillimetrische schaal en kwam goed overeen met echografiebeelden en de gouden standaard van weefselpathologie.
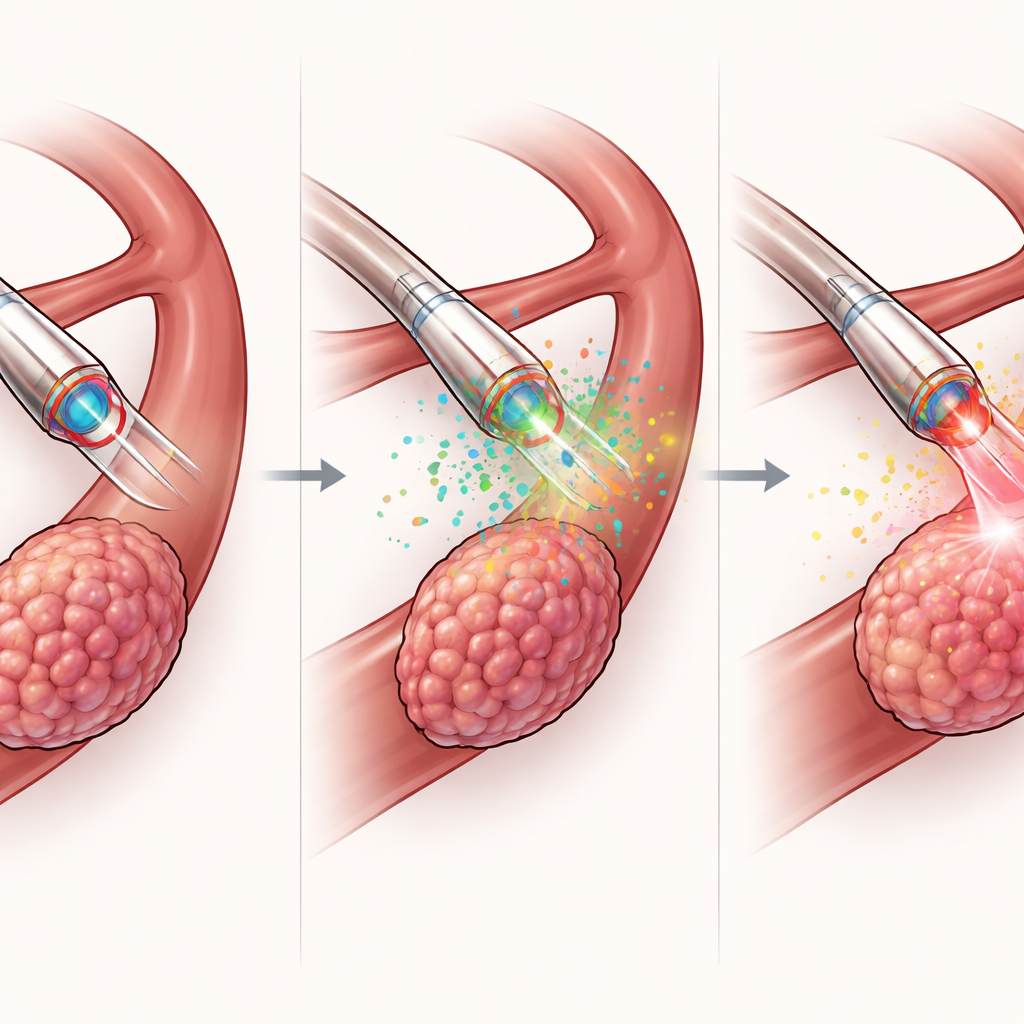
Van mapping naar gerichte behandeling
Buiten diagnose is de MDMOC ontworpen om te handelen. Via het interne kanaal levert hij een geconcentreerde dosis van een lichtactief geneesmiddel direct in de tumor, waarbij veel minder medicatie wordt gebruikt dan bij systemische toediening. De optische vezel zendt vervolgens rood licht om fotodynamische therapie te activeren, waardoor het geneesmiddel reactieve zuurstofsoorten genereert die nabije kankercellen doden. In muismodellen voor leverkanker leidde deze gelokaliseerde aanpak tot sterkere tumorkrimp, kleinere uiteindelijke tumorgroottes en meer kankerceldood dan een vergelijkbare behandeling via de huid of licht zonder medicatie, allemaal zonder merkbaar gewichtsverlies of schade aan belangrijke organen. Belangrijk is dat dezelfde katheter die de therapie geleidt ook de tumorchimie meet vóór en tijdens de behandeling, waardoor een snelle ‘voelen–beslissen–behandelen’ lus binnen minuten in plaats van dagen mogelijk is.
Het apparaat testen in grotere, realistischer lichamen
Om te onderzoeken hoe goed deze technologie naar klinische praktijk zou kunnen vertalen, testten de onderzoekers een langere versie van de katheter in varkens, waarvan de bloedvaten en organen meer op die van mensen lijken. Onder röntgenbeelden en magnetische besturing navigeerde de MDMOC van grote aders naar smalle takken van de hepaticale en renale aders en maakte scherpe bochten die conventionele katheters zouden uitdagen. Hij kon contrastmiddelen nauwkeurig in deze takken afleveren zonder lekkage, en onder laparoscopische begeleiding prikte hij specifieke plekken op het leveroppervlak en de blaaswand om in situ sensing en gesimuleerde behandeling uit te voeren. Zelfs met orgaanbeweging door een kloppend hart bleef de magnetisch geleide katheter stabiel op doelplaatsen, wat het potentieel voor realistische, beeldgegeleide procedures benadrukt.
Wat dit zou kunnen betekenen voor toekomstige kankerzorg
In wezen wijst dit werk op een nieuwe klasse van slimme, magnetisch bestuurbare katheters die navigatie, chemische mapping en gerichte therapie in één slank instrument combineren. Door het chemische landschap van de tumor ter plekke uit te lezen en die informatie te gebruiken om medicijnen en licht precies te sturen waar ze het meest effectief zijn, zou de MDMOC chirurgen kunnen helpen tumorranden nauwkeuriger af te bakenen, gezond weefsel te sparen en bijwerkingen door het hele lichaam te verminderen. Hoewel meer studies nodig zijn voordat menselijk gebruik mogelijk is—met name om het bereik van detecteerbare biomarkers te vergroten en het systeem af te stemmen op specifieke kankers—biedt het concept een blik op minimaal invasieve kankerbehandelingen die niet alleen door beelden worden geleid, maar door de chemie van de tumor zelf.
Bronvermelding: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
Trefwoorden: magnetisch geleide katheter, tumormicro‑omgeving, minimaal invasieve kankertherapie, realtime biosensing, fotodynamische therapie