Clear Sky Science · ar
قسطرة بصرية-إلكترونية متعددة الوظائف مدفوعة بالمغناطيس للرسم الكيميائي داخل الجسم والعلاج الموجه بدقة للأورام
أدوات أذكى لاكتشاف وعلاج الأورام الخفيّة
يعتمد أطباء السرطان بشكل متزايد على إجراءات قليلة التوغل، حيث يمررون أنابيب رفيعة عبر الأوعية الدموية أو تجاويف الجسم للوصول إلى أورام يصعب الوصول إليها. ومع ذلك، غالبًا ما تكافح الأدوات الحالية للتوجيه الدقيق، ورؤية حواف الورم بوضوح، وتقديم العلاج دون إلحاق ضرر بالأنسجة السليمة. يقدم هذا البحث نوعًا جديدًا من القسطرات الصغيرة الموجهة مغناطيسيًا المصممة للتنقل عبر تشريح معقّد، واستشعار البصمة الكيميائية للورم في الوقت الحقيقي، وتوصيل العلاج المركز مباشرة إلى المكان المطلوب — بهدف جعل علاج السرطان أكثر دقة وألطف على بقية الجسم.
لماذا من الصعب رؤية حواف الورم
لا تزال رعاية السرطان القياسية تعتمد بشكل كبير على الخزعات، والفحوصات، والجراحة، والعلاج الكيميائي، والإشعاع. وعلى الرغم من أنها منقذة للحياة، فهذه الطرق لديها نقاط عمياء. قد تفوت عينة خزعة واحدة أجزاء من ورم غير متجانس وغير منتظم، ويمكن أن يؤخر الفاصل الطويل بين أخذ العينة والعلاج اتخاذ قرارات حرجة. غالبًا لا يستطيع الجراحون رؤية الحدود الحقيقية بين الخلايا السرطانية والنسيج الطبيعي، مما يزيد من خطر ترك خلايا سرطانية متفرقة. أما العلاج الكيميائي والإشعاع الجهازيان فيعالجان الجسم بأكمله، مما يؤدي إلى آثار جانبية لأنهما لا يميزان بسهولة بين الخلايا المريضة والسليمة. يجادل المؤلفون بأن المطلوب هو أداة يمكنها التحرك بخفة داخل الجسم، ورسم خريطة كيميائية للورم على الفور، وتركيز العلاج فقط حيثما يكون مطلوبًا فعلاً.
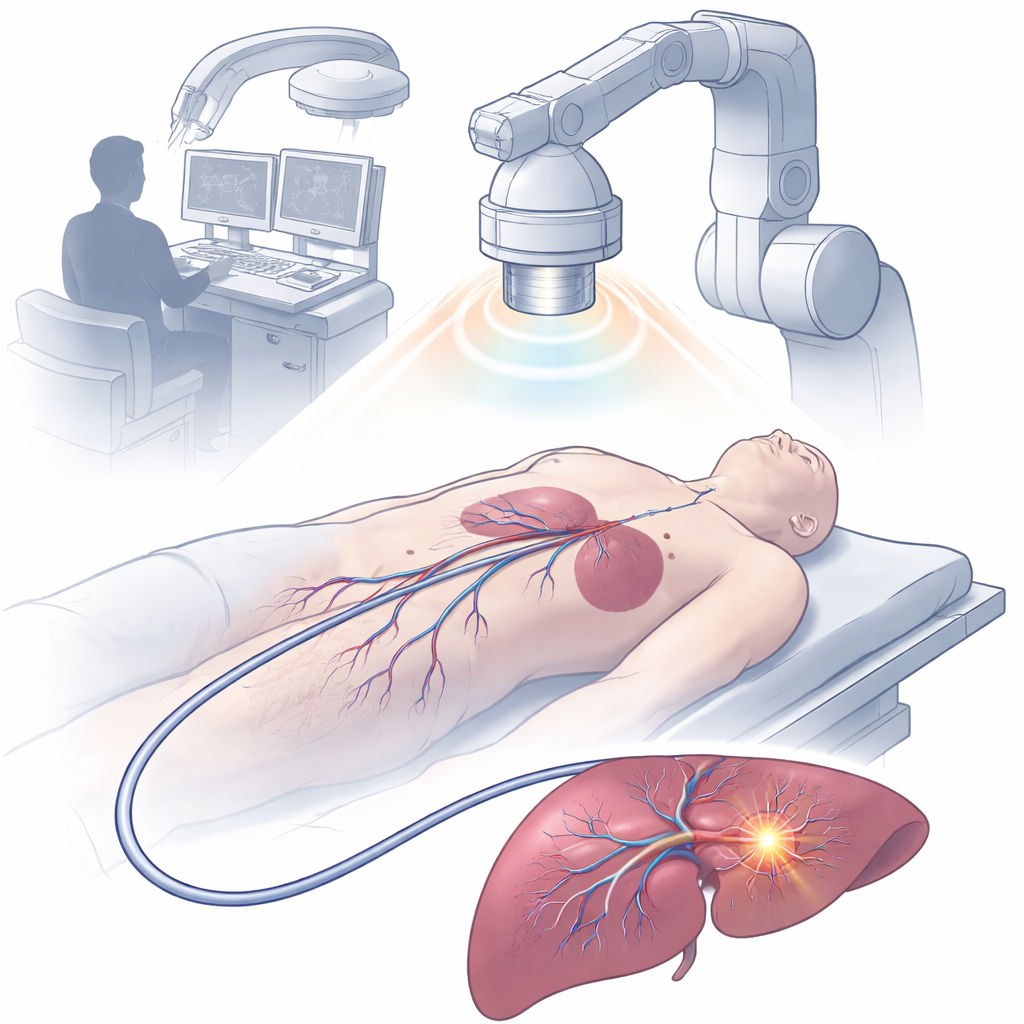
قسطرة صغيرة موجهة بالمغناطيس ومليئة بالوظائف
بنَت الفريق جهازًا بعرض 2.5 مليمتر أطلقوا عليه اسم القسطرة البصرية-الإلكترونية متعددة الوظائف المدفوعة مغناطيسيًا، أو MDMOC. باستخدام الطباعة ثلاثية الأبعاد المتقدمة متعددة المحاور، جمعوا عمودًا مرنًا يحتوي على قنوات من معدن سائل للتوصيل الكهربائي، وخلية ضوئية لنقل الضوء، ومسارات جوفاء للأدوية، ومغانط حلقيّة للتوجيه والرؤية بالأشعة السينية. يُغطى طرف القسطرة برأس بوليمري صغير مخترق بمسام على شكل ماسة تسمح لتدفقات السوائل المحلية بالمرور بجوار أقطاب استشعار محمية. طلاء هيدروجيل رقيق خارجيًا يجعل سطح القسطرة أملسًا، مما يقلل الاحتكاك مع الأنسجة ويساعدها على التنقل بأمان عبر الأوعية الدموية والأعضاء. وعلى الرغم من صغر حجمه، يمكن ثني MDMOC وتوجيهه عن بُعد بواسطة مجال مغناطيسي خارجي، مما يتيح له الانسياب عبر منحنيات حادة وتفرعات وعائية معقّدة.
قراءة البصمة الكيميائية للورم في الوقت الحقيقي
ما يميز هذه القسطرة هو "عيناها الكيميائيتان" المدمجتان. تقيس أربعة حساسات كيميائية كهربائية مصغرة عند الطرف باستمرار علامات رئيسية تختلف بين الأورام والأنسجة السليمة: الحموضة (الرقم الهيدروجيني)، وبيروكسيد الهيدروجين، وأيونات البوتاسيوم، والجلوتاثيون، وهو جزيء مرتبط بالإجهاد الخلوي والدفاع. في الاختبارات المخبرية أظهرت كل حسّاس حساسية وخصوصية واستقرارًا عاليًا، حتى بوجود مواد كيميائية جسمانية أخرى شائعة. عند استخدامها في أرانب مصابة بأورام كبدية، قُيِدت القسطرة مغناطيسيًا عبر فتحة بطنية صغيرة إلى مواقع الآفات المشتبه بها. من خلال أخذ عينات من نقاط متعددة، أنتج الفريق خرائط كيميائية مفصّلة كشفت عن تدرجات حادة حيث يلتقي الورم بالنسيج الطبيعي. أدى دمج بيانات الحساسات الأربعة في خريطة "اندماجية" واحدة إلى تحسين كشف الحدود إلى مقياس دون المليمتر تقريبًا، وتطابقت النتائج جيدًا مع صور الموجات فوق الصوتية وباثولوجيا الأنسجة المعيارية الذهبية.
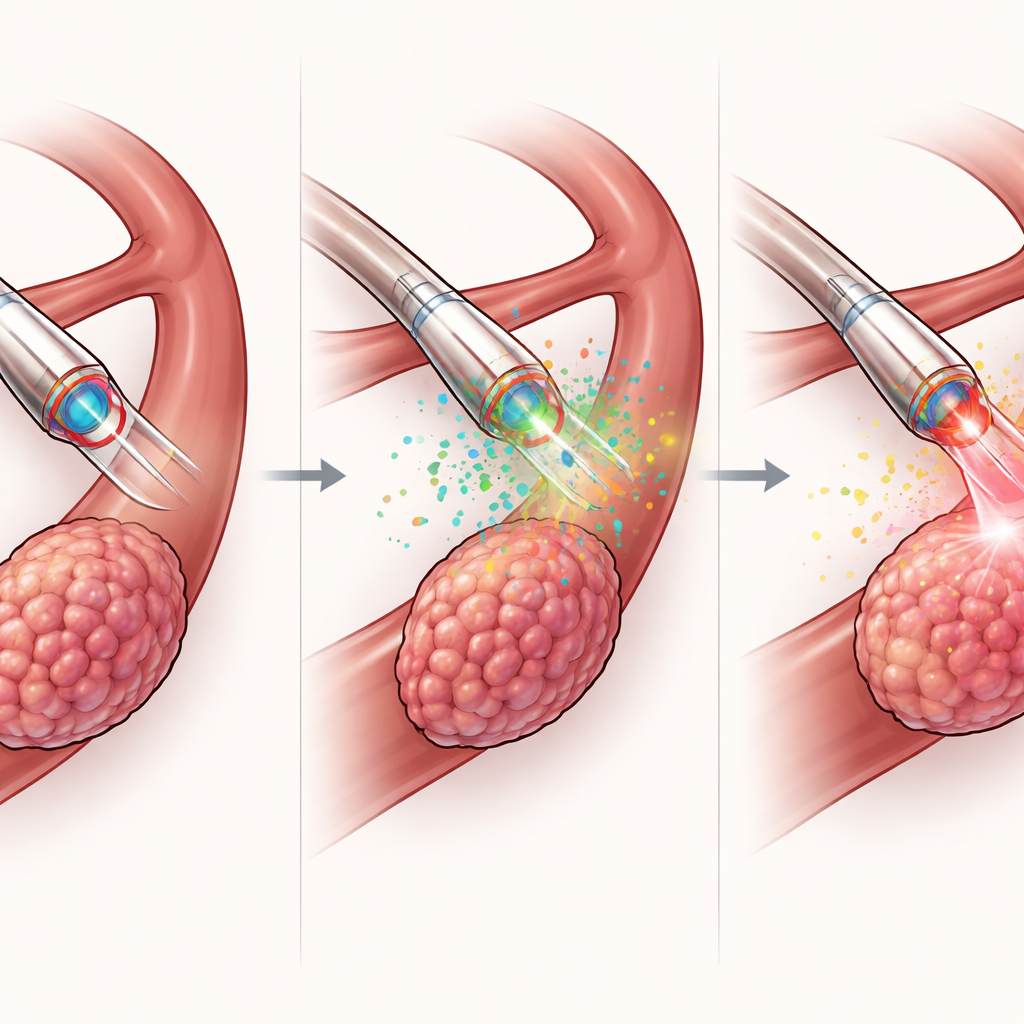
من التخطيط إلى العلاج الموجَّه
تتعدى وظيفة MDMOC التشخيص؛ فهي مصممة أيضًا للتنفيذ. عبر قناتها الداخلية، توصل جرعة مركزة من دواء مفعل بالضوء مباشرة إلى الورم، مستخدمةً كمية أقل بكثير من الدواء مقارنة بالطرق الجهازية. ثم يُنقل الضوء الأحمر عبر الليف البصري لتحفيز العلاج الضوئي الديناميكي، ما يجعل الدواء يولد أنواعًا تفاعلية من الأكسجين تقتل الخلايا السرطانية المجاورة. في نماذج فأرية لسرطان الكبد، أدى هذا النهج الموضعي إلى تقلص أقوى للأورام، وحجوم نهائية أصغر للأورام، ومعدلات موت خلوي سرطاني أعلى مقارنةً بعلاج مماثل واصل عبر الجلد أو بالضوء وحده دون دواء، وكل ذلك دون فقدان وزن ملحوظ أو تلف في الأعضاء الرئيسية. والأهم أن نفس القسطرة التي توجه العلاج تقيس أيضًا كيمياء الورم قبل وأثناء العلاج، مما يتيح حلقة سريعة من "استشعار–قرار–علاج" خلال دقائق بدلًا من أيام.
اختبار الجهاز في أجسام أكبر وأكثر واقعية
لاستكشاف مدى قابلية تكيّف هذه التقنية مع الممارسة السريرية، اختبر الباحثون نسخة أطول من القسطرة في خنازير، التي تشبه أوعيتها الدموية وأعضاؤها الإنسان أكثر. تحت تصوير بالأشعة السينية وتحكم مغناطيسي، تنقلت MDMOC من الأوردة الرئيسية إلى تفرعات ضيقة في الأوردة الكبدية والكلوية، آخذة منحنيات حادة كانت لتشكل تحديًا للقسطرات التقليدية. استطاعت توصيل عوامل تباين بدقة إلى هذه التفرعات دون تسرب، وتحت توجيه منظاري اخترقت نقاطًا محددة على سطح الكبد وجدار المثانة لتنفيذ استشعار موضعي وعلاج محاكٍ. حتى مع حركة الأعضاء الناتجة عن نبض القلب، ظلت القسطرة الموجهة مغناطيسيًا مستقرة عند المواقع المستهدفة، مما يبرز وعدها للإجراءات الموجهة بالصور في العالم الواقعي.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
بالمجمل، يشير هذا العمل إلى فئة جديدة من القسطرات الذكية الموجهة مغناطيسيًا التي تجمع بين الملاحة، والرسم الكيميائي، والعلاج المركز في أداة رفيعة واحدة. من خلال قراءة المشهد الكيميائي للورم فورًا واستخدام تلك المعلومات لتوجيه الأدوية والضوء إلى حيث تكون أكثر فعالية، قد تساعد MDMOC الجراحين على تحديد هوامش الورم بدقة أكبر، وحماية الأنسجة السليمة، وتقليل الآثار الجانبية المنتشرة بالجسم. وبينما يلزم إجراء المزيد من الدراسات قبل الاستخدام البشري، خاصة لتوسيع نطاق العلامات الحيوية القابلة للكشف وتكييف النظام ليناسب أنواعًا محددة من السرطان، يقدم المفهوم لمحة عن علاجات سرطانية قليلة التوغل لا تُوجَّه بالصور فحسب — بل بت chemistry� )"كيمياء" الورم نفسها).
الاستشهاد: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
الكلمات المفتاحية: قسطرة موجهة مغناطيسياً, البيئة الدقيقة للورم, علاج السرطان بتداخل طفيف, الاستشعار الحيوي في الوقت الحقيقي, العلاج الضوئي الديناميكي