Clear Sky Science · fr
Cathéter optoélectronique multifonction piloté par aimant pour cartographie chimique in vivo et thérapie tumorale guidée avec précision
Des outils plus intelligents pour localiser et traiter les tumeurs cachées
Les oncologues recourent de plus en plus à des procédures peu invasives, faisant passer de fins tubes dans les vaisseaux sanguins ou les cavités corporelles pour atteindre des tumeurs difficiles d’accès. Pourtant, les instruments actuels peinent souvent à se diriger avec précision, à délimiter clairement les bords tumoraux et à délivrer un traitement sans endommager les tissus sains. Cette recherche présente un nouveau type de minuscule cathéter piloté magnétiquement, conçu pour naviguer dans une anatomie complexe, détecter en temps réel l’empreinte chimique de la tumeur et administrer une thérapie ciblée exactement là où elle est nécessaire — visant à rendre le traitement du cancer à la fois plus précis et moins agressif pour le reste du corps.
Pourquoi les bords tumoraux sont si difficiles à voir
Les soins contre le cancer s’appuient encore largement sur les biopsies, les examens d’imagerie, la chirurgie, la chimiothérapie et la radiothérapie. Bien qu’ils sauvent des vies, ces approches présentent des angles morts. Un seul prélèvement peut manquer des portions d’une tumeur irrégulière et fragmentée, et le long délai entre l’échantillonnage et le traitement peut retarder des décisions cruciales. Les chirurgiens ne voient souvent pas la véritable frontière entre tissu cancéreux et tissu normal, ce qui augmente le risque de laisser des cellules cancéreuses résiduelles. La chimiothérapie systémique et la radiothérapie, quant à elles, exposent tout le corps au traitement et entraînent des effets secondaires parce qu’elles distinguent mal les cellules malades des cellules saines. Les auteurs soutiennent qu’il faut un outil capable de se déplacer avec agilité à l’intérieur du corps, de cartographier la chimie tumorale sur place et de concentrer la thérapie uniquement là où elle est réellement nécessaire.
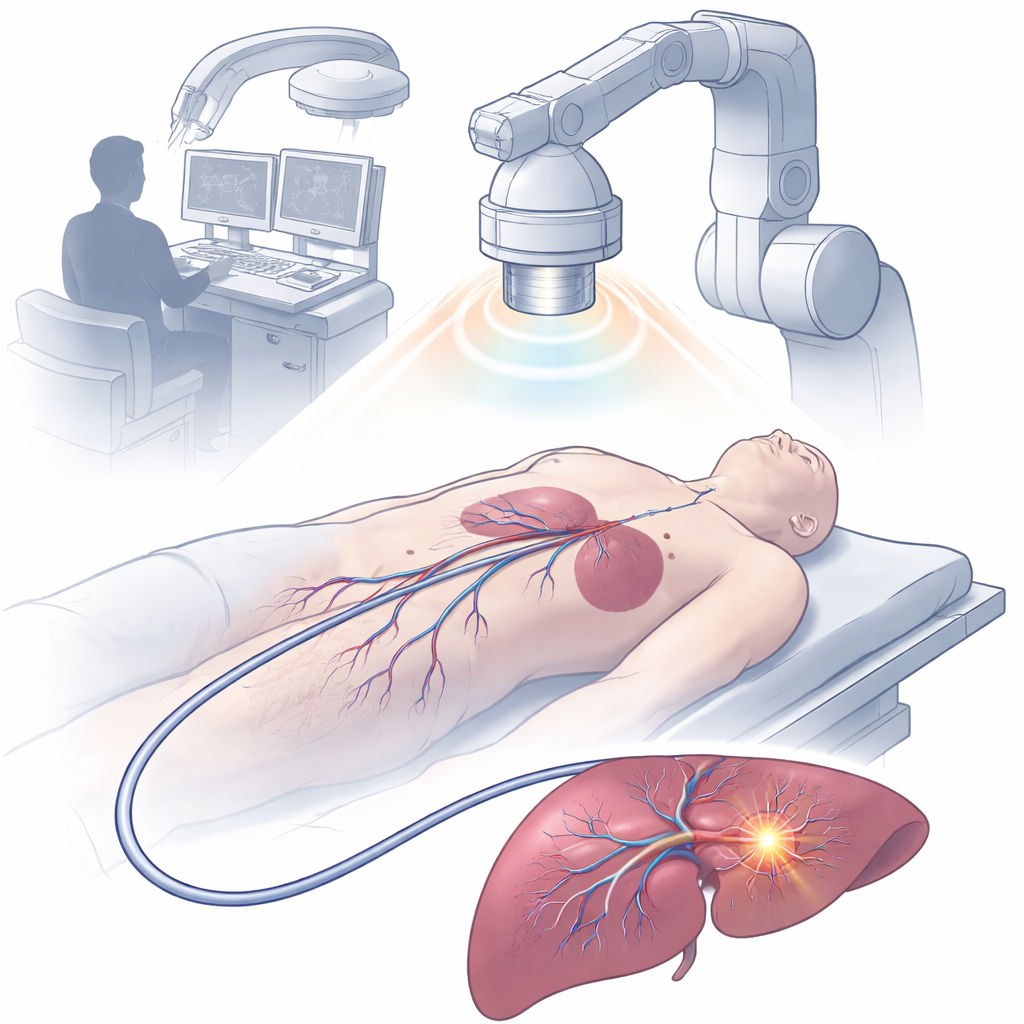
Un minuscule cathéter magnétique chargé de fonctions
L’équipe a conçu un dispositif de 2,5 millimètres de diamètre appelé cathéter optoélectronique multifonction piloté par aimant, ou MDMOC. Grâce à l’impression 3D multi-axes avancée, ils ont assemblé un arbre flexible contenant des canaux de métal liquide pour la conduction électrique, une fibre optique pour la délivrance de lumière, des conduits creux pour les médicaments et des anneaux magnétiques pour la direction et la visibilité aux rayons X. L’extrémité du cathéter est coiffée d’une petite tête en polymère percée de pores en forme de losange qui laissent les fluides locaux circuler autour des électrodes de détection protégées. Un fin revêtement en hydrogel rend la surface du cathéter glissante, réduisant les frottements avec les tissus et facilitant son déplacement en toute sécurité dans les vaisseaux sanguins et les organes. Malgré sa petite taille, le MDMOC peut être plié et orienté à distance par un champ magnétique externe, lui permettant de serpenter à travers des virages serrés et des branches vasculaires complexes.
Lire la signature chimique de la tumeur en temps réel
Ce qui distingue ce cathéter, ce sont ses « yeux chimiques » intégrés. Quatre capteurs électrochimiques miniatures à l’extrémité mesurent en continu des marqueurs clés qui diffèrent entre tumeurs et tissus sains : acidité (pH), peroxyde d’hydrogène, ions potassium et glutathion, une molécule liée au stress cellulaire et à la défense. En laboratoire, chaque capteur a montré une sensibilité, une sélectivité et une stabilité élevées, même en présence d’autres substances courantes de l’organisme. Utilisé chez des lapins porteuses de tumeurs hépatiques, le cathéter a été guidé magnétiquement à travers une petite ouverture abdominale vers des sites de lésions suspectées. En échantillonnant plusieurs points, l’équipe a produit des cartes chimiques détaillées révélant des gradients nets à la jonction entre tumeur et tissu normal. La fusion des données des quatre capteurs en une carte unique a amélioré la détection des marges jusqu’à des échelles submillimétriques environ, et s’est bien corrélée aux échographies et à l’histopathologie, référence standard.
De la cartographie au traitement ciblé
Au-delà du diagnostic, le MDMOC est conçu pour agir. Par son canal interne, il délivre une dose concentrée d’un médicament activable par la lumière directement dans la tumeur, en utilisant beaucoup moins de produit qu’une administration systémique. La fibre optique éclaire ensuite en rouge pour déclencher la thérapie photodynamique, entraînant la formation d’espèces réactives de l’oxygène qui détruisent les cellules cancéreuses environnantes. Dans des modèles murins de cancer du foie, cette approche localisée a entraîné une réduction tumorale plus marquée, des volumes tumoraux finaux plus petits et davantage de mort cellulaire tumorale que des traitements comparables administrés à travers la peau ou que la lumière seule sans médicament, le tout sans perte de poids notable ni atteinte des principaux organes. Fait important, le même cathéter qui guide la thérapie mesure aussi la chimie tumorale avant et pendant le traitement, permettant une boucle rapide « sentir–décider–traiter » en quelques minutes au lieu de plusieurs jours.
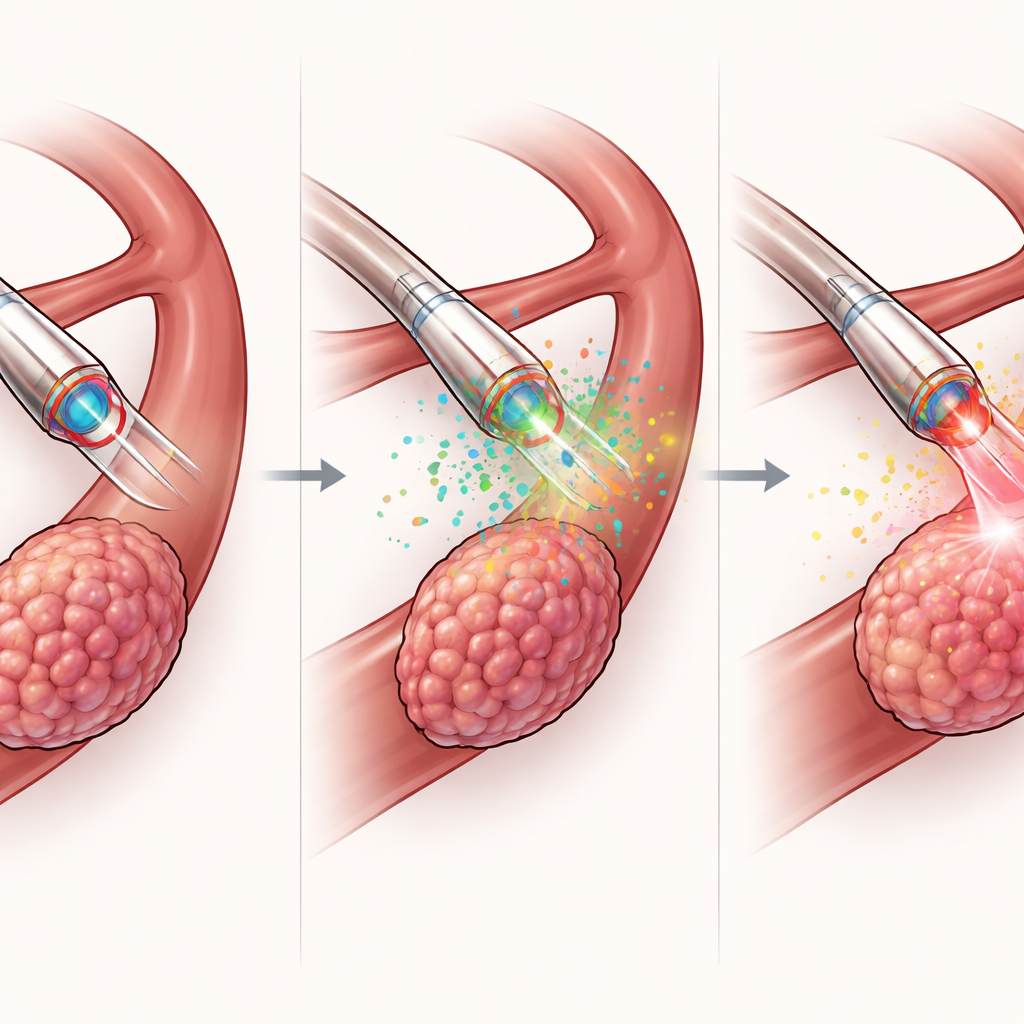
Tester l’appareil dans des corps plus grands et plus réalistes
Pour évaluer la transposabilité clinique potentielle, les chercheurs ont testé une version plus longue du cathéter chez des porcs, dont les vaisseaux sanguins et les organes ressemblent davantage à ceux des humains. Sous imagerie aux rayons X et contrôle magnétique, le MDMOC a navigué depuis les veines principales jusque dans de fines branches des veines hépatiques et rénales, prenant des virages serrés qui poseraient problème aux cathéters conventionnels. Il a pu délivrer des agents de contraste précisément dans ces branches sans fuite, et sous guidage laparoscopique il a perforé des points spécifiques sur la surface du foie et la paroi de la vessie pour réaliser des mesures in situ et des traitements simulés. Même avec le mouvement des organes lié aux battements cardiaques, le cathéter guidé magnétiquement est resté stable sur les sites cibles, soulignant son potentiel pour des procédures pratiques guidées par l’imagerie.
Ce que cela pourrait signifier pour les soins contre le cancer à venir
En substance, ce travail ouvre la voie à une nouvelle catégorie de cathéters intelligents pilotés magnétiquement qui combinent navigation, cartographie chimique et thérapie ciblée en un seul instrument mince. En lisant sur le vif le paysage chimique de la tumeur et en utilisant ces informations pour diriger médicaments et lumière exactement là où ils sont les plus efficaces, le MDMOC pourrait aider les chirurgiens à mieux définir les marges tumorales, épargner les tissus sains et réduire les effets secondaires systémiques. Bien que des études supplémentaires soient nécessaires avant une utilisation humaine — notamment pour élargir la gamme de biomarqueurs détectables et adapter le système à des cancers spécifiques — le concept offre un aperçu de traitements anticancéreux peu invasifs qui seraient guidés non seulement par l’imagerie, mais par la chimie même de la tumeur.
Citation: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
Mots-clés: cathéter guidé magnétiquement, microenvironnement tumoral, thérapie anticancéreuse peu invasive, biosurveillance en temps réel, thérapie photodynamique