Clear Sky Science · pl
Magnetycznie sterowany wielofunkcyjny światłowodowo-elektroniczny cewnik do in vivo mapowania chemicznego i precyzyjnie ukierunkowanej terapii nowotworowej
Mądrzejsze narzędzia do odnajdywania i leczenia ukrytych guzów
Onkolodzy coraz częściej polegają na procedurach minimalnie inwazyjnych, wprowadzając cienkie rurki przez naczynia krwionośne lub jamy ciała, by dotrzeć do trudno dostępnych guzów. Jednak współczesne narzędzia często mają problem z precyzyjnym prowadzeniem, wyraźnym uwidacznianiem brzegów guza i dostarczaniem terapii bez uszkodzenia zdrowych tkanek. Badanie to przedstawia nowy typ miniaturowego, magnetycznie sterowanego cewnika zaprojektowanego do poruszania się w skomplikowanej anatomii, wykrywania chemicznego „odcisku” guza w czasie rzeczywistym i dostarczania ukierunkowanej terapii dokładnie tam, gdzie jest potrzebna — z zamiarem zwiększenia precyzji leczenia i zmniejszenia obciążenia dla reszty organizmu.
Dlaczego granice guza są trudne do zauważenia
Standardowa opieka onkologiczna wciąż opiera się w dużej mierze na biopsjach, badaniach obrazowych, operacjach, chemioterapii i radioterapii. Choć ratują życie, metody te mają swoje luki. Pojedynczy pobrany materiał może pominąć fragmenty niejednorodnego, nieregularnego guza, a długi czas między pobraniem a leczeniem może opóźnić kluczowe decyzje. Chirurdzy często nie widzą rzeczywistej granicy między tkanką nowotworową a zdrową, co zwiększa ryzyko pozostawienia komórek nowotworowych. Z kolei terapia systemowa — chemioterapia i radioterapia — działa na cały organizm, wywołując skutki uboczne, bo trudno jej odróżnić chore komórki od zdrowych. Autorzy proponują, że potrzebne jest narzędzie zdolne poruszać się zwinie wewnątrz ciała, mapować chemię guza na miejscu i koncentrować terapię tylko tam, gdzie rzeczywiście jest konieczna.
Maleńki cewnik prowadzony magnesami, pełen funkcji
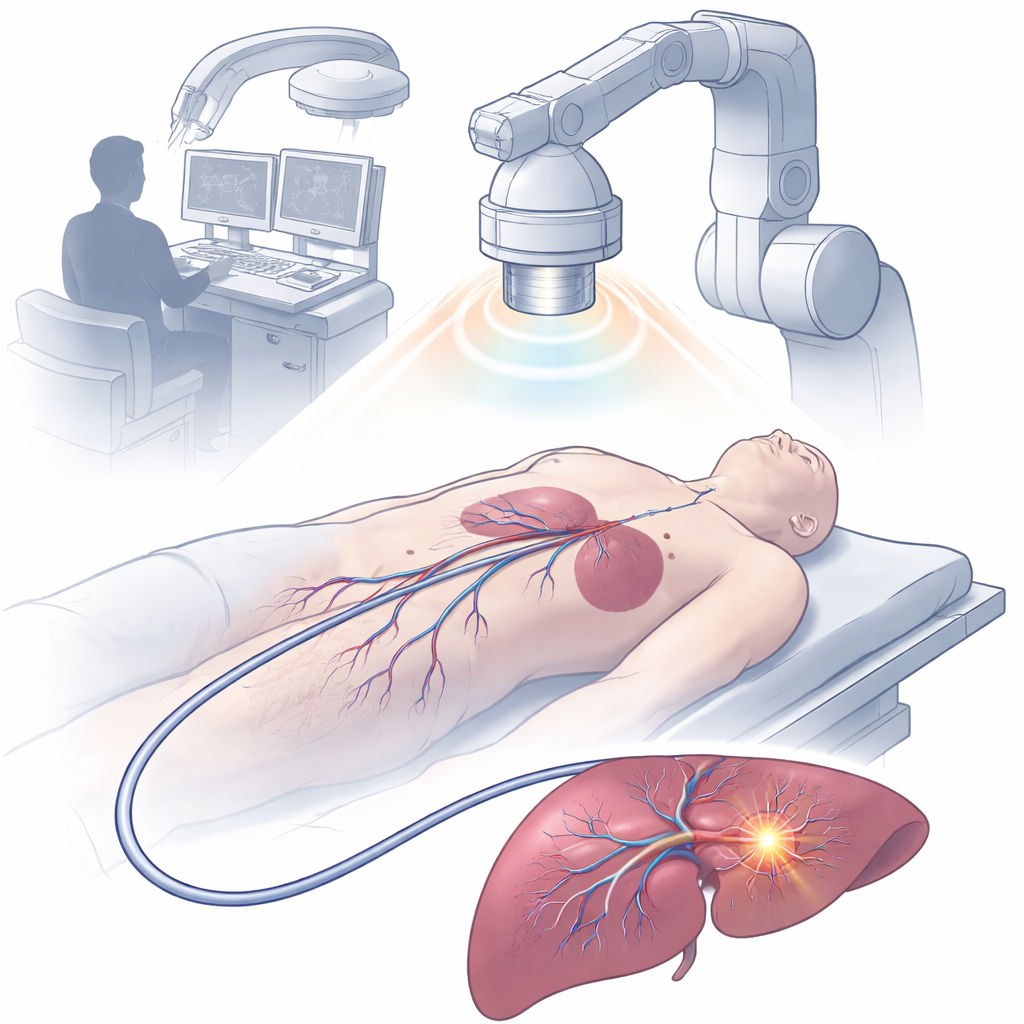
Zespół zbudował urządzenie o średnicy 2,5 milimetra, nazwane magnetycznie napędzanym wielofunkcyjnym światłowodowo-elektronicznym cewnikiem (MDMOC). Wykorzystując zaawansowane, wieloosiowe drukowanie 3D, skonstruowano elastyczny trzon zawierający kanały z ciekłym metalem do przewodzenia prądu, włókno optyczne do dostarczania światła, puste przewody do podawania leków oraz pierścieniowe magnesy do sterowania i widoczności w promieniach rentgena. Końcówka cewnika zakończona jest małą główką z polimeru, przebitą romboidalnymi porami, które pozwalają lokalnym płynom przepływać obok chronionych elektrod czujnikowych. Cienka powłoka hydrożelowa na zewnątrz obniża tarcie z tkankami i ułatwia bezpieczne przemieszczanie się przez naczynia i organy. Pomimo niewielkich rozmiarów, MDMOC można zdalnie wyginać i kierować dzięki zewnętrznemu polu magnetycznemu, co pozwala mu wypełzać przez ostre zakręty i skomplikowane rozgałęzienia naczyń.
Odczytywanie chemicznego podpisu guza w czasie rzeczywistym
To, co wyróżnia ten cewnik, to wbudowane „chemiczne oczy”. Cztery miniaturowe sensory elektrochemiczne w końcówce mierzą ciągle kluczowe markery odróżniające guzy od tkanek zdrowych: kwasowość (pH), nadtlenek wodoru, jony potasu i glutation — cząsteczkę związaną ze stresem komórkowym i mechanizmami obronnymi. W testach laboratoryjnych każdy sensor wykazywał wysoką czułość, selektywność i stabilność, nawet w obecności innych powszechnych związków biologicznych. W badaniach na królikach z guzami wątroby cewnik był magnetycznie prowadzony przez niewielkie cięcie w jamie brzusznej do podejrzanych miejsc zmian. Pobierając próbki w wielu punktach, zespół stworzył szczegółowe mapy chemiczne, które ujawniły ostre gradienty na granicy guza i tkanki normalnej. Połączenie danych ze wszystkich czterech sensorów w jedną mapę „fuzji” poprawiło wykrywanie granic do skali poniżej milimetra i dobrze korelowało z badaniem ultrasonograficznym oraz złotym standardem patologicznym tkanki.
Od mapowania do ukierunkowanego leczenia
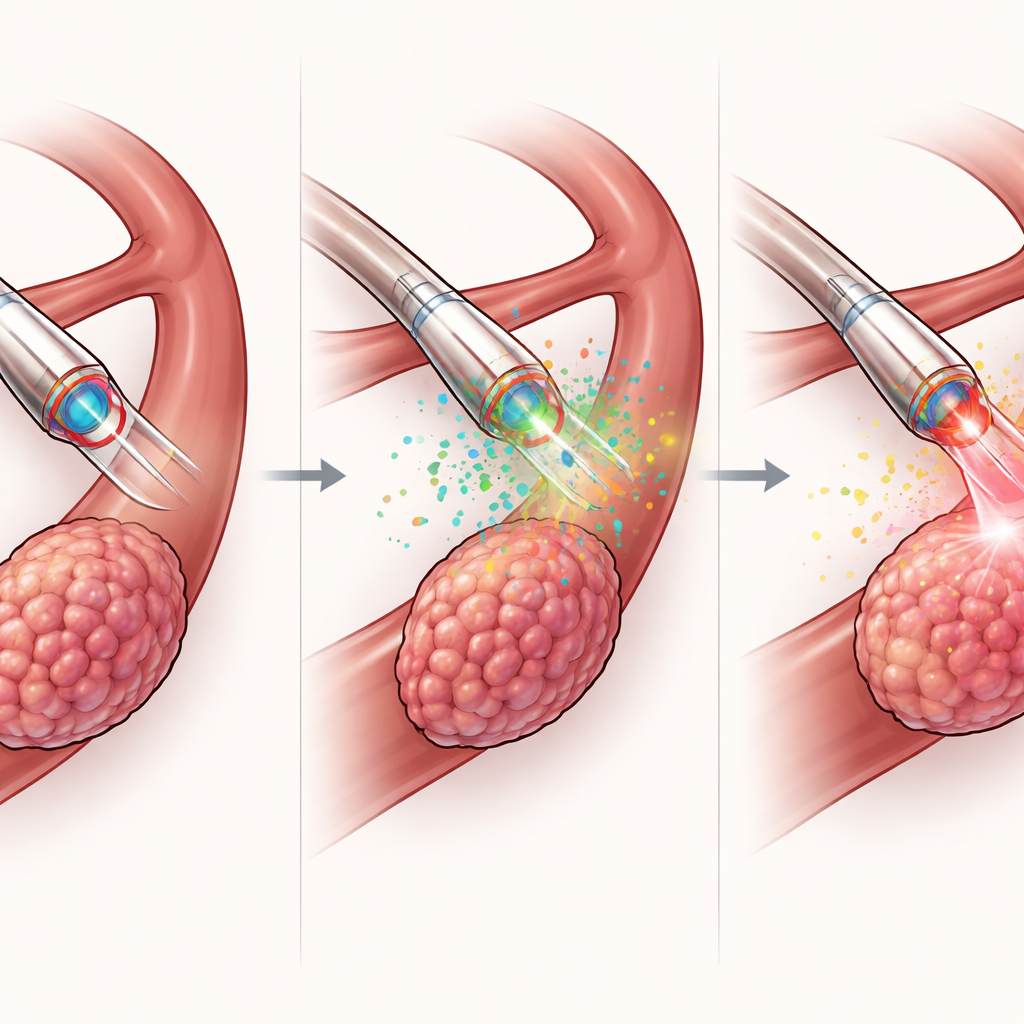
Ponad diagnostyką, MDMOC został zaprojektowany także jako narzędzie terapeutyczne. Przez wewnętrzny kanał dostarcza skoncentrowaną dawkę leku aktywowanego światłem bezpośrednio do guza, wykorzystując znacznie mniejsze ilości niż przy drogach systemowych. Następnie włókno optyczne emituje czerwone światło, uruchamiając terapię fotodynamiczną — lek generuje reaktywne formy tlenu, które zabijają pobliskie komórki nowotworowe. W modelach mysich raka wątroby takie lokalne podejście prowadziło do silniejszego kurczenia się guza, mniejszych końcowych objętości oraz większego odsetka obumarłych komórek nowotworowych niż porównywalne leczenie przezskórne lub samo oświetlenie bez leku, i to bez zauważalnej utraty masy ciała czy uszkodzeń głównych narządów. Co ważne, ten sam cewnik, który prowadzi terapię, jednocześnie mierzy chemię guza przed i w trakcie leczenia, umożliwiając szybkie cykle „wyczuj–zdecyduj–lecz” w ciągu minut zamiast dni.
Testy urządzenia w większych, bardziej realistycznych ciałach
Aby zbadać, jak technologia mogłaby przełożyć się na praktykę kliniczną, badacze przetestowali dłuższą wersję cewnika u świń, których naczynia i organy bardziej przypominają ludzkie. Pod kontrolą obrazowania rentgenowskiego i sterowania magnetycznego MDMOC nawigował z głównych żył do wąskich rozgałęzień żył wątrobowych i nerkowych, wykonując ostre zakręty, które stanowią wyzwanie dla konwencjonalnych cewników. Mógł precyzyjnie dostarczać środki kontrastowe do tych odgałęzień bez wycieku, a pod kontrolą laparoskopii nakłuwał wybrane miejsca na powierzchni wątroby i ścianie pęcherza, przeprowadzając pomiary in situ i symulowane leczenie. Nawet przy ruchu narządów spowodowanym biciem serca magnetycznie sterowany cewnik pozostawał stabilny w miejscach docelowych, co podkreśla jego potencjał do zabiegów obrazowych i prowadzonych w warunkach rzeczywistych.
Co to może oznaczać dla przyszłej opieki onkologicznej
W istocie praca ta wskazuje na nową klasę inteligentnych, magnetycznie kontrolowanych cewników łączących nawigację, mapowanie chemiczne i ukierunkowaną terapię w jednym, smukłym narzędziu. Czytając chemiczny krajobraz guza na bieżąco i wykorzystując te informacje do precyzyjnego dostarczania leków i światła tam, gdzie są najbardziej skuteczne, MDMOC mógłby pomóc chirurgom dokładniej definiować marginesy guza, oszczędzać tkanki zdrowe i ograniczać skutki uboczne dla całego organizmu. Choć potrzebne są dalsze badania przed zastosowaniem u ludzi — zwłaszcza w celu poszerzenia zakresu wykrywanych biomarkerów i dostosowania systemu do konkretnych rodzajów raka — koncepcja ta daje wyobrażenie minimalnie inwazyjnych terapii onkologicznych kierowanych nie tylko obrazem, lecz także własną chemią guza.
Cytowanie: Chen, F., Liu, X., Zhang, Y. et al. Magnetic-driven multifunctional optoelectronic catheter for in vivo chemical mapping and precisely guided-tumor therapy. Nat Commun 17, 3725 (2026). https://doi.org/10.1038/s41467-026-70529-6
Słowa kluczowe: cewnik prowadzony magnetycznie, mikrośrodowisko guza, minimalnie inwazyjna terapia nowotworowa, bioczujniki w czasie rzeczywistym, fotodynamiczna terapia