Clear Sky Science · zh
一种微生物群–IPA轴通过Hopx相关程序促进结肠炎中肠道干细胞介导的再生
友善肠道细菌如何帮助受损肠道愈合
数以百万计的炎性肠病患者长期承受慢性刺激和受损的肠道。当肠道内层屏障被破坏时,会出现疼痛和通透性增加,使微生物和食物颗粒进一步刺激机体。该研究揭示了某些有益肠道细菌及其代谢产物如何激活一组特殊的备用肠道干细胞,从而加速这一脆弱屏障的修复。理解微生物、饮食与干细胞之间的这种协同关系,指向了更温和的治疗策略,帮助肠道自我重建,而不是单纯依赖强力免疫抑制药物。
炎症肠道中缺失的帮手
研究人员首先比较了克罗恩病(一种炎性肠病)患者与健康志愿者的肠道微生物。他们发现一种在正常情况下常见的细菌Blautia coccoides在患者及多种结肠炎小鼠模型中显著减少。当他们有意将这种细菌补入小鼠肠道时,动物对化学诱导的肠道损伤表现出更强的抵抗力:结肠保持得更长、更不萎缩,显微镜下的组织损伤较轻,炎症信号也被抑制。这种保护作用在不同类型的肠道损伤(包括化学刺激和放射损伤)中均成立,表明该微生物广泛支持肠道抵御并从伤害中恢复的能力。
备用干细胞:肠道的应急小组
肠道内层通过位于微小隐窝(crypts)内的干细胞不断更新。最为人所知的干细胞高度活跃但易受损;在严重炎症下常被清除。研究团队表明,Blautia coccoides有助于另一类更具韧性的“储备”干细胞介入修复。在接受该细菌的小鼠中,储备干细胞相关基因在损伤后早期被激活,而在几天后对照动物大多失去这些细胞时,储备和活跃干细胞群都得以保存。追踪储备干细胞命运的实验显示,在该细菌的影响下,这些平静的细胞被唤醒、增殖,并分化为新的活跃干细胞,重建受损的隐窝。体外培养的人源与鼠源类肠道器官也证实,这一再生程序在人类组织中同样可行。
从饮食到微生物再到干细胞的化学链
接着,科学家们探究了肠道细菌如何发出如此精确的修复信号。他们发现,Blautia coccoides重塑肠细胞内的代谢,提升一种与能量代谢相关的小分子——β-羟基丁酸的产生。这种化合物并非由细菌自身直接合成,而是在宿主细胞感知某些微生物产物后产生的。β-羟基丁酸被证明至关重要:直接给予小鼠或人类类器官该分子即可模拟该细菌在损伤后激活储备干细胞的能力,随着愈合进展又将系统转向恢复的活跃干细胞库。当研究者在储备干细胞中有选择地删除了关键基因Hopx时,β-羟基丁酸不再能改善再生,证明该化学物质通过储备干细胞内的Hopx相关程序发挥作用。
肠道细菌与饮食的协作
进一步研究显示了一条更长的链条,将饮食、不同细菌伙伴与干细胞行为连接起来。Blautia coccoides将膳食氨基酸色氨酸转化为一种中间产物——吲哚-3-乳酸,但其自身无法完成全部代谢途径。其他常见肠道微生物,如Peptostreptococcus russellii和Clostridium sporogenes,接手将这一中间产物进一步转化为吲哚-3-丙酸(indole-3-propionic acid, IPA)。这一终产物刺激肠道细胞生成更多的β-羟基丁酸,进而激活Hopx阳性的储备干细胞。在培养皿中共同培养这些微生物,或在无菌小鼠中共同定植,均提高了IPA水平并增强了干细胞的修复信号。携带单一来自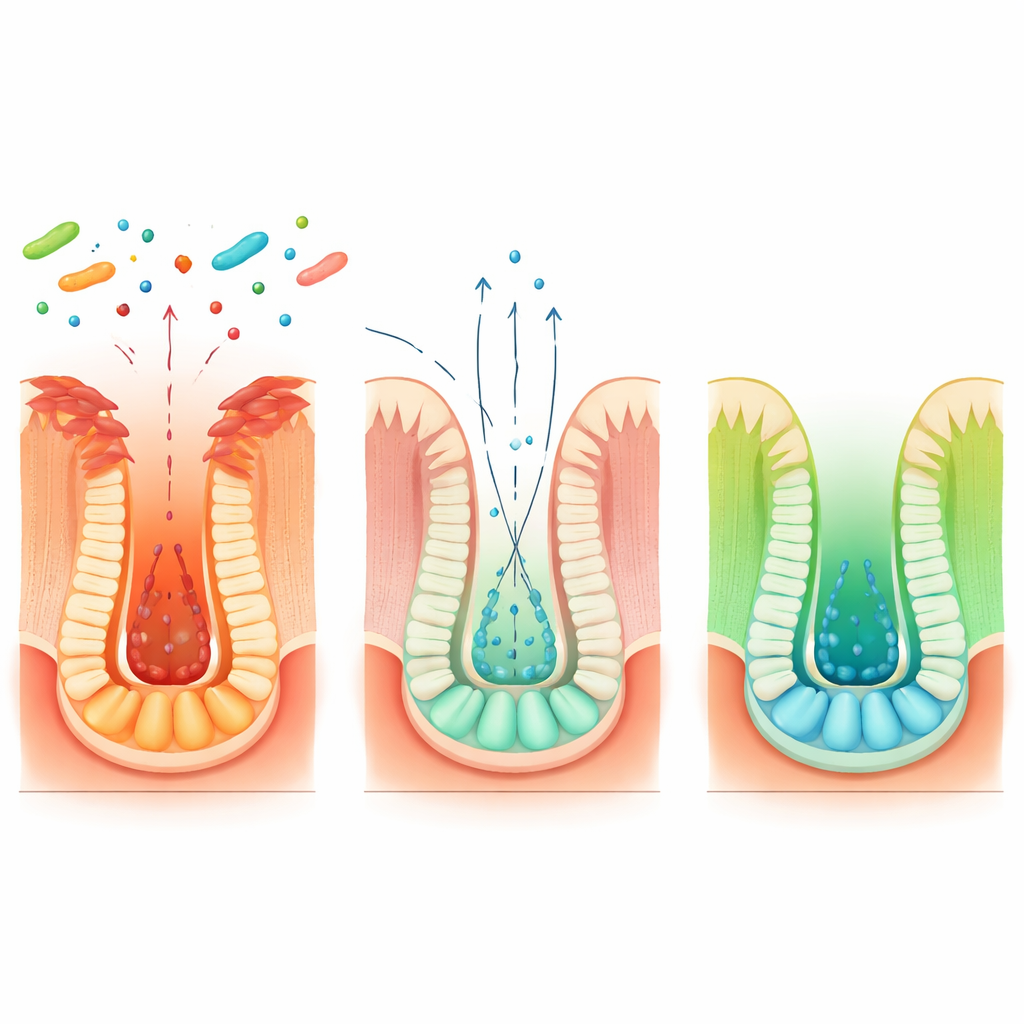
这对未来肠道治疗意味着什么
为测试饮食的重要性,研究人员让小鼠摄入不含色氨酸的饮食,这显著降低了吲哚类化合物的产生。这些动物出现更严重的结肠炎和更弱的干细胞反应。值得注意的是,直接补充吲哚-3-丙酸,或在补回色氨酸的同时重新引入工程化细菌,均可恢复愈合和干细胞激活。综合来看,这项工作勾勒出一条“微生物群—代谢物—干细胞”轴:膳食色氨酸被一组肠道微生物处理为一种信号,该信号促使肠道细胞产生β-羟基丁酸,后者通过Hopx激活储备干细胞以重建受损黏膜。对患者而言,这提示了一类新型治疗策略——结合精心选择的微生物、酶或代谢物与饮食干预,以温和促使肠道自身修复,而非单纯抑制免疫反应。
引用: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
关键词: 肠道微生物组, 炎性肠病, 肠道干细胞, 微生物代谢物, 黏膜修复