Clear Sky Science · it
Un asse microbiota-IPA facilita la rigenerazione mediata dalle cellule staminali intestinali nella colite tramite un programma associato a Hopx
Come i batteri gentili dell’intestino aiutano a riparare un intestino ferito
Milioni di persone con malattia infiammatoria intestinale convivono con un intestino cronicamente irritato e danneggiato. Quando il rivestimento interno dell’intestino si compromette, diventa doloroso e permeabile, permettendo a microbi e particelle di cibo di irritare ulteriormente il corpo. Questo studio rivela come alcuni batteri utili dell’intestino e i composti che producono possano attivare una riserva speciale di cellule staminali intestinali, accelerando la riparazione di questa barriera delicata. Comprendere questa collaborazione tra microbi, dieta e cellule staminali indica la strada verso terapie più miti che aiutino l’intestino a ricostruirsi invece di affidarsi solo a potenti farmaci immunosoppressori.
Un aiuto mancante nell’intestino infiammato
I ricercatori hanno iniziato confrontando i microbi intestinali di persone con malattia di Crohn, una forma di malattia infiammatoria intestinale, con quelli di volontari sani. Hanno scoperto che un batterio normalmente comune, Blautia coccoides, era drasticamente ridotto nei pazienti e in diversi modelli murini di colite. Quando hanno aggiunto deliberatamente questo batterio nell’intestino dei topi, gli animali risultavano molto più protetti da lesioni intestinali indotte chimicamente: i loro coloni restavano più lunghi e meno ristretti, i danni tissutali al microscopio erano più lievi e i segnali infiammatori erano ridotti. L’effetto protettivo si è mantenuto attraverso diversi tipi di lesione intestinale, inclusi irritazione chimica e radiazioni, suggerendo che questo microbo supporta in modo generale la capacità dell’intestino di resistere e recuperare dai danni. 
Cellule staminali di riserva: la squadra di emergenza dell’intestino
Il rivestimento dell’intestino si rinnova costantemente grazie a cellule staminali che risiedono in piccole cripte. Le cellule staminali più note sono molto attive ma fragili; spesso vengono distrutte durante infiammazioni gravi. Il gruppo ha dimostrato che Blautia coccoides aiuta un altro gruppo, più resistente, di cellule staminali “di riserva” a intervenire. Nei topi trattati con questo batterio, i geni legati alle cellule staminali di riserva venivano attivati precocemente dopo il danno, e sia le riserve sia i compartimenti di cellule staminali attive venivano preservati giorni dopo, quando negli animali di controllo erano in buona parte perduti. Esperimenti che hanno seguito il destino delle cellule staminali di riserva hanno mostrato che, sotto l’influenza del batterio, queste cellule quiescenti si sono risvegliate, si sono moltiplicate e hanno generato nuove cellule staminali attive che hanno ricostruito le cripte danneggiate. Mini-intestini umani e murini coltivati in laboratorio hanno confermato che questo programma rigenerativo può operare anche in tessuto umano.
Una catena chimica dalla dieta al microbo alla cellula staminale
Successivamente, gli scienziati si sono chiesti come un batterio intestinale potesse inviare un segnale di riparazione così preciso. Hanno scoperto che Blautia coccoides rimodella la chimica all’interno delle cellule intestinali per aumentare la produzione di una piccola molecola legata all’energia chiamata beta-idrossibutirrato. Piuttosto che essere prodotta dal batterio stesso, questa sostanza è fabbricata dalle cellule ospiti quando percepiscono certi prodotti microbici. Il beta-idrossibutirrato si è rivelato cruciale: somministrarlo direttamente a topi o organoidi umani ha imitato la capacità del batterio di attivare le cellule staminali di riserva dopo il danno e poi di riportare il sistema verso un pool rinnovato di cellule staminali attive mentre la guarigione procedeva. Quando i ricercatori hanno eliminato un gene chiave, Hopx, specificamente nelle cellule staminali di riserva, il beta-idrossibutirrato non migliorava più la rigenerazione, dimostrando che questo composto agisce attraverso un programma legato a Hopx nella riserva di cellule staminali.
Lavoro di squadra tra batteri intestinali e dieta
Approfondendo, il team ha mappato una catena più lunga che collega la dieta, diversi partner batterici e il comportamento delle cellule staminali. Blautia coccoides converte l’aminoacido dietetico triptofano in un composto intermedio chiamato acido indolo-3-lattico, ma non può completare da sola la via. Altri comuni microbi intestinali, come Peptostreptococcus russellii e Clostridium sporogenes, subentrano trasformando questo intermedio in acido indolo-3-propionico. Questo prodotto finale stimola le cellule intestinali a produrre più beta-idrossibutirrato, che poi attiva le cellule staminali di riserva Hopx-positive. Co-coltivare questi microbi in piastre, o co-colonizzare topi privi di microbi, aumentava i livelli di acido indolo-3-propionico e potenziava i segnali di riparazione delle cellule staminali. Un ceppo ingegnerizzato di E. coli portatore di un singolo enzima da Blautia ha riprodotto questa via nei topi, confermando ulteriormente i passaggi chiave. 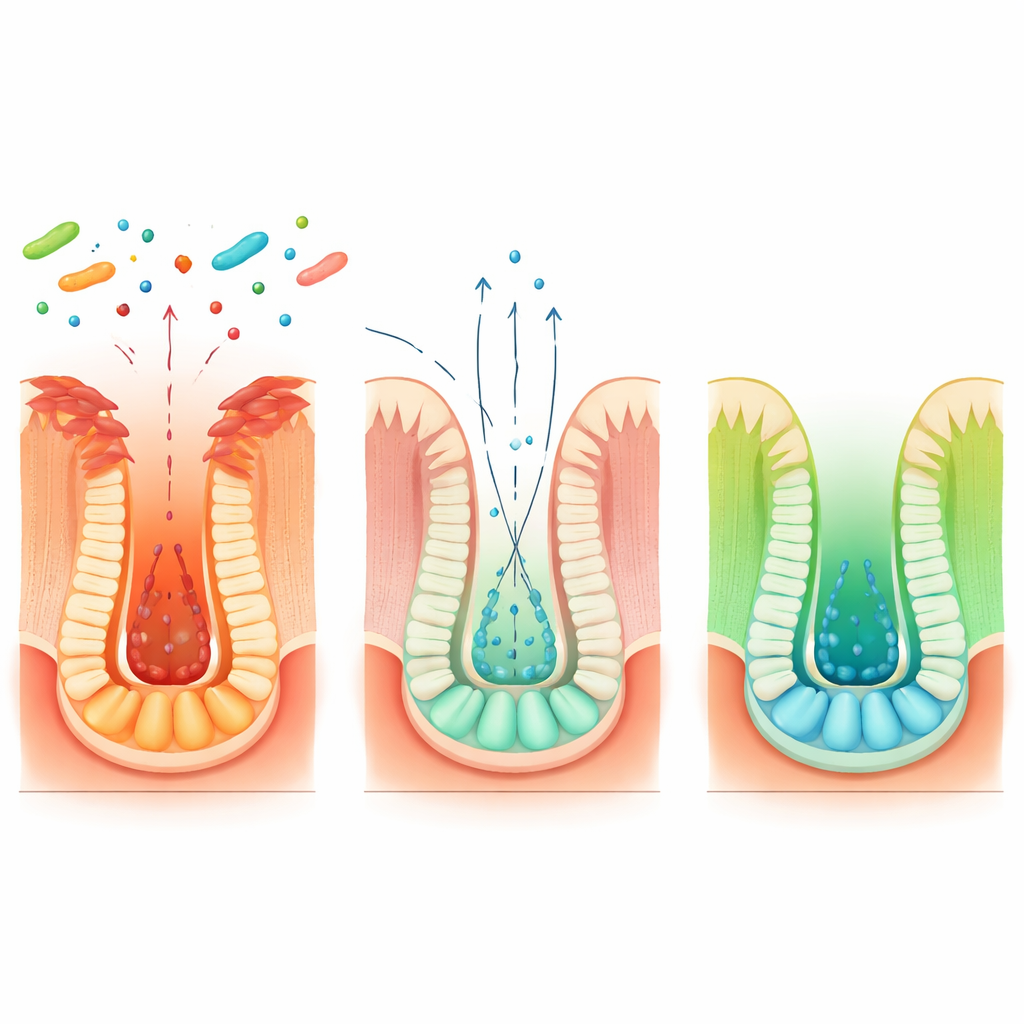
Cosa significa per le terapie intestinali future
Per testare l’importanza della dieta, i ricercatori hanno messo i topi su un regime privo di triptofano che ha ridotto drasticamente la produzione di composti indolici. Questi animali hanno sviluppato una colite più grave e risposte più deboli delle cellule staminali. Notevolmente, somministrare direttamente acido indolo-3-propionico, o reintrodurre il triptofano insieme ai batteri ingegnerizzati, ha ripristinato la guarigione e l’attivazione delle cellule staminali. Nel complesso, il lavoro delinea un «asse microbiota–metabolita–cellula staminale»: il triptofano alimentare è elaborato da una squadra di microbi intestinali in un segnale che induce le cellule intestinali a generare beta-idrossibutirrato, il quale a sua volta attiva le cellule staminali di riserva via Hopx per ricostruire il rivestimento danneggiato. Per i pazienti, questo suggerisce una nuova classe di terapie — usando microbi, enzimi o metaboliti scelti con cura, insieme alla dieta — per incoraggiare delicatamente le squadre di riparazione naturali dell’intestino invece di limitarsi ad abbassare la risposta immunitaria.
Citazione: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
Parole chiave: microbiota intestinale, malattia infiammatoria intestinale, cellule staminali intestinali, metaboliti microbici, guarigione della mucosa