Clear Sky Science · ru
Ось микробиоты–IPA облегчает регенерацию кишечника при колите за счёт стволовых клеток через программу, связанную с Hopx
Как дружественные кишечные микробы помогают болящему кишечнику заживать
Миллионы людей с воспалительным заболеванием кишечника живут с хронически раздражённой и повреждённой слизистой. Когда внутренняя оболочка кишки разрушается, это вызывает боль и повышенную проницаемость, позволяя микробам и частицам пищи ещё сильнее раздражать организм. В этом исследовании показано, как некоторые полезные кишечные бактерии и вещества, которые они стимулируют, могут включать специальный резервный пул кишечных стволовых клеток, ускоряя восстановление этого хрупкого барьера. Понимание этого взаимодействия между микробами, питанием и стволовыми клетками указывает на более мягкие методы лечения, помогающие кишечнику восстановиться самостоятельно, а не полагаться только на сильные иммуносупрессивные препараты.
Отсутствующий помощник в воспалённом кишечнике
Исследователи начали с сравнения кишечной микробиоты у людей с болезнью Крона, формы воспалительного заболевания кишечника, и у здоровых добровольцев. Они обнаружили, что обычно распространённая бактерия, Blautia coccoides, у пациентов и в нескольких мышиных моделях колита была резко сокращена. Когда учёные целенаправленно добавляли эту бактерию в кишечник мышей, животные оказались гораздо лучше защищены от химически вызванного повреждения кишечника: их толстая кишка оставалась дольше и меньше сужалась, повреждение тканей при микроскопии было мягче, а воспалительные сигналы уменьшились. Защитный эффект сохранялся при различных видах повреждений кишечника, включая химическое раздражение и облучение, что говорит о том, что этот микроорганизм в целом поддерживает способность кишечника противостоять и восстанавливаться после повреждений. 
Резервные стволовые клетки: аварийная бригада кишечника
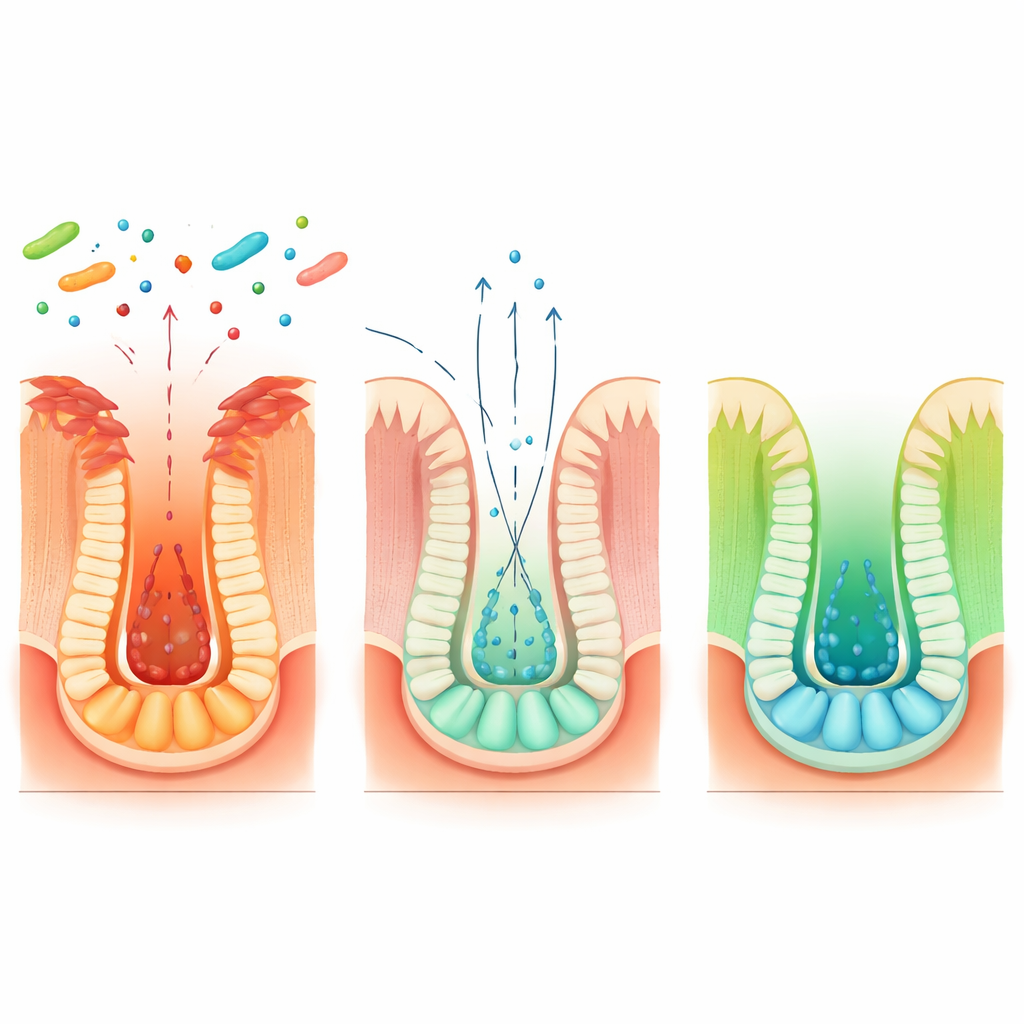
Слизистая кишечника постоянно обновляется стволовыми клетками, которые живут в крошечных впадинах — криптах. Наиболее известные стволовые клетки очень активны, но хрупки; при тяжёлом воспалении их часто уничтожают. Группа показала, что Blautia coccoides помогает другой, более устойчивой группе «резервных» стволовых клеток вступить в работу. У мышей, получивших эту бактерию, гены, связанные с резервными стволовыми клетками, включались рано после повреждения, и как резервный, так и активный стволовые популяции сохранялись через несколько дней, когда у контрольных животных они в значительной степени исчезали. Эксперименты с отслеживанием судьбы резервных стволовых клеток показали, что под влиянием бактерии эти «тихие» клетки просыпались, размножались и порождали новые активные стволовые клетки, которые восстанавливали повреждённые крипты. Мини-кишечники человека и мыши, выращенные в лаборатории, подтвердили, что эта регенеративная программа также работает в человеческой ткани.
Химическая цепочка от диеты через микроб до стволовой клетки
Далее учёные выясняли, как кишечная бактерия посылает столь точный сигнал к восстановлению. Они обнаружили, что Blautia coccoides меняет химию внутри кишечных клеток, усиливая производство небольшого энергетического молекулы бета-гидроксибутирата. Эта молекула не синтезируется самой бактерией, а вырабатывается клетками хозяина, когда те чувствуют определённые микробные продукты. Бета-гидроксибутират оказался критически важен: его введение напрямую мышам или человеческим органоидам имитировало способность бактерии активировать резервные стволовые клетки после повреждения, а затем по мере заживления возвращать систему к восстановленному пулу активных стволовых клеток. Когда исследователи удалили ключевой ген Hopx специально в резервных стволовых клетках, бета-гидроксибутират уже не улучшал регенерацию, что доказывает: этот химический сигнал действует через программу, связанную с Hopx, в резервном пуле стволовых клеток.
Командная работа между кишечными бактериями и диетой
Углубляясь, команда проследила более длинную цепочку, связывающую питание, различных бактериальных партнёров и поведение стволовых клеток. Blautia coccoides превращает пищевую аминокислоту триптофан в промежуточное соединение индол-3-молочную кислоту, но сам по себе не завершает путь. Другие распространённые кишечные микробы, такие как Peptostreptococcus russellii и Clostridium sporogenes, берут эту цепочку на себя, превращая промежуточное соединение в индол-3-пропионовую кислоту. Этот конечный продукт стимулирует кишечные клетки к производству большего количества бета-гидроксибутирата, который затем активирует Hopx-положительные резервные стволовые клетки. Совместное культивирование этих микроорганизмов в чашках Петри или ко-колонизация бесмикробных мышей повышало уровни индол-3-пропионовой кислоты и усиливало сигналы реставрации стволовых клеток. Инженерный штамм E. coli, несущий один фермент от Blautia, воспроизвёл этот путь в мышах, дополнительно подтверждая ключевые звенья.
Что это значит для будущих терапий кишечника
Чтобы проверить значение диеты, исследователи посадили мышей на рацион без триптофана, что резко снизило образование индольных соединений. Эти животные перенесли более тяжёлый колит и показали слабые ответы стволовых клеток. Поразительно, что введение индол-3-пропионовой кислоты непосредственно или повторное введение триптофана вместе с инженерными бактериями восстановило заживление и активацию стволовых клеток. В совокупности работа описывает «ось микробиота–метаболит–стволовая клетка»: пищевой триптофан перерабатывается командой кишечных микробов в сигнал, который побуждает клетки хозяина производить бета-гидроксибутират, а тот через Hopx включает резервные стволовые клетки для восстановления повреждённой оболочки. Для пациентов это предлагает новый класс терапий — использование тщательно подобранных микробов, ферментов или метаболитов в сочетании с диетой — чтобы мягко стимулировать собственные ремонтные силы кишечника, а не просто подавлять иммунный ответ.
Цитирование: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
Ключевые слова: кишечный микробиом, воспалительное заболевание кишечника, кишечные стволовые клетки, микробные метаболиты, заживление слизистой