Clear Sky Science · fr
Un axe microbiote–IPA facilite la régénération médiée par les cellules souches intestinales dans la colite via un programme associé à Hopx
Comment les bactéries amies de l’intestin aident une muqueuse blessée à guérir
Des millions de personnes atteintes de maladie inflammatoire de l’intestin vivent avec un intestin enflammé et endommagé en permanence. Lorsque la couche interne de l’intestin se détériore, elle devient douloureuse et perméable, permettant aux microbes et aux particules alimentaires d’irriter encore davantage l’organisme. Cette étude révèle comment certaines bactéries utiles du microbiote et les composés qu’elles produisent peuvent activer une réserve spéciale de cellules souches intestinales, accélérant la réparation de cette barrière fragile. Comprendre ce partenariat entre microbes, alimentation et cellules souches ouvre la voie à des traitements plus doux qui favorisent la reconstruction par l’intestin lui‑même plutôt que de dépendre uniquement de puissants médicaments immunosuppresseurs.
Un auxiliaire manquant dans l’intestin enflammé
Les chercheurs ont commencé par comparer les microbes intestinaux de personnes atteintes de la maladie de Crohn, une forme de maladie inflammatoire de l’intestin, à ceux de volontaires sains. Ils ont constaté qu’une bactérie normalement courante, Blautia coccoides, était fortement diminuée chez les patients et dans plusieurs modèles murins de colite. Lorsqu’ils ont délibérément introduit cette bactérie dans les intestins de souris, les animaux ont été beaucoup mieux protégés contre des lésions intestinales induites chimiquement : leurs côlons restaient plus longs et moins rétractés, les lésions tissulaires observées au microscope étaient plus modérées et les signaux inflammatoires étaient réduits. L’effet protecteur se maintenait face à différents types d’atteintes intestinales, y compris une irritation chimique et des radiations, suggérant que ce microbe soutient de façon générale la capacité de l’intestin à résister et à se remettre des dommages. 
Des cellules souches de secours : l’équipe d’urgence de l’intestin
La muqueuse intestinale se renouvelle en permanence grâce à des cellules souches qui résident dans de petits puits appelés cryptes. Les cellules souches les mieux connues sont très actives mais fragiles ; elles sont souvent anéanties lors d’une inflammation sévère. L’équipe a montré que Blautia coccoides aide un autre groupe plus résilient de cellules souches « de réserve » à intervenir. Chez les souris recevant cette bactérie, les gènes liés aux cellules souches de réserve s’activent tôt après la lésion, et les compartiments de cellules souches de réserve et actives sont préservés plusieurs jours plus tard, alors que chez les animaux témoins ils étaient largement perdus. Des expériences de traçage du devenir des cellules souches de réserve ont montré que, sous l’influence de la bactérie, ces cellules silencieuses se réveillent, se multiplient et donnent naissance à de nouvelles cellules souches actives qui reconstruisent les cryptes endommagées. Des mini‑intestins humains et murins cultivés en laboratoire ont confirmé que ce programme de régénération peut également opérer dans le tissu humain.
Une chaîne chimique reliant alimentation, microbe et cellule souche
Les scientifiques se sont ensuite demandé comment une bactérie intestinale pouvait envoyer un signal de réparation aussi précis. Ils ont découvert que Blautia coccoides modifie la chimie à l’intérieur des cellules intestinales pour augmenter la production d’une petite molécule liée à l’énergie appelée bêta‑hydroxybutyrate. Plutôt que d’être produite par la bactérie elle‑même, cette molécule est synthétisée par les cellules de l’hôte lorsqu’elles détectent certains produits microbiens. Le bêta‑hydroxybutyrate s’est avéré crucial : l’en administrer directement à des souris ou à des organoïdes humains imitait la capacité de la bactérie à activer les cellules souches de réserve après une lésion, puis à réorienter le système vers un pool renouvelé de cellules souches actives au fur et à mesure de la cicatrisation. Lorsque les chercheurs ont supprimé un gène clé, Hopx, spécifiquement dans les cellules souches de réserve, le bêta‑hydroxybutyrate n’a plus amélioré la régénération, prouvant que ce composé agit via un programme associé à Hopx dans le pool de cellules souches de secours.
Travail d’équipe entre bactéries intestinales et alimentation
En creusant davantage, l’équipe a cartographié une chaîne plus longue reliant l’alimentation, différents partenaires bactériens et le comportement des cellules souches. Blautia coccoides convertit l’acide aminé alimentaire tryptophane en un composé intermédiaire appelé acide indole‑3‑lactique, mais ne peut pas achever la voie seul. D’autres microbes courants de l’intestin, tels que Peptostreptococcus russellii et Clostridium sporogenes, prennent le relais pour transformer cet intermédiaire en acide indole‑3‑propionique. Ce produit final stimule les cellules intestinales à produire davantage de bêta‑hydroxybutyrate, qui active ensuite les cellules souches de réserve positives pour Hopx. Le cocultivage de ces microbes en boîtes de Pétri, ou la co‑colonisation de souris exemptes de microbes, augmentait les niveaux d’acide indole‑3‑propionique et renforçait les signaux de réparation des cellules souches. Une souche d’E. coli modifiée portant une seule enzyme issue de Blautia a reproduit cette voie chez la souris, confirmant encore les étapes clés. 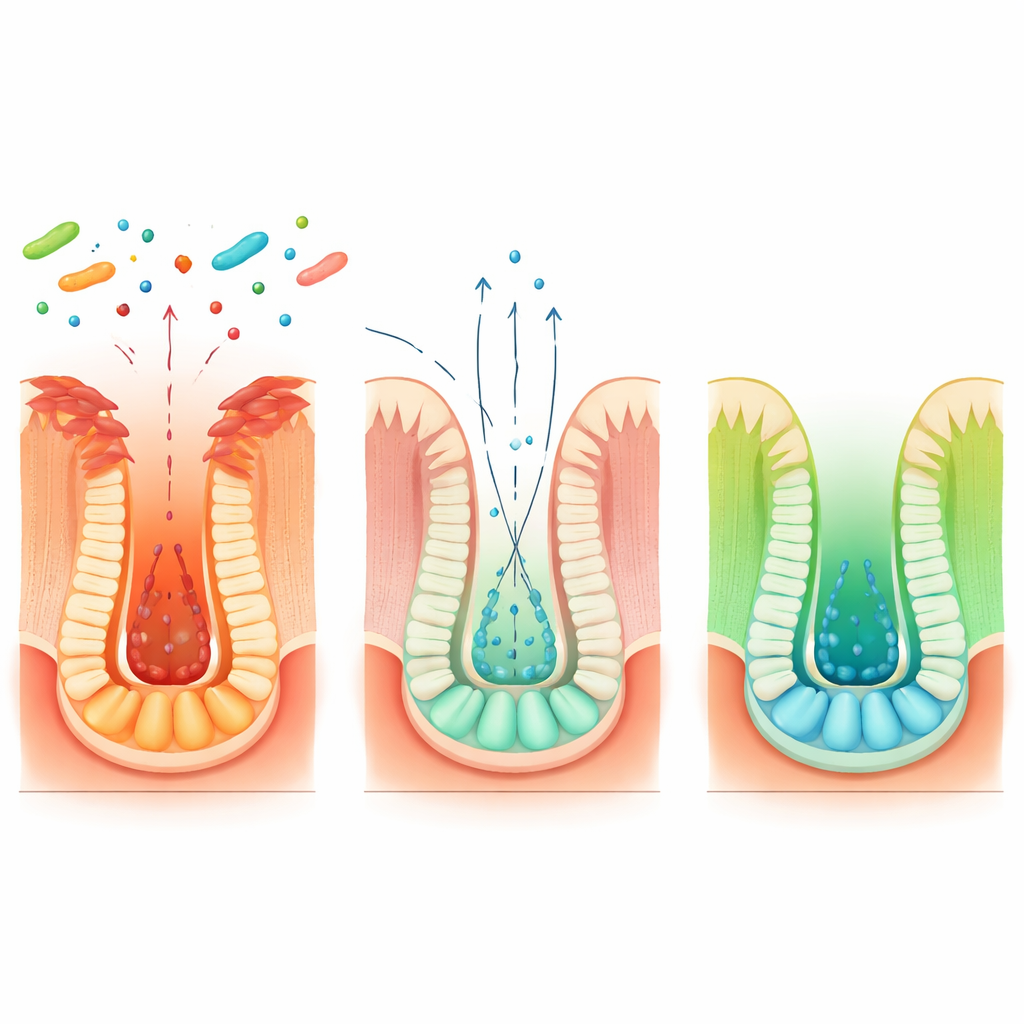
Ce que cela signifie pour les futures thérapies intestinales
Pour tester l’importance de l’alimentation, les chercheurs ont soumis des souris à un régime sans tryptophane qui a fortement réduit la production de composés indoliques. Ces animaux ont souffert d’une colite plus grave et de réponses des cellules souches affaiblies. Remarquablement, l’administration directe d’acide indole‑3‑propionique, ou la réintroduction de tryptophane avec les bactéries modifiées, a restauré la cicatrisation et l’activation des cellules souches. Au total, ce travail décrit un axe « microbiote–métabolite–cellule souche » : le tryptophane alimentaire est transformé par une équipe de microbes intestinaux en un signal qui incite les cellules intestinales à produire du bêta‑hydroxybutyrate, lequel active via Hopx les cellules souches de réserve pour reconstruire la muqueuse endommagée. Pour les patients, cela suggère une nouvelle catégorie de thérapies — utilisant des microbes sélectionnés, des enzymes ou des métabolites, en association avec l’alimentation — pour stimuler en douceur les équipes de réparation de l’intestin plutôt que de se contenter d’atténuer la réponse immunitaire.
Citation: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
Mots-clés: microbiote intestinal, maladie inflammatoire de l’intestin, cellules souches intestinales, métabolites microbiens, cicatrisation muqueuse