Clear Sky Science · ar
محور الميكروبيوتا-IPA يسهل تجدد الخلايا الجذعية المعوية في التهاب القولون عبر برنامج مرتبط بـ Hopx
كيف تساعد البكتيريا النافعة في الأمعاء الأمعاء المتألمة على الشفاء
يعيش ملايين الأشخاص المصابين بمرض الأمعاء الالتهابي مع أمعاء متهيجة ومتضررة بشكل مزمن. عندما يتعطل الغطاء الداخلي للأمعاء، يصبح الأمر مؤلمًا وتسري السوائل عبره، مما يسمح للميكروبات وجزيئات الطعام بإثارة الجسم بشكل أكبر. تكشف هذه الدراسة كيف أن بعض بكتيريا الأمعاء المفيدة والمواد الكيميائية التي تصنعها يمكن أن تشغّل مجموعة احتياطية خاصة من الخلايا الجذعية المعوية، ما يسرّع إصلاح هذا الحاجز الحساس. وفهم هذا التعاون بين الميكروبات والنظام الغذائي والخلايا الجذعية يشير إلى علاجات ألطف تساعد الأمعاء على إعادة بناء نفسها بدل الاعتماد فقط على أدوية قوية مثبطة للمناعة.
مساعد مفقود في الأمعاء الملتهبة
بدأ الباحثون بمقارنة ميكروبات الأمعاء لدى أشخاص مصابين بداء كرون، وهو شكل من أشكال مرض الأمعاء الالتهابي، مع ميكروبات متطوعين أصحاء. وجدوا أن بكتيريا كانت شائعة عادة، Blautia coccoides، كانت منخفضة بشكل ملحوظ لدى المرضى وفي عدة نماذج فئران لالتهاب القولون. عندما أضافوا هذه البكتيريا عمدًا إلى أمعاء الفئران، كانت الحيوانات محمية بشكل أفضل بكثير من الإصابة الكيميائية في الأمعاء: ابقت أمعاؤهم الغليظة أطول وأقل تضيّقًا، وكان الضرر النسيجي تحت المجهر أخف، وتراجعت الإشارات الالتهابية. دام التأثير الوقائي عبر أنواع مختلفة من إصابات الأمعاء، بما في ذلك التهيج الكيميائي والإشعاع، ما يوحي أن هذه الميكروب تدعم بشكل عام قدرة الأمعاء على الصمود والتعافي من الأذى. 
الخلايا الجذعية الاحتياطية: طواقم الطوارئ في الأمعاء
يتجدد الغطاء الداخلي للأمعاء باستمرار بواسطة خلايا جذعية تعيش في حفر دقيقة تسمى الحُفَر. أشهر الخلايا الجذعية معروفة بنشاطها العالي لكنها هشة؛ غالبًا ما تُدمر أثناء الالتهاب الشديد. أظهرت المجموعة أن Blautia coccoides يساعد مجموعة أخرى أكثر مرونة من الخلايا الجذعية "الاحتياطية" لتتدخل. في الفئران التي أعطيت هذه البكتيريا، شغلت جينات مرتبطة بالخلايا الجذعية الاحتياطية مبكرًا بعد الإصابة، وحُفظت كل من مقصورات الخلايا الجذعية الاحتياطية والنشطة بعد أيام، بينما فقدت حيوانات الضبط معظم خلاياها. أظهرت تجارب تتبّع مصير الخلايا الجذعية الاحتياطية أنه تحت تأثير البكتيريا، استيقظت هذه الخلايا الهادئة، وتكاثرت، وأنتجت خلايا جذعية نشطة جديدة أعادت بناء الحُفَر المتضررة. أكدت أمعاء مصغرة بشرية وفئر نمت في المختبر أن هذا البرنامج التجديدي يمكن أن يعمل أيضًا في نسيج بشري.
سلسلة كيميائية من النظام الغذائي إلى الميكروب إلى الخلية الجذعية
سأل العلماء بعد ذلك كيف يمكن لبكتيريا معوية أن ترسل إشارة إصلاح دقيقة كهذه. اكتشفوا أن Blautia coccoides يعيد تشكيل الكيمياء داخل خلايا الأمعاء ليعزز إنتاج جزيء صغير مرتبط بالطاقة يدعى بيتا-هيدروكسي بيوتيرات. لم يُصنع هذا المركب بواسطة البكتيريا نفسها بقدر ما يُنتَج بواسطة خلايا المضيف عندما تستشعر منتجات ميكروبية معينة. تبين أن بيتا-هيدروكسي بيوتيرات حاسم: إعطاؤه مباشرة للفئران أو للأعضاء المعوية المصغرة البشرية حاكى قدرة البكتيريا على تنشيط الخلايا الجذعية الاحتياطية بعد الإصابة ثم إعادة توجيه النظام نحو تجمع متجدد من الخلايا الجذعية النشطة مع تقدم الشفاء. عندما حذف الباحثون جينًا رئيسيًا، Hopx، بشكل محدد في الخلايا الجذعية الاحتياطية، لم يعد بيتا-هيدروكسي بيوتيرات يحسّن التجدد، مما يثبت أن هذه المادة الكيميائية تعمل عبر برنامج مرتبط بـ Hopx في تجمع الخلايا الجذعية الاحتياطية.
عمل جماعي بين بكتيريا الأمعاء والنظام الغذائي
بالتعمق أكثر، رسم الفريق سلسلة أطول تربط النظام الغذائي وشركاء بكتيريين مختلفين وسلوك الخلايا الجذعية. يحول Blautia coccoides الحمض الأميني الغذائي تريبتوفان إلى مركب وسيط يدعى حمض الإندول-3-لاكتيك، لكنه لا يستطيع إكمال المسار بمفرده. تتولى ميكروبات أمعاء شائعة أخرى، مثل Peptostreptococcus russellii وClostridium sporogenes، من هناك، وتحول هذا الوسيط إلى حمض الإندول-3-بروبيونيك. هذا المنتج النهائي يحفز خلايا الأمعاء على صنع مزيد من بيتا-هيدروكسي بيوتيرات، الذي ينشط بدوره الخلايا الجذعية الاحتياطية الإيجابية لـ Hopx. زادت زرع هذه الميكروبات معًا في أطباق أو استعمار فئران خالية من الجراثيم بمجموعات مشتركة من مستويات حمض الإندول-3-بروبيونيك وعززت إشارات إصلاح الخلايا الجذعية. أعاد سلالة مهندسة من E. coli تحمل إنزيمًا واحدًا من Blautia إنتاج هذا المسار في الفئران، مؤكدًا المزيد من خطواته الأساسية. 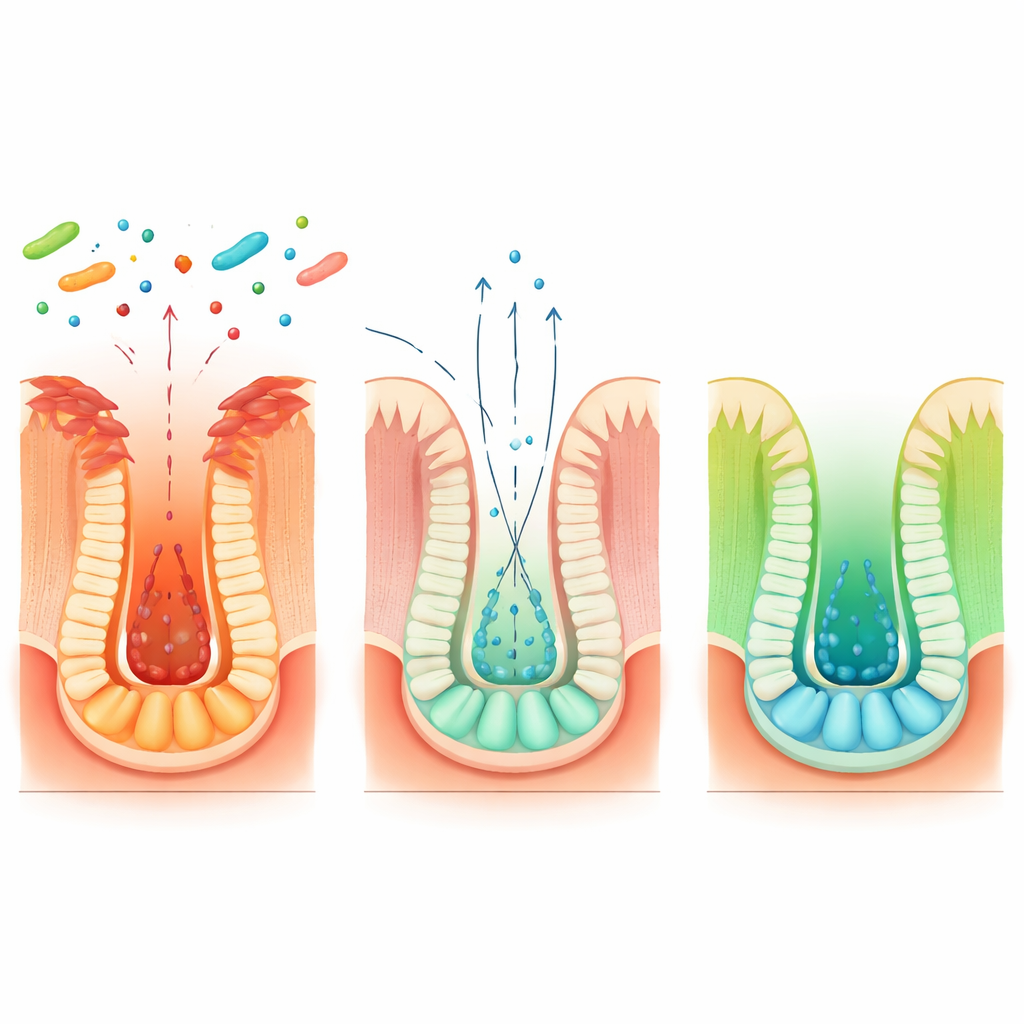
ما الذي يعنيه هذا لعلاجات الأمعاء المستقبلية
لاختبار أهمية النظام الغذائي، وضع الباحثون الفئران على نظام خالٍ من التريبتوفان خفض بشدة إنتاج مركبات الإندول. عانت هذه الحيوانات من التهاب قولون أسوأ واستجابات خلايا جذعية أضعف. بشكل لافت، أدى تزويدها بحمض الإندول-3-بروبيونيك مباشرة، أو إعادة إدخال التريبتوفان مع البكتيريا المهندسة، إلى استعادة الشفاء وتنشيط الخلايا الجذعية. مجتمعة، توضح هذه النتائج محورًا "الميكروبيوتا–المستقلب–الخلايا الجذعية": يُعالَج التريبتوفان الغذائي بواسطة فريق من ميكروبات الأمعاء إلى إشارة تدفع خلايا الأمعاء لإنتاج بيتا-هيدروكسي بيوتيرات، الذي يشغّل بعد ذلك الخلايا الجذعية الاحتياطية عبر Hopx لإعادة بناء الغطاء المتضرر. بالنسبة للمرضى، يقترح هذا فئة جديدة من العلاجات—باستخدام ميكروبات، أو إنزيمات، أو مستقلبات مختارة بعناية، جنبًا إلى جنب مع النظام الغذائي—لتشجيع طواقم الإصلاح الذاتية في الأمعاء بلطف بدلًا من الاقتصار على خفض استجابة المناعة.
الاستشهاد: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
الكلمات المفتاحية: الميكروبيوم المعوي, مرض الأمعاء الالتهابي, الخلايا الجذعية المعوية, نواتج أيضية ميكروبية, التئام الغشاء المخاطي