Clear Sky Science · pl
Oś mikrobiota–IPA ułatwia regenerację jelit sterowaną przez komórki macierzyste w colitis poprzez program związany z Hopx
Jak przyjazne bakterie jelitowe pomagają zranionemu jelitu się zregenerować
Miliony osób z chorobami zapalnymi jelit żyją z przewlekle podrażnionym i uszkodzonym jelitem. Gdy wewnętrzna wyściółka przewodu pokarmowego ulega zniszczeniu, staje się bolesna i przepuszczalna, co pozwala bakteriom i fragmentom pokarmu jeszcze bardziej drażnić organizm. Badanie to ujawnia, w jaki sposób niektóre pożyteczne bakterie jelitowe i związki przez nie wytwarzane mogą uruchomić specjalną pulę zapasowych komórek macierzystych jelita, przyspieszając naprawę tej delikatnej bariery. Zrozumienie tej współpracy między mikrobiotą, dietą a komórkami macierzystymi otwiera drogę do delikatniejszych terapii, które pomagają jelitu się odbudować, zamiast polegać wyłącznie na silnych lekach tłumiących układ odpornościowy.
Brakujący pomocnik w zapalonym jelicie
Naukowcy zaczęli od porównania mikrobioty jelitowej osób z chorobą Crohna, formą choroby zapalnej jelit, z mikrobiotą zdrowych ochotników. Stwierdzili, że powszechnie występujący zwykle drobnoustrój, Blautia coccoides, był wyraźnie zredukowany u pacjentów oraz w kilku modelach mysich colitis. Gdy celowo wprowadzono tę bakterię do jelit myszy, zwierzęta były znacznie lepiej chronione przed chemicznie wywołanym uszkodzeniem jelita: ich okrężnice pozostawały dłuższe i mniej skurczone, uszkodzenia tkanek w mikroskopie były łagodniejsze, a sygnały zapalne zmniejszone. Efekt ochronny utrzymywał się przy różnych rodzajach urazów jelit, w tym przy podrażnieniu chemicznym i promieniowaniu, co sugeruje, że ten mikroorganizm w szerokim zakresie wspiera zdolność jelita do znoszenia i odzyskiwania równowagi po uszkodzeniu. 
Zapasowe komórki macierzyste: zespół ratunkowy jelita
Wyściółka jelita jest nieustannie odnawiana przez komórki macierzyste żyjące w drobnych zagłębieniach zwanych kryptami. Najbardziej znane komórki macierzyste są bardzo aktywne, lecz kruche; często są niszczone podczas silnego zapalenia. Zespół wykazał, że Blautia coccoides wspiera inną, bardziej odporną grupę „rezerwowych” komórek macierzystych, które wkraczają do akcji. U myszy otrzymujących tę bakterię geny związane z rezerwową pulą komórek macierzystych były włączane wcześnie po urazie, a zarówno rezerwowe, jak i aktywne populacje komórek macierzystych były zachowane kilka dni później, gdy w kontrolnych zwierzętach większość z nich zniknęła. Eksperymenty śledzące los rezerwowych komórek pokazały, że pod wpływem bakterii te ciche komórki budziły się, namnażały i dawały początek nowym aktywnym komórkom macierzystym, które odbudowywały uszkodzone krypty. Mini-jelita ludzkie i mysie hodowane w laboratorium potwierdziły, że ten program regeneracyjny może działać także w ludzkiej tkance.
Łańcuch chemiczny: od diety przez mikroby do komórek macierzystych
Następnie naukowcy zapytali, jak bakteria jelitowa może wysyłać tak precyzyjny sygnał naprawczy. Odkryli, że Blautia coccoides przekształca chemię wewnątrz komórek jelitowych tak, że zwiększa produkcję małej cząsteczki związanej z energią, zwanej beta-hydroksymaślanem. Związek ten nie jest wytwarzany przez bakterie same, lecz produkowany przez komórki gospodarza, gdy wykrywają określone produkty mikrobiologiczne. Beta-hydroksymaślan okazał się kluczowy: podawanie go bezpośrednio myszom lub organoidom ludzkim naśladowało zdolność bakterii do aktywacji rezerwowych komórek macierzystych po urazie, a następnie przesunięcia systemu w stronę uzupełnionej puli aktywnych komórek macierzystych w miarę gojenia. Gdy badacze usunęli kluczowy gen Hopx specyficznie w rezerwowych komórkach macierzystych, beta-hydroksymaślan przestał poprawiać regenerację, dowodząc, że ta cząsteczka działa poprzez program powiązany z Hopx w zapasowej puli komórek macierzystych.
Współpraca bakterii jelitowych i diety
Dłuższe poszukiwania doprowadziły zespół do mapy łączącej dietę, różnych partnerów bakteryjnych i zachowanie komórek macierzystych. Blautia coccoides przekształca aminokwas pokarmowy tryptofan w pośredni związek zwany indol-3-mlekowym, ale nie kończy tej ścieżki sama. Inne powszechne bakterie jelitowe, takie jak Peptostreptococcus russellii i Clostridium sporogenes, przejmują dalej, przekształcając ten pośrednik w indol-3-propionowy kwas (indole-3-propionic acid). Ten końcowy produkt stymuluje komórki jelitowe do wytwarzania większej ilości beta-hydroksymaślanu, który następnie aktywuje Hopx-dodatnie rezerwowe komórki macierzyste. Wspólne hodowle tych mikroorganizmów na szalkach lub współkolonizacja myszy wolnych od drobnoustrojów zwiększały poziomy indol-3-propionowego kwasu i wzmacniały sygnały naprawcze komórek macierzystych. Inżynieryjny szczep E. coli niosący pojedynczy enzym z Blautia odtworzył tę ścieżkę u myszy, co dodatkowo potwierdziło kluczowe etapy. 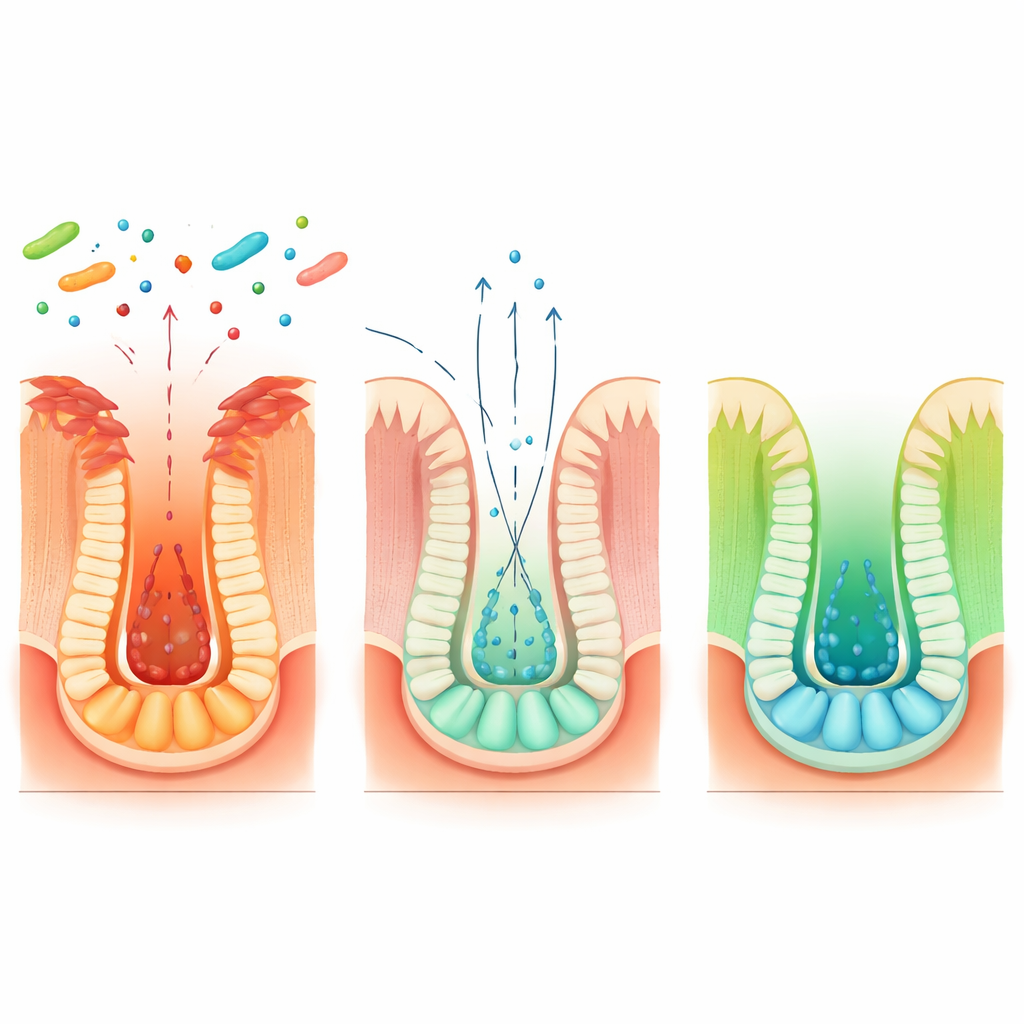
Co to oznacza dla przyszłych terapii jelitowych
Aby przetestować znaczenie diety, badacze umieścili myszy na diecie pozbawionej tryptofanu, co wyraźnie zmniejszyło produkcję związków indolowych. Zwierzęta te doświadczyły cięższej postaci colitis i słabszych reakcji komórek macierzystych. Zadziwiająco, podawanie indol-3-propionowego kwasu bezpośrednio lub ponowne wprowadzenie tryptofanu wraz z inżynieryjnymi bakteriami przywracało gojenie i aktywację komórek macierzystych. W sumie praca opisuje oś „mikrobiota–metabolit–komórka macierzysta”: tryptofan z diety jest przetwarzany przez zespół mikroorganizmów jelitowych na sygnał, który pobudza komórki jelitowe do produkcji beta-hydroksymaślanu, a ten z kolei włącza rezerwowe komórki macierzyste przez Hopx, aby odbudować uszkodzoną wyściółkę. Dla pacjentów sugeruje to nową klasę terapii — wykorzystanie starannie dobranych mikroorganizmów, enzymów lub metabolitów wraz z dietą — aby delikatnie pobudzać własne zespoły naprawcze jelita zamiast jedynie tłumić odpowiedź immunologiczną.
Cytowanie: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
Słowa kluczowe: mikrobiom jelitowy, choroba zapalna jelit, komórki macierzyste jelit, metabolity mikrobiologiczne, gojenie błony śluzowej