Clear Sky Science · pt
Um eixo microbiota-IPA facilita a regeneração mediada por células-tronco intestinais na colite por meio de um programa associado a Hopx
Como germes amigáveis do intestino ajudam um intestino lesionado a se curar
Milhões de pessoas com doença inflamatória intestinal vivem com o intestino cronicamente irritado e danificado. Quando o revestimento interno do intestino se rompe, ele fica dolorido e permeável, permitindo que micróbios e partículas de alimento irritem ainda mais o corpo. Este estudo revela como certas bactérias benéficas do intestino e os compostos que elas produzem podem ativar um reservatório especial de células-tronco intestinais, acelerando o reparo dessa barreira delicada. Compreender essa parceria entre micróbios, dieta e células-tronco aponta para tratamentos mais brandos que ajudam o intestino a se reconstruir em vez de depender apenas de medicamentos fortes que suprimem o sistema imune.
Um ajudante ausente no intestino inflamado
Os pesquisadores começaram comparando os micróbios intestinais de pessoas com doença de Crohn, uma forma de doença inflamatória intestinal, com os de voluntários saudáveis. Eles descobriram que uma bactéria normalmente comum, Blautia coccoides, estava marcadamente reduzida em pacientes e em vários modelos murinos de colite. Quando eles adicionaram propositalmente essa bactéria aos intestinos de camundongos, os animais ficaram muito mais protegidos contra lesão intestinal induzida quimicamente: seus cólons permaneceram por mais tempo e menos encolhidos, o dano tecidual ao microscópio foi mais leve e os sinais inflamatórios foram reduzidos. O efeito protetor se manteve em diferentes tipos de lesão intestinal, incluindo irritação química e radiação, sugerindo que esse micro-organismo apoia de forma ampla a capacidade do intestino de resistir e se recuperar do dano. 
Células-tronco de reserva: a equipe de emergência do intestino
O revestimento do intestino é renovado continuamente por células-tronco que vivem em pequenas cavidades chamadas criptas. As células-tronco mais conhecidas são altamente ativas, mas frágeis; frequentemente são eliminadas durante inflamações severas. A equipe mostrou que Blautia coccoides ajuda outro grupo, mais resiliente, de células-tronco “de reserva” a intervir. Em camundongos recebendo essa bactéria, genes ligados às células-tronco de reserva foram ativados precocemente após a lesão, e tanto os compartimentos de reserva quanto os ativos das células-tronco foram preservados dias depois, quando os animais controle já haviam perdido a maior parte deles. Experimentos rastreando o destino das células-tronco de reserva mostraram que, sob a influência da bactéria, essas células silenciosas despertaram, se multiplicaram e deram origem a novas células-tronco ativas que reconstruíram as criptas danificadas. Mini-intestinos humanos e de camundongo cultivados em laboratório confirmaram que esse programa regenerativo também pode operar em tecido humano.
Uma cadeia química da dieta ao micro-organismo até a célula-tronco
Em seguida, os cientistas perguntaram como uma bactéria intestinal poderia enviar um sinal de reparo tão preciso. Eles descobriram que Blautia coccoides remodela a química dentro das células intestinais para aumentar a produção de uma pequena molécula relacionada à energia chamada beta-hidroxibutirato. Em vez de ser produzida pela própria bactéria, essa substância é gerada pelas células do hospedeiro quando elas detectam certos produtos microbianos. O beta-hidroxibutirato mostrou-se crucial: administrá-lo diretamente a camundongos ou organoides humanos imitou a capacidade da bactéria de ativar células-tronco de reserva após a lesão e, à medida que a cicatrização progredia, de recolocar o sistema em direção a um pool reabastecido de células-tronco ativas. Quando os pesquisadores deletaram um gene chave, Hopx, especificamente nas células-tronco de reserva, o beta-hidroxibutirato deixou de melhorar a regeneração, provando que esse composto age por meio de um programa ligado a Hopx no pool de células-tronco de reserva.
Trabalho em equipe entre bactérias intestinais e dieta
Investigando mais a fundo, a equipe mapeou uma cadeia mais longa que conecta a dieta, diferentes parceiros bacterianos e o comportamento das células-tronco. Blautia coccoides converte o aminoácido dietético triptofano em um composto intermediário chamado ácido indol-3-láctico, mas não consegue completar a via sozinha. Outros micróbios intestinais comuns, como Peptostreptococcus russellii e Clostridium sporogenes, assumem a partir daí, transformando esse intermediário em ácido indol-3-propiónico. Esse produto final estimula as células intestinais a produzir mais beta-hidroxibutirato, que então ativa as células-tronco de reserva Hopx-positivas. Co-cultivar esses micróbios em placas ou co-colonizar camundongos livres de germes aumentou os níveis de ácido indol-3-propiónico e reforçou os sinais de reparo das células-tronco. Uma cepa de E. coli engenheirada carregando uma única enzima de Blautia reproduziu essa via em camundongos, confirmando ainda mais as etapas-chave. 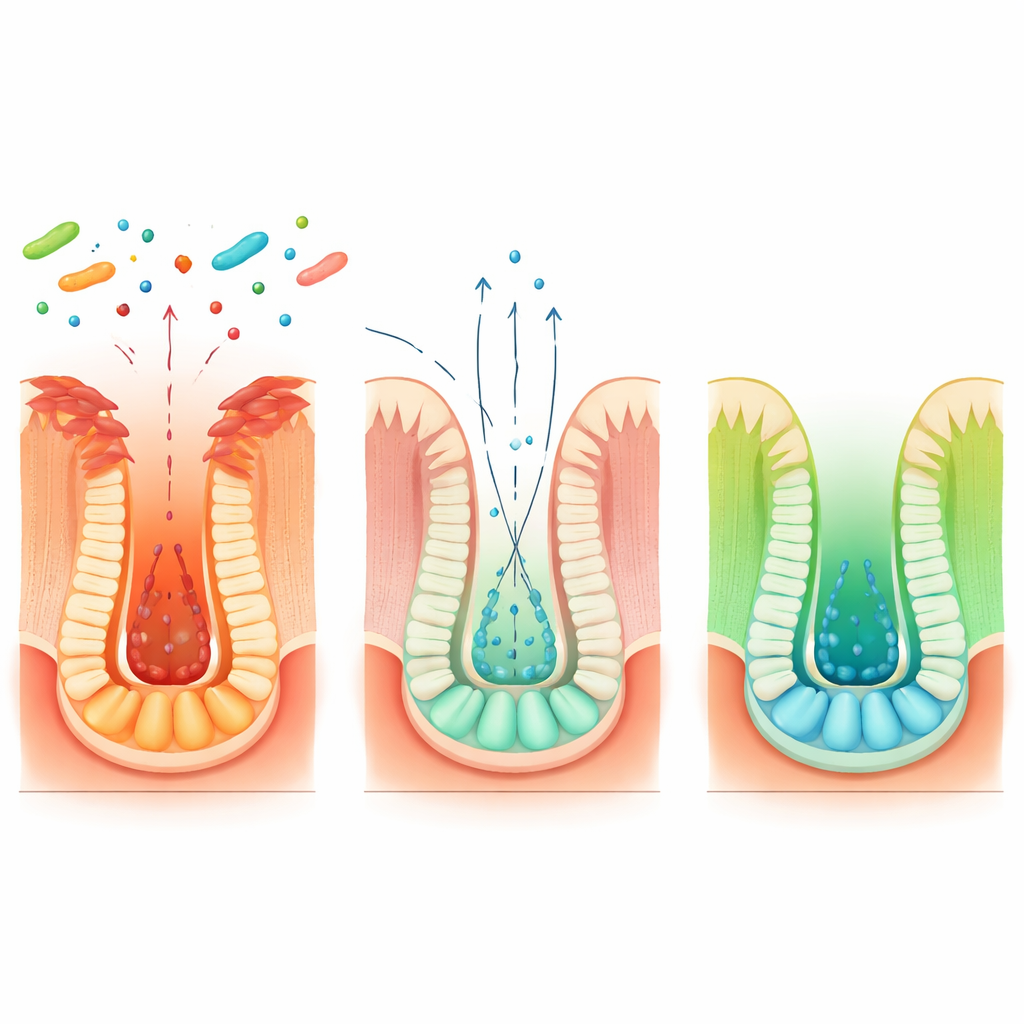
O que isso significa para terapias intestinais futuras
Para testar a importância da dieta, os pesquisadores colocaram camundongos em um regime sem triptofano que reduziu drasticamente a produção de compostos indólicos. Esses animais sofreram colite mais grave e respostas de células-tronco mais fracas. Notavelmente, fornecer ácido indol-3-propiónico diretamente, ou reintroduzir o triptofano juntamente com as bactérias engenheiradas, restaurou a cicatrização e a ativação das células-tronco. Em conjunto, o trabalho delineia um eixo “microbiota–metabólito–célula-tronco”: o triptofano dietético é processado por uma equipe de micróbios intestinais em um sinal que induz as células intestinais a gerar beta-hidroxibutirato, que então ativa células-tronco de reserva via Hopx para reconstruir o revestimento danificado. Para os pacientes, isso sugere uma nova classe de terapias — usando micróbios, enzimas ou metabólitos cuidadosamente escolhidos, juntamente com a dieta — para encorajar suavemente as próprias equipes de reparo do intestino em vez de simplesmente reprimir a resposta imune.
Citação: Zhang, Y., Meng, J., Tu, S. et al. A microbiota-IPA axis facilitates intestinal stem cell-mediated regeneration in colitis through a Hopx-associated program. Nat Commun 17, 3196 (2026). https://doi.org/10.1038/s41467-026-70062-6
Palavras-chave: microbioma intestinal, doença inflamatória intestinal, células-tronco intestinais, metabólitos microbianos, cicatrização mucosal