Clear Sky Science · zh
VRAC在肠上皮细胞中协调营养吸收与抗菌防御之间的权衡以抵御炎症
肠道平衡为何重要
我们的肠道面临持续的两难:既要从食物中吸收营养,又要抵御有害微生物。本研究探讨了一种在肠上皮细胞中鲜为人知的通道——VRAC——如何管理这一权衡。当该通道功能失调时,肠道的微妙平衡会偏向过度防御,导致营养处理不良、微生物群失衡以及类似炎症性肠病的慢性炎症。
肠上皮细胞的日常工作
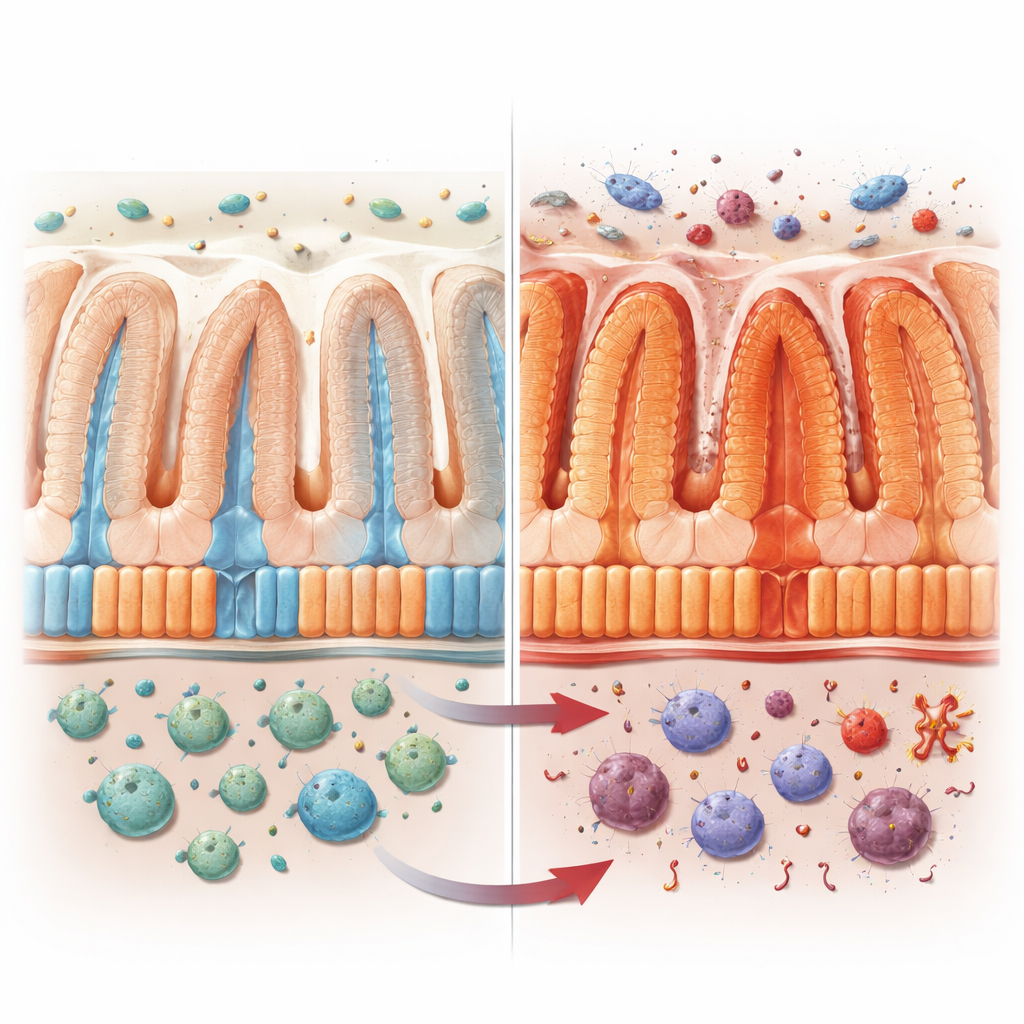
肠道内表面由肠上皮细胞(enterocytes)覆盖,这些细胞构成了肠道屏障的主要部分。这些细胞并非完全相同。位于皱襞深处的细胞偏重防御,会产生抗菌物质;而靠近表面的细胞则专门负责吸收糖类、脂肪、维生素和其他营养物质。它们共同构成一种“分区”化的装配线,既保障机体营养又维持防护。研究者旨在弄清VRAC——一种对体积变化敏感的离子通道——在这种劳动分工中,尤其是在炎症期间,发挥了怎样的作用。
通道失灵时会发生什么
为了探明VRAC的作用,研究人员构建了仅在肠上皮细胞中缺失其关键组成成分LRRC8A的老鼠模型。在正常条件下,这些动物看起来健康。但当暴露于模拟结肠炎或促使结肠癌发生的化学物质时,它们体重下降更多,结肠更短且损伤更严重,肿瘤数量也多于同窝的对照组。它们的肠道屏障出现渗漏,细胞间紧密连接受破坏,与炎症和抗菌防御相关的基因显著上调,而负责营养与脂质转运的基因则下降。将VRAC从免疫细胞中去除并未产生相同效应,指向肠上皮细胞为关键位点。
从吸收转向防御的变化
单细胞分析和迷你“肠样”类器官揭示了组织内部的变化。没有VRAC时,肠上皮细胞沿隐窝到表面的分化未能正常成熟。与营养吸收相关的细胞,尤其是表面区域的细胞,被耗损,而位于基底的防御型细胞则扩增。这种重编程损害了营养处理:来自VRAC缺失小鼠的类器官对脂质和葡萄糖的吸收减少。此次转变的一个核心牺牲品是维生素A代谢。将膳食维生素A转化为信号分子视黄酸的酶类显著减少,总体视黄醛脱氢酶(retinoic dehydrogenase)活性下降。
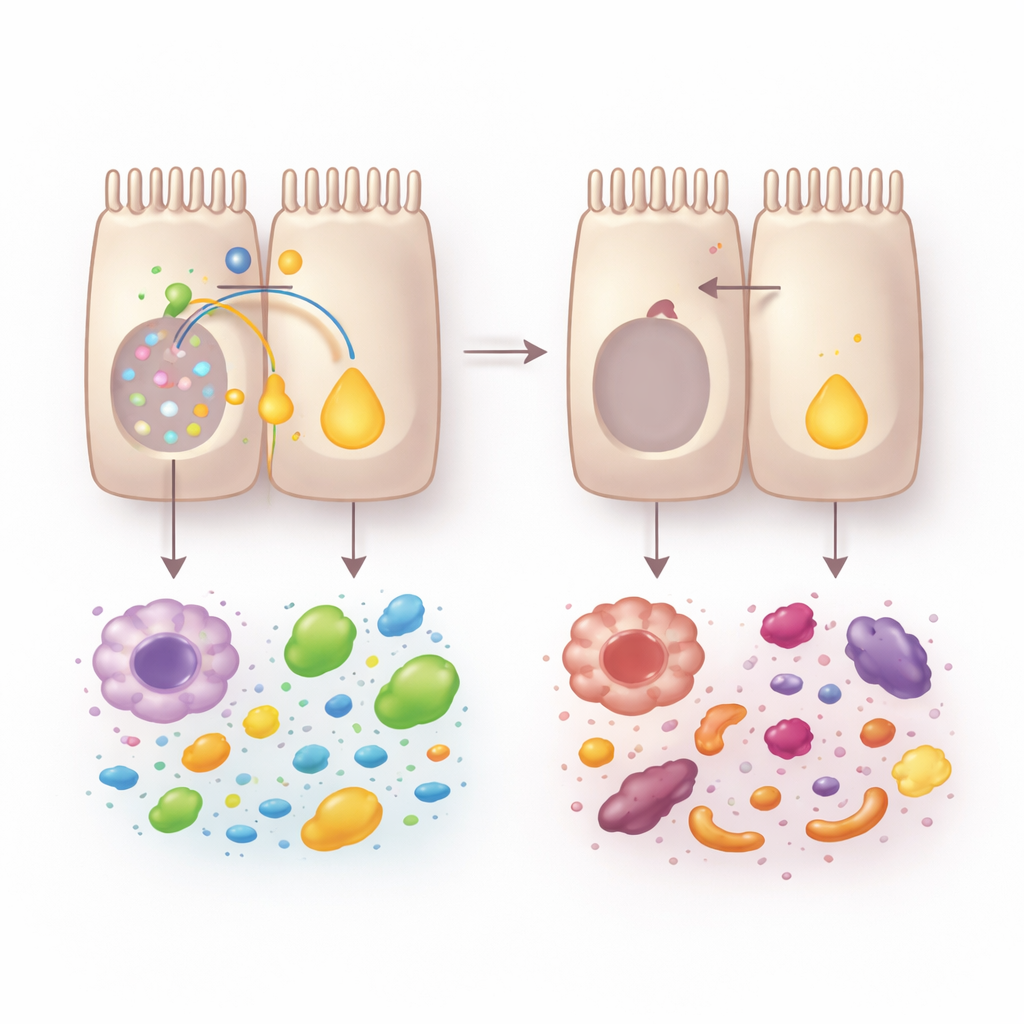
维生素A信号与有益微生物的救援
鉴于视黄酸成为关键通路,团队测试了恢复视黄酸能否逆转损伤。在结肠炎诱发前给予全反式视黄酸(all-trans retinoic acid)可减少体重下降和结肠损伤,恢复维生素A处理酶的表达,并改善成熟营养吸收型肠上皮细胞的数量。它还恢复了产生IL-17和IL-22的有益免疫细胞,这些分子对修复肠道上皮至关重要。与此同时,VRAC的丧失改变了微生物组:多样性下降,有益的乳酸杆菌(Lactobacillus)种类减少。这些微生物学变化十分重要:通过同屋饲养使微生物均衡或用抗生素抹除微生物后,正常与VRAC缺失动物之间的差异大部分消失。将VRAC缺失小鼠的粪便移植到健康受体中会加重结肠炎,而补充特定的乳酸杆菌菌株则促进维生素A代谢、使抗菌肽水平正常化并恢复保护性免疫细胞。
对肠道健康的意义
总体而言,该研究表明肠上皮细胞中的VRAC像一个调节器,控制肠道在吸收营养与抵御微生物之间投入的资源。当VRAC缺失时,系统会锁定在高防御模式:抗菌活性和炎症上升,营养吸收与维生素A信号下降,有益细菌被压缩。通过恢复视黄酸或重新引入有益的乳酸杆菌,研究者能够在小鼠中重新平衡该系统并缓解疾病。对于炎症性肠病等人群,这些发现凸显了肠上皮自身离子通道——以及它们与膳食来源维生素和益生菌的联系——作为未来治疗的有希望的干预点。
引用: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
关键词: 炎症性肠病, 肠上皮, 视黄酸, 肠道微生物组, 益生菌