Clear Sky Science · it
VRAC coordina il compromesso tra assorbimento di nutrienti e difesa antimicrobica negli enterociti contro l’infiammazione
Perché l’equilibrio dell’intestino conta
I nostri intestini affrontano un dilemma costante: devono assorbire i nutrienti dal cibo e allo stesso tempo respingere i microrganismi dannosi. Questo studio esplora come una porta poco conosciuta nelle cellule intestinali, chiamata VRAC, contribuisca a gestire questo compromesso. Quando questa porta non funziona, il delicato equilibrio intestinale si sposta verso una difesa eccessiva, scarso trattamento dei nutrienti, disturbo del microbiota e infiammazione cronica simile alla malattia infiammatoria intestinale.
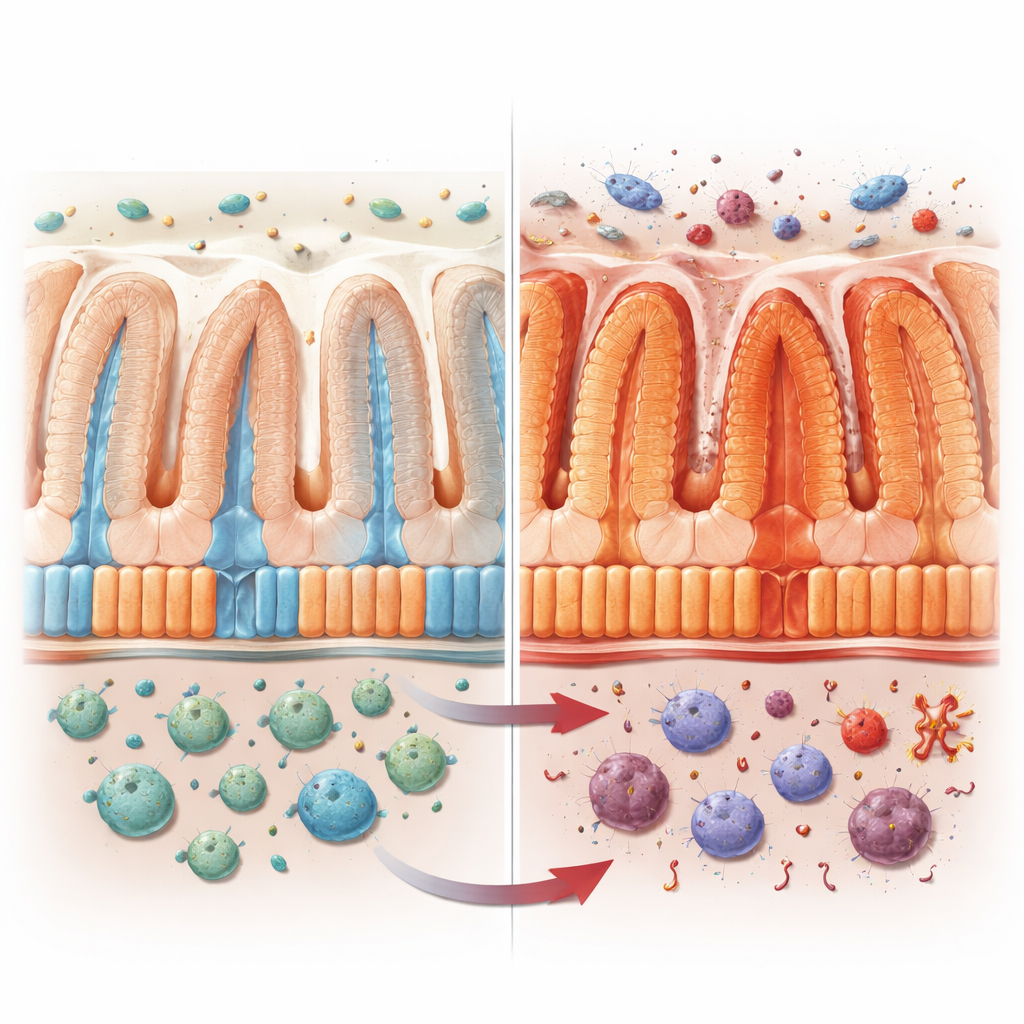
Il lavoro quotidiano delle cellule della mucosa intestinale
La superficie interna dell’intestino è rivestita da enterociti, cellule che costituiscono la maggior parte della barriera intestinale. Queste cellule non sono tutte uguali. Quelle in profondità nelle pieghe si concentrano sulla difesa, producendo sostanze antimicrobiche, mentre quelle più vicine alla superficie sono specializzate nell’assorbimento di zuccheri, grassi, vitamine e altri nutrienti. Insieme formano una catena di montaggio “zonata” che mantiene il corpo sia nutrito che protetto. Gli autori hanno voluto capire come VRAC, un canale ionico sensibile al volume in queste cellule, contribuisca a questa divisione del lavoro, specialmente durante l’infiammazione.
Cosa succede quando la porta fallisce
Per sondare il ruolo di VRAC, i ricercatori hanno generato topi privi del suo componente chiave, LRRC8A, solo nelle cellule dell’epitelio intestinale. In condizioni normali questi animali erano apparentemente sani. Ma quando esposti a sostanze chimiche che imitano la colite o promuovono il cancro del colon, persero più peso, ebbero colon più corti e danneggiati e svilupparono più tumori rispetto ai loro fratelli normali. Le loro barriere intestinali risultarono più permeabili, le giunzioni strette tra le cellule furono disturbate e i geni legati all’infiammazione e alle difese antimicrobiche aumentarono, mentre i geni per il trasporto di nutrienti e grassi diminuirono. La rimozione di VRAC dalle cellule immunitarie non produsse gli stessi effetti, identificando l’epitelio intestinale come il sito critico.
Dal nutrire al combattere
Analisi a singola cellula e organoidi miniaturizzati a “intestino in provetta” hanno rivelato cosa stava accadendo nel tessuto. Senza VRAC, gli enterociti non maturarono correttamente lungo l’asse dalla criptia alla superficie. Le cellule associate all’assorbimento di nutrienti, specialmente in superficie, risultarono deplete, mentre le cellule orientate alla difesa alla base si espandevano. Questo riprogrammamento danneggiò la gestione dei nutrienti: gli organoidi dei topi privi di VRAC assorbirono meno lipidi e glucosio. Una vittima centrale di questo cambiamento fu il metabolismo della vitamina A. Gli enzimi che convertono la vitamina A alimentare in acido retinoico — una molecola segnale che sostiene l’identità degli enterociti, la riparazione tissutale e l’equilibrio immunitario — risultarono fortemente ridotti, e l’attività complessiva delle retino-deidrogenasi calò.
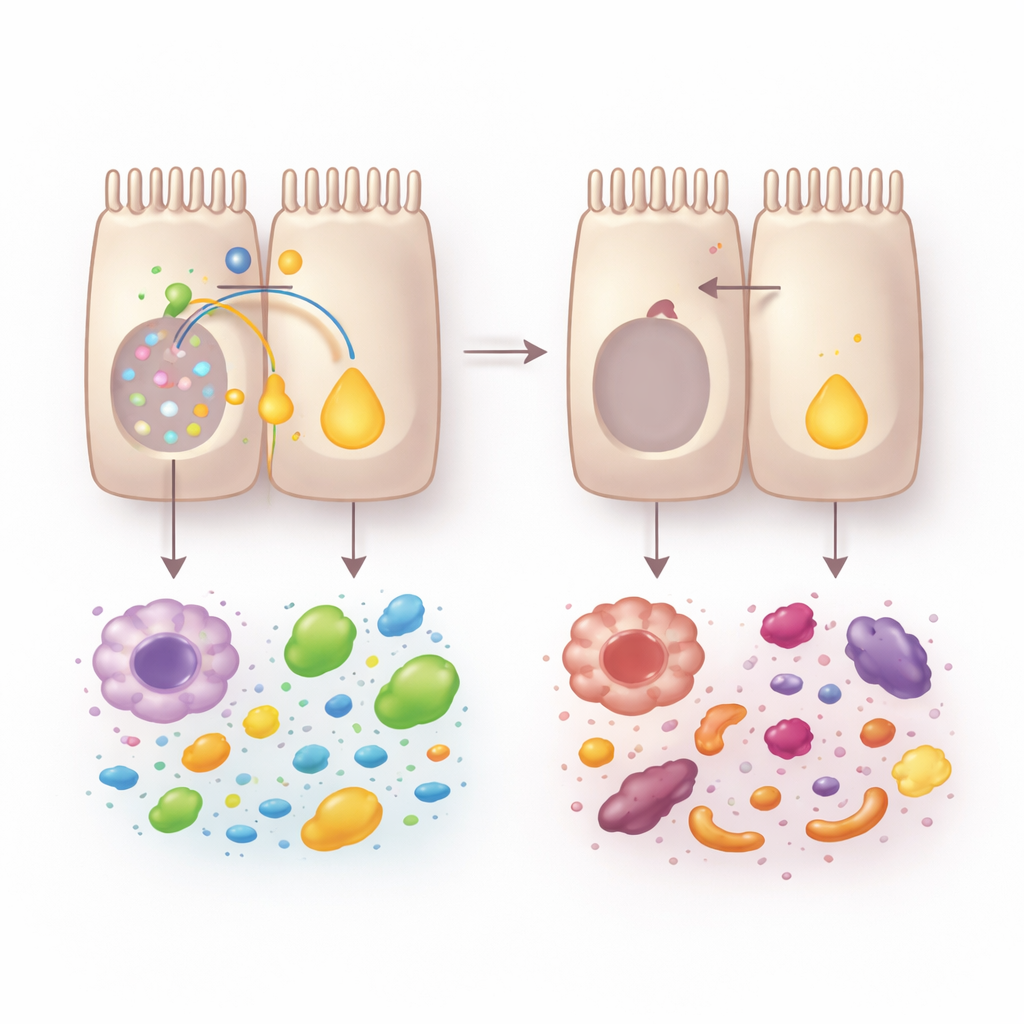
I segnali della vitamina A e i microbi amici in soccorso
Poiché l’acido retinoico emerse come una via chiave, il gruppo ha testato se il suo ripristino potesse contrastare il danno. Somministrare ai topi acido retinoico all-trans prima della colite ridusse la perdita di peso e il danno al colon, riattivò gli enzimi per il metabolismo della vitamina A e migliorò la presenza di enterociti maturi assorbenti. Ripristinò inoltre cellule immunitarie utili che producono IL-17 e IL-22, molecole cruciali per la riparazione della mucosa intestinale. Allo stesso tempo, la perdita di VRAC alterò il microbiota: la diversità diminuì e le specie benefiche di Lactobacillus calarono. Questi cambiamenti microbici si rivelarono importanti; uniformare il microbiota ospitando insieme i topi o azzerandolo con antibiotici cancellò gran parte delle differenze tra animali normali e privi di VRAC. Trapiantare feci da topi privi di VRAC in recipienti sani peggiorò la colite, mentre l’integrazione di specifici ceppi di Lactobacillus migliorò il metabolismo della vitamina A, normalizzò i livelli di peptidi antimicrobici e ripristinò le cellule immunitarie protettive.
Cosa significa per la salute intestinale
Nel complesso, lo studio mostra che VRAC nelle cellule dell’epitelio intestinale funziona come un reostato, modulando quanto sforzo l’intestino investe nell’assorbire nutrienti rispetto a combattere i microrganismi. Quando VRAC manca, il sistema si blocca in modalità alta difesa: l’attività antimicrobica e l’infiammazione aumentano, l’assorbimento dei nutrienti e la segnalazione della vitamina A calano, e i batteri benefici vengono spinti via. Ripristinando l’acido retinoico o reintroducendo Lactobacillus amici, i ricercatori sono riusciti a riequilibrare questo sistema e alleviare la malattia nei topi. Per le persone con condizioni come la malattia infiammatoria intestinale, questi risultati mettono in luce i canali ionici della mucosa — e i loro legami con vitamine derivate dalla dieta e probiotici — come leve promettenti per terapie future.
Citazione: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Parole chiave: malattia infiammatoria intestinale, epitelio intestinale, acido retinoico, microbioma intestinale, probiotici