Clear Sky Science · pt
VRAC coordena o equilíbrio entre absorção de nutrientes e defesa antimicrobiana em enterócitos contra a inflamação
Por que o equilíbrio do intestino importa
Nosso intestino enfrenta um dilema constante: precisa absorver nutrientes dos alimentos ao mesmo tempo em que afasta micróbios nocivos. Este estudo investiga como uma porta pouco conhecida nas células intestinais, chamada VRAC, ajuda a gerir esse trade-off. Quando essa porta funciona mal, o equilíbrio delicado do intestino desloca-se em direção a uma defesa excessiva, manuseio deficiente de nutrientes, perturbação da microbiota e inflamação crônica semelhante à doença inflamatória intestinal.
O trabalho cotidiano das células do revestimento intestinal
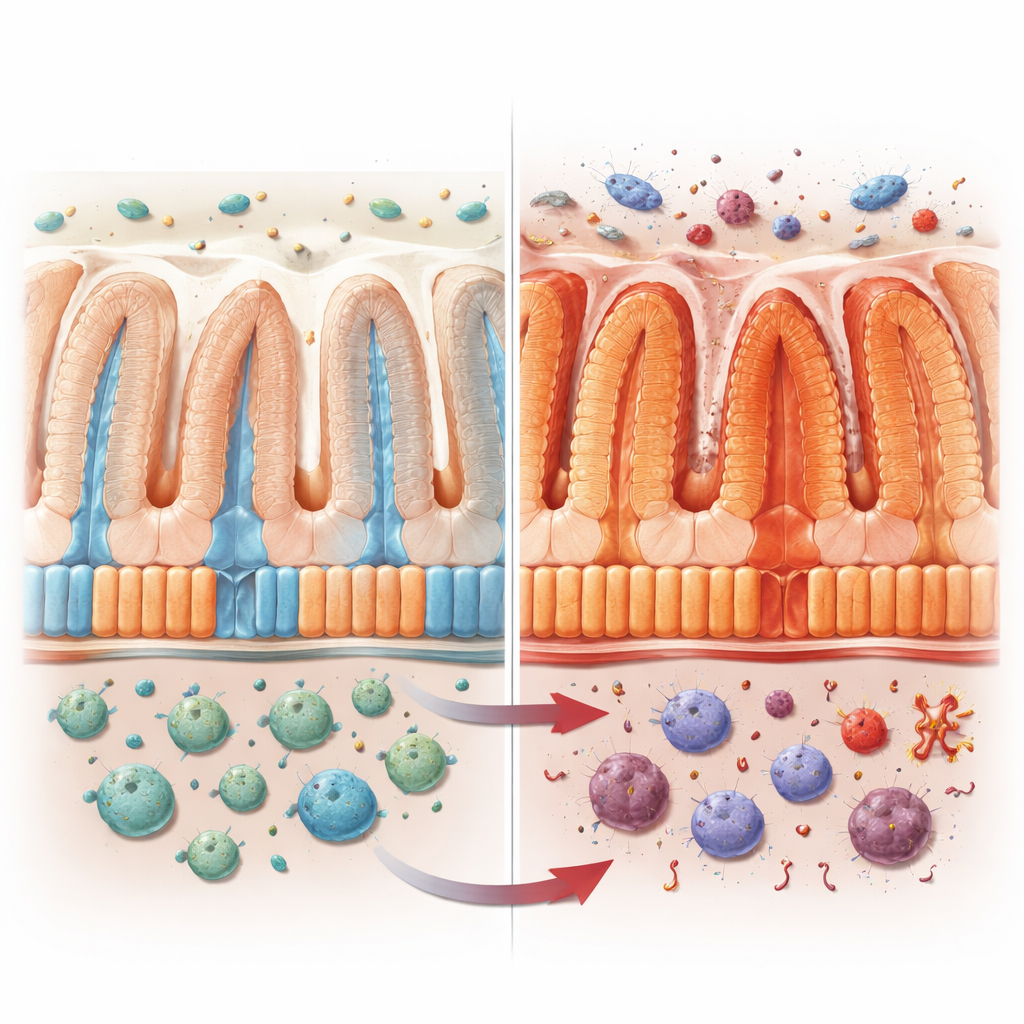
A superfície interna do intestino é revestida por enterócitos, células que compõem a maior parte da barreira intestinal. Essas células não são todas iguais. As que ficam nas pregas profundas concentram-se na defesa, produzindo substâncias antimicrobianas, enquanto as mais próximas da superfície se especializam em absorver açúcares, gorduras, vitaminas e outros nutrientes. Juntas, formam uma linha de montagem “zonada” que mantém o corpo nutrido e protegido. Os autores buscaram entender como o VRAC, um canal iônico sensível ao volume nessas células, contribui para essa divisão de trabalho, especialmente durante a inflamação.
O que acontece quando a porta falha
Para sondar o papel do VRAC, os pesquisadores produziram camundongos que não possuíam seu componente chave, LRRC8A, apenas nas células do revestimento intestinal. Em condições normais esses animais pareciam saudáveis. Mas quando expostos a produtos químicos que imitam colite ou que promovem câncer de cólon, perderam mais peso, tiveram cólons mais curtos e danificados e desenvolveram mais tumores que seus irmãos normais. Suas barreiras intestinais ficaram permeáveis, as junções de vedação entre as células foram interrompidas, e genes ligados à inflamação e às defesas antimicrobianas aumentaram, enquanto genes de transporte de nutrientes e gorduras caíram. Remover o VRAC de células imunológicas não produziu os mesmos efeitos, apontando o revestimento intestinal como o local crítico.
Passando de alimentar para combater
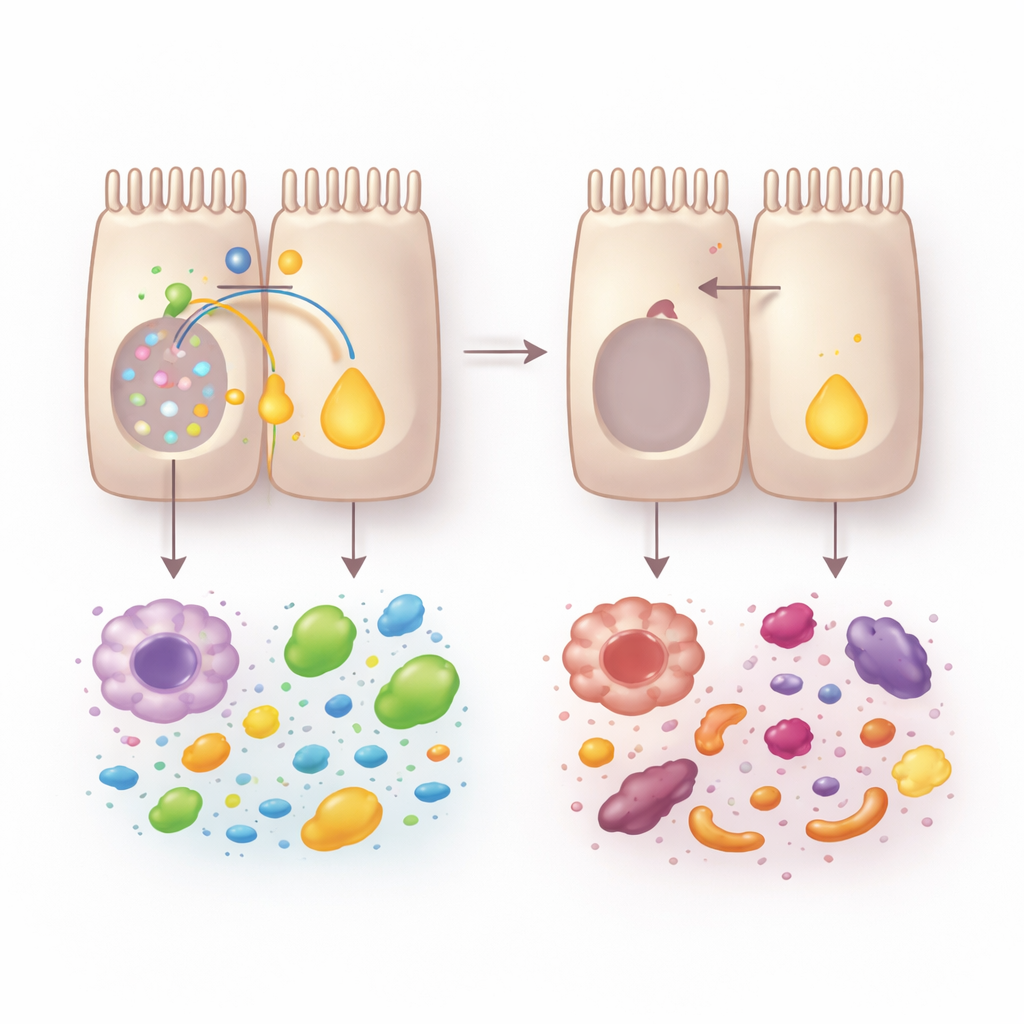
Análises de célula única e organoides em miniatura revelaram o que acontecia dentro do tecido. Sem VRAC, os enterócitos não amadureceram corretamente ao longo do eixo das criptas até a superfície. Células associadas à captação de nutrientes, especialmente na superfície, foram reduzidas, enquanto células orientadas à defesa na base se expandiram. Essa reconfiguração prejudicou o processamento de nutrientes: organoides de camundongos deficientes em VRAC absorveram menos lipídio e glicose. Uma vítima central dessa mudança foi o processamento da vitamina A. Enzimas que convertem a vitamina A dietética em ácido retinoico — uma molécula sinalizadora que sustenta a identidade dos enterócitos, a reparação tecidual e o equilíbrio imune — foram fortemente reduzidas, e a atividade geral da retinoaldeído desidrogenase caiu.
Sinais de vitamina A e micróbios benéficos salvam o dia
Como o ácido retinoico surgiu como via chave, a equipe testou se restaurá-lo poderia contrabalançar os danos. Administrar ácido retinoico todo-trans aos camundongos antes da colite reduziu a perda de peso e lesão do cólon, reativou enzimas de processamento da vitamina A e melhorou a presença de enterócitos maduros absorventes de nutrientes. Também restaurou células imunes úteis que produzem IL-17 e IL-22, moléculas cruciais para reparar o revestimento intestinal. Ao mesmo tempo, a perda de VRAC alterou a microbiota: a diversidade caiu e espécies benéficas de Lactobacillus diminuíram. Essas mudanças microbianas mostraram-se importantes; igualar a microbiota por coabitação dos animais ou eliminá-la com antibióticos apagou grande parte das diferenças entre animais normais e deficientes em VRAC. Transplantar fezes de camundongos deficientes em VRAC para recipientes saudáveis piorou a colite, enquanto suplementar cepas específicas de Lactobacillus impulsionou o metabolismo da vitamina A, normalizou níveis de peptídeos antimicrobianos e reativou células imunes protetoras.
O que isso significa para a saúde intestinal
No conjunto, o estudo mostra que o VRAC nas células do revestimento intestinal atua como um reostato, ajustando quanto esforço o intestino dedica a absorver nutrientes versus combater micróbios. Quando o VRAC está ausente, o sistema trava em modo de alta defesa: atividade antimicrobiana e inflamação aumentam, absorção de nutrientes e sinalização de vitamina A caem, e bactérias benéficas são suprimidas. Ao restaurar o ácido retinoico ou reintroduzir Lactobacillus benéficos, os pesquisadores conseguiram reequilibrar esse sistema e aliviar a doença em camundongos. Para pessoas com condições como a doença inflamatória intestinal, esses achados destacam os canais iônicos do próprio revestimento intestinal — e suas conexões com vitaminas derivadas da dieta e probióticos — como alavancas promissoras para futuras terapias.
Citação: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Palavras-chave: doença inflamatória intestinal, epitélio intestinal, ácido retinoico, microbioma intestinal, probióticos