Clear Sky Science · fr
Le canal VRAC coordonne le compromis entre l’absorption des nutriments et la défense antimicrobienne des entérocytes contre l’inflammation
Pourquoi l’équilibre intestinal est crucial
Nos intestins font face à un dilemme permanent : ils doivent absorber les nutriments issus des aliments tout en repoussant les microbes nuisibles. Cette étude examine comment un portillon peu connu des cellules intestinales, nommé VRAC, aide à gérer ce compromis. Lorsque ce portillon dysfonctionne, l’équilibre délicat de l’intestin bascule vers une défense excessive, une mauvaise gestion des nutriments, un dérangement du microbiote et une inflammation chronique rappelant la maladie inflammatoire de l’intestin.
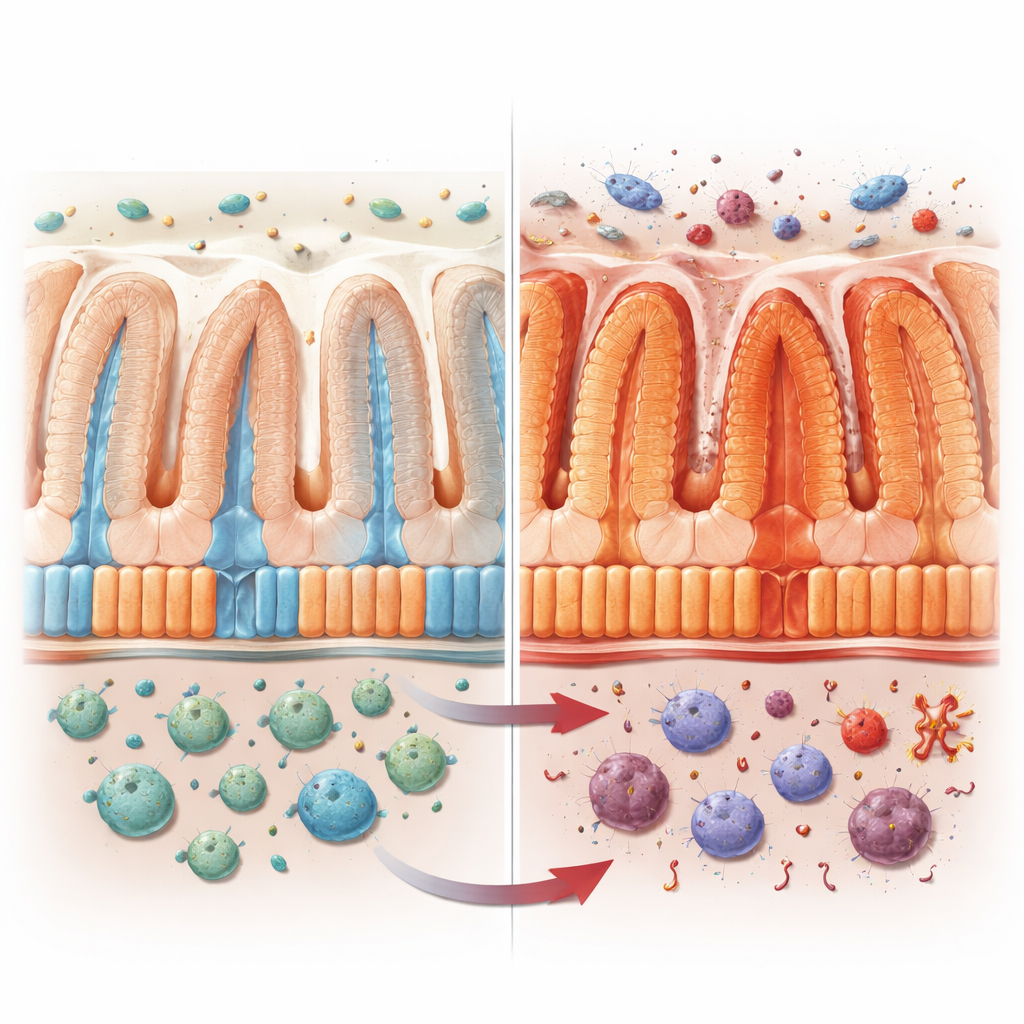
Le travail quotidien des cellules de la muqueuse intestinale
La surface interne de l’intestin est tapissée d’entérocytes, des cellules qui constituent la majeure partie de la barrière intestinale. Ces cellules ne sont pas toutes identiques. Celles situées au fond des cryptes se concentrent sur la défense, produisant des substances antimicrobiennes, tandis que celles plus proches de la surface se spécialisent dans l’absorption des sucres, des lipides, des vitamines et d’autres nutriments. Ensemble, elles forment une chaîne de production « zonée » qui maintient à la fois la nutrition et la protection de l’organisme. Les auteurs ont cherché à comprendre comment VRAC, un canal ionique sensible au volume dans ces cellules, contribue à cette division du travail, en particulier lors de l’inflammation.
Que se passe-t-il quand le portillon échoue
Pour sonder le rôle de VRAC, les chercheurs ont généré des souris dépourvues de sa composante clé, LRRC8A, uniquement dans les cellules de la muqueuse intestinale. En conditions normales, ces animaux paraissaient en bonne santé. Mais lorsqu’ils ont été exposés à des produits chimiques reproduisant la colite ou favorisant le cancer du côlon, ils ont perdu plus de poids, présenté des côlons plus courts et plus endommagés, et développé davantage de tumeurs que leurs congénères normaux. Leur barrière intestinale fuyait, les jonctions serrées entre cellules étaient perturbées, et les gènes liés à l’inflammation et aux défenses antimicrobiennes étaient fortement augmentés, tandis que ceux impliqués dans le transport des nutriments et des lipides diminuaient. La suppression de VRAC dans les cellules immunitaires n’a pas produit les mêmes effets, ce qui identifie la muqueuse intestinale comme le site critique.
Passer de l’alimentation à la défense
Des analyses mono-cellulaires et des organoïdes intestinaux miniatures ont révélé ce qui se passait au sein du tissu. Sans VRAC, les entérocytes ne parvenaient pas à maturer correctement suivant l’axe de la crypte vers la surface. Les cellules associées à l’absorption des nutriments, surtout en surface, étaient épuisées, tandis que les cellules orientées vers la défense à la base se développaient. Cette réorganisation a nui à la prise en charge des nutriments : les organoïdes issus de souris déficientes en VRAC absorbaient moins de lipides et de glucose. Une victime centrale de ce changement fut le métabolisme de la vitamine A. Les enzymes qui convertissent la vitamine A alimentaire en acide rétinoïque — une molécule de signalisation qui soutient l’identité des entérocytes, la réparation tissulaire et l’équilibre immunitaire — étaient fortement réduites, et l’activité globale des rétino-déshydrogénases chutait.
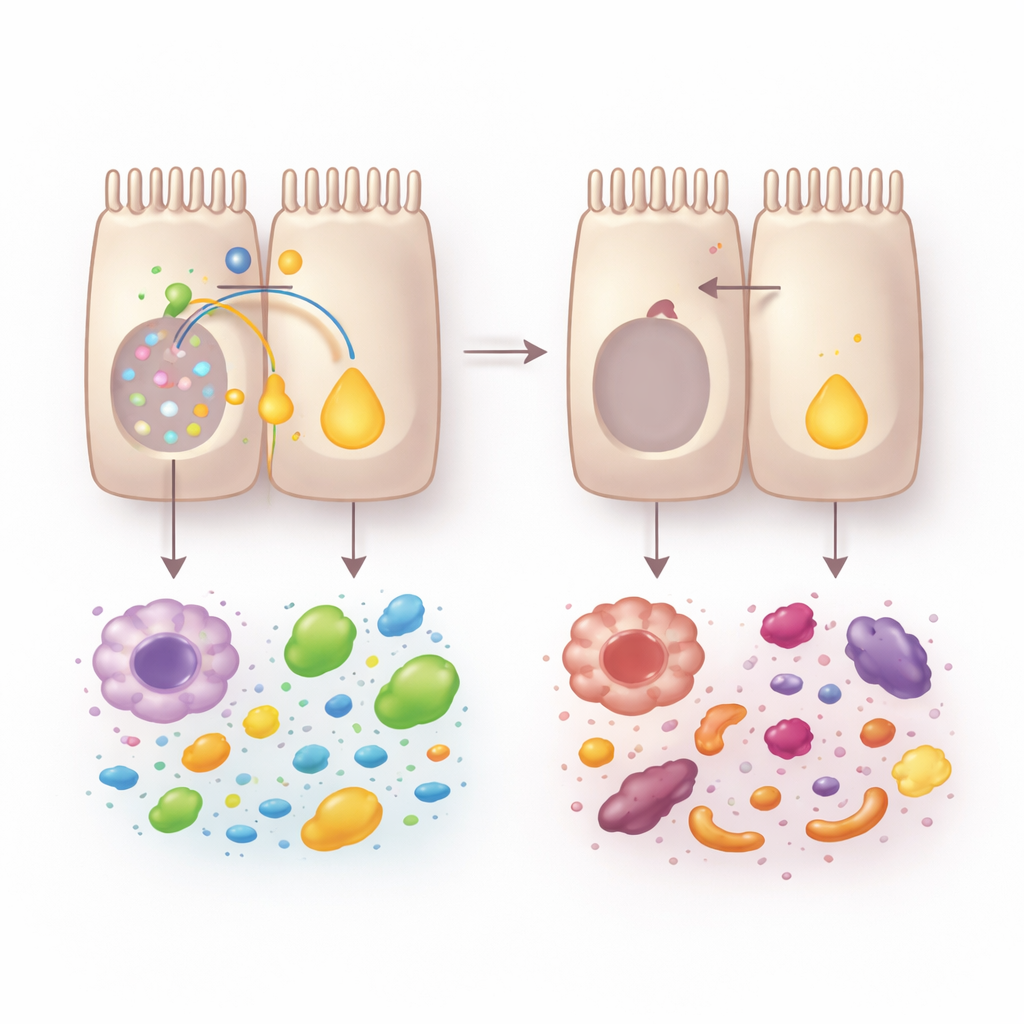
Les signaux de la vitamine A et les microbes amis viennent en aide
Parce que l’acide rétinoïque est apparu comme une voie clé, l’équipe a testé si sa restauration pouvait contrer les dégâts. L’administration d’acide rétinoïque tout-trans avant la colite a réduit la perte de poids et les lésions du côlon, ravivé les enzymes de traitement de la vitamine A et amélioré la présence d’entérocytes matures absorbant les nutriments. Elle a aussi rétabli des cellules immunitaires utiles produisant IL-17 et IL-22, des molécules cruciales pour la réparation de la muqueuse intestinale. Parallèlement, la perte de VRAC a modifié le microbiote : la diversité a chuté et les espèces bénéfiques de Lactobacillus ont diminué. Ces changements microbien se sont révélés importants ; homogénéiser le microbiote en co‑logement ou l’effacer avec des antibiotiques a estompé une grande partie de la différence entre souris normales et déficientes en VRAC. La transplantation de selles de souris déficientes en VRAC vers des receveurs sains a aggravé la colite, tandis que la supplémentation en souches spécifiques de Lactobacillus a stimulé le métabolisme de la vitamine A, normalisé les niveaux de peptides antimicrobiens et ravivé les cellules immunitaires protectrices.
Ce que cela signifie pour la santé intestinale
Dans l’ensemble, l’étude montre que VRAC dans les cellules de la muqueuse intestinale agit comme un rhéostat, modulant l’effort que l’intestin consacre à l’absorption des nutriments versus la lutte contre les microbes. Quand VRAC manque, le système se bloque en mode haute défense : l’activité antimicrobienne et l’inflammation augmentent, l’absorption des nutriments et la signalisation de la vitamine A diminuent, et les bactéries bénéfiques sont repoussées. En restaurant l’acide rétinoïque ou en réintroduisant des Lactobacillus bienfaisants, les chercheurs ont pu rééquilibrer ce système et atténuer la maladie chez la souris. Pour les personnes souffrant de pathologies comme la maladie inflammatoire de l’intestin, ces résultats mettent en lumière les canaux ioniques de la muqueuse intestinale — et leurs liens avec les vitamines d’origine alimentaire et les probiotiques — comme des leviers prometteurs pour de futures thérapies.
Citation: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Mots-clés: maladie inflammatoire de l’intestin, épithélium intestinal, acide rétinoïque, microbiote intestinal, probiotiques