Clear Sky Science · de
VRAC koordiniert den Kompromiss zwischen Nährstoffaufnahme und antimikrobiellem Schutz in Enterozyten bei Entzündungen
Warum der Balanceakt des Darms wichtig ist
Unser Darm steht vor einem ständigen Dilemma: Er muss Nährstoffe aus der Nahrung aufnehmen und gleichzeitig schädliche Mikroben abwehren. Diese Studie untersucht, wie ein wenig bekanntes Tor in den Darmschleimhautzellen, genannt VRAC, dabei hilft, diesen Kompromiss zu steuern. Wenn dieses Tor nicht richtig funktioniert, kippt das empfindliche Gleichgewicht in Richtung übertriebener Abwehr, schlechter Nährstoffverarbeitung, gestörter Mikrobiota und chronischer Entzündung, ähnlich wie bei entzündlichen Darmerkrankungen.
Die tägliche Arbeit der Darmschleimhautzellen
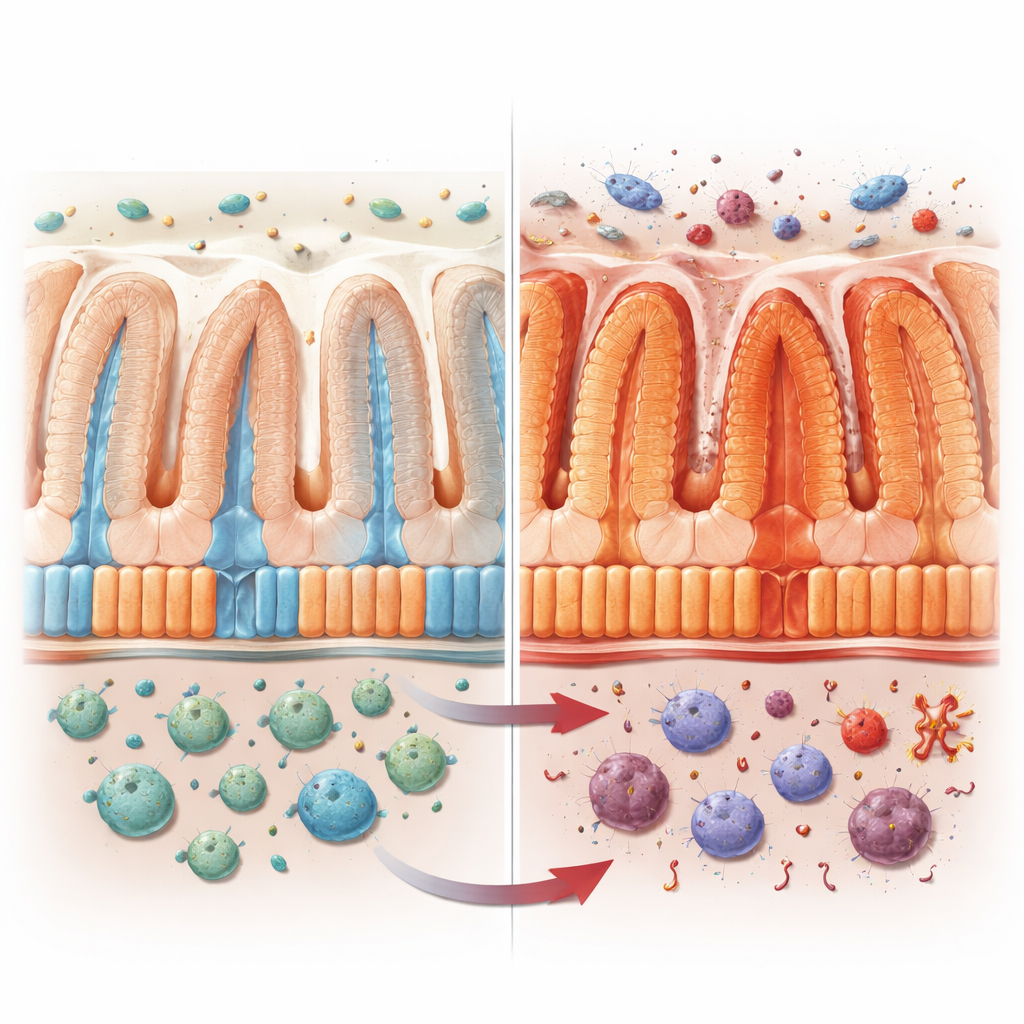
Die Innenfläche des Darms ist mit Enterozyten ausgekleidet, Zellen, die den Großteil der Darmbarriere bilden. Diese Zellen sind nicht alle gleich. Die tief in den Falten liegenden Zellen konzentrieren sich auf Abwehr und produzieren antimikrobielle Substanzen, während die näher an der Oberfläche liegenden auf die Aufnahme von Zuckern, Fetten, Vitaminen und anderen Nährstoffen spezialisiert sind. Gemeinsam bilden sie eine „zonierte“ Produktionskette, die den Körper sowohl versorgt als auch schützt. Die Autoren wollten verstehen, wie VRAC, ein volumen-sensitiver Ionenkanal in diesen Zellen, zu dieser Arbeitsteilung beiträgt, besonders während Entzündungen.
Was passiert, wenn das Tor ausfällt
Um die Rolle von VRAC zu untersuchen, erzeugten die Forscher Mäuse, denen die Schlüsselkomponente LRRC8A nur in den Darmschleimhautzellen fehlte. Unter normalen Bedingungen wirkten diese Tiere gesund. Wurden sie jedoch Chemikalien ausgesetzt, die Kolitis nachahmen oder Darmkrebs fördern, verloren sie mehr Gewicht, hatten kürzere und stärker geschädigte Kolons und entwickelten mehr Tumoren als ihre normalen Wurfgeschwister. Ihre Darmbarriere wurde undicht, die Tight Junctions zwischen den Zellen waren gestört, und Gene, die mit Entzündung und antimikrobieller Abwehr verknüpft sind, schossen nach oben, während Gene für Nährstoff- und Fetttransport heruntergingen. Das Entfernen von VRAC aus Immunzellen erzeugte nicht die gleichen Effekte, wodurch die Darmschleimhaut als kritischer Ort identifiziert wurde.
Vom Füttern zum Kämpfen
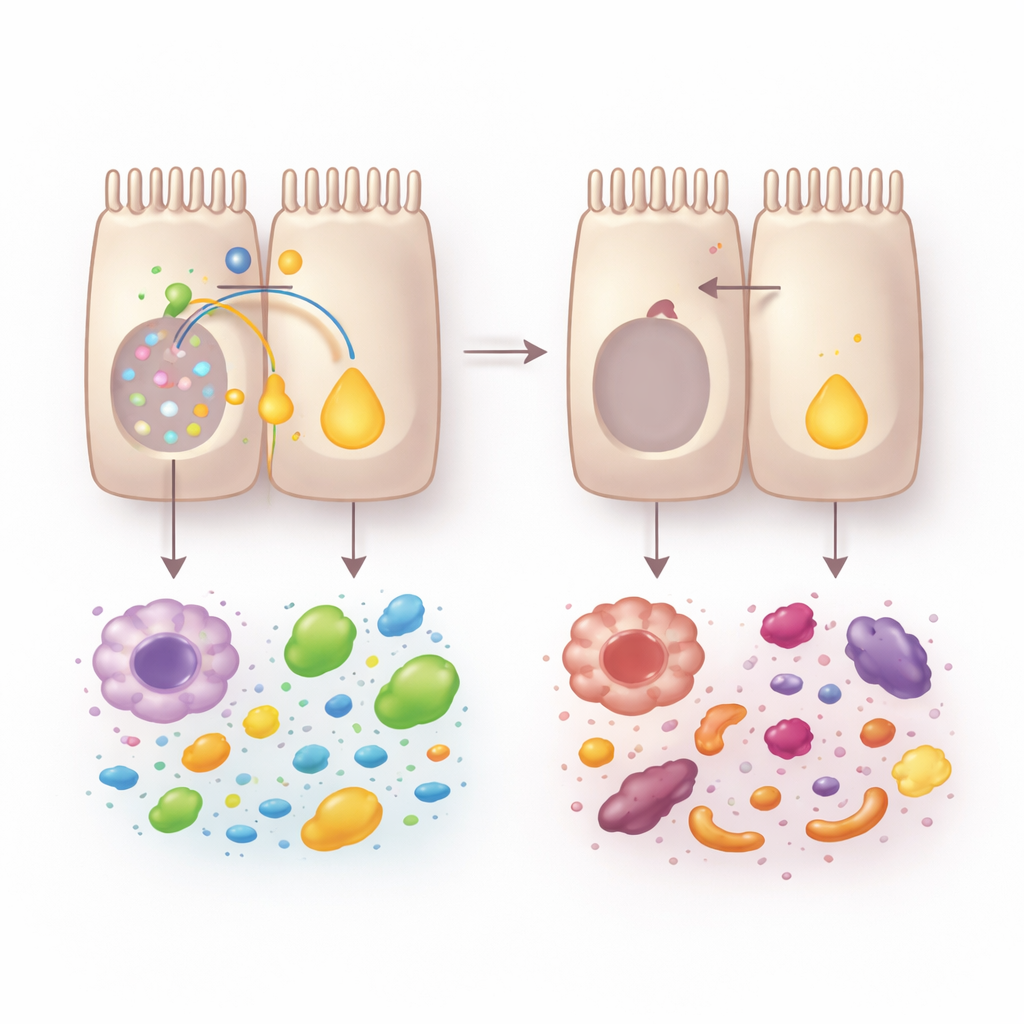
Einzelzellanalysen und miniature „Darm-in-der-Petrischale“-Organoide zeigten, was im Gewebe vorging. Ohne VRAC reiften Enterozyten entlang der Krypten-zu-Oberfläche-Achse nicht richtig aus. Zellen, die mit Nährstoffaufnahme assoziiert sind, besonders an der Oberfläche, gingen zurück, während abwehrorientierte Zellen an der Basis zunahmen. Diese Umstrukturierung schadete der Nährstoffverarbeitung: Organoide aus VRAC-defizienten Mäusen nahmen weniger Lipide und Glukose auf. Ein zentrales Opfer dieses Wechsels war die Verarbeitung von Vitamin A. Enzyme, die Nahrungsvitamin A in Retinsäure — ein Signalstoff, der Enterozytenidentität, Gewebereparatur und Immunbalance unterstützt — umwandeln, waren stark reduziert, und die gesamt Retinoaldehyddehydrogenase-Aktivität fiel.
Vitamin-A-Signale und freundliche Mikroben als Rettung
Da Retinsäure als Schlüsselweg hervorging, prüfte das Team, ob deren Wiederherstellung den Schaden abmildern könnte. Die Gabe von all-trans-Retinsäure vor Kolitis verringerte Gewichtsverlust und Kolonschäden, belebte die Vitamin-A-verarbeitenden Enzyme und verbesserte das Vorkommen reifer, nährstoffaufnehmender Enterozyten. Sie stellte auch hilfreiche Immunzellen wieder her, die IL-17 und IL-22 produzieren — Moleküle, die für die Reparatur der Darmschleimhaut wichtig sind. Gleichzeitig veränderte der Verlust von VRAC die Mikrobiota: Die Diversität nahm ab und nützliche Lactobacillus-Arten gingen zurück. Diese mikrobiellen Veränderungen waren bedeutsam; eine Angleichung der Mikrobiota durch gemeinsames Housing oder deren Entfernen mit Antibiotika beseitigte viele Unterschiede zwischen normalen und VRAC-defizienten Tieren. Die Übertragung von Stuhl aus VRAC-defizienten Mäusen auf gesunde Empfänger verschlechterte die Kolitis, während die Ergänzung bestimmter Lactobacillus-Stämme den Vitamin-A-Stoffwechsel förderte, die Spiegel antimikrobieller Peptide normalisierte und schützende Immunzellen wiederbelebte.
Was das für die Darmgesundheit bedeutet
Insgesamt zeigt die Studie, dass VRAC in Darmschleimhautzellen wie ein Rheostat wirkt und einstellt, wie viel Aufwand der Darm in Nährstoffaufnahme versus Abwehr von Mikroben investiert. Fehlt VRAC, schaltet das System in einen Hochschutzmodus: antimikrobielle Aktivität und Entzündung steigen, Nährstoffaufnahme und Vitamin-A-Signalisierung fallen, und nützliche Bakterien werden verdrängt. Durch die Wiederherstellung von Retinsäure oder das Wiedereinführen freundlicher Lactobacillus-Stämme konnten die Forscher dieses System wieder ins Gleichgewicht bringen und die Krankheit bei Mäusen lindern. Für Menschen mit Erkrankungen wie entzündlichen Darmerkrankungen heben diese Befunde die Ionenkanäle der Darmschleimhaut — und ihre Verknüpfung mit ernährungsabhängigen Vitaminen und Probiotika — als vielversprechende Ansatzpunkte für künftige Therapien hervor.
Zitation: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Schlüsselwörter: entzündliche Darmerkrankung, intestinales Epithel, Retinsäure, Darmmikrobiom, Probiotika