Clear Sky Science · es
VRAC coordina la compensación entre la absorción de nutrientes y la defensa antimicrobiana en los enterocitos frente a la inflamación
Por qué importa el acto de equilibrio del intestino
Nuestros intestinos afrontan un dilema constante: deben absorber nutrientes de los alimentos al tiempo que rechazan microbios perjudiciales. Este estudio explora cómo una puerta poco conocida en las células intestinales, llamada VRAC, ayuda a gestionar ese compromiso. Cuando esta puerta funciona mal, el delicado equilibrio intestinal se inclina hacia una defensa excesiva, un manejo deficiente de los nutrientes, alteraciones en los microbios y una inflamación crónica similar a la de la enfermedad inflamatoria intestinal.
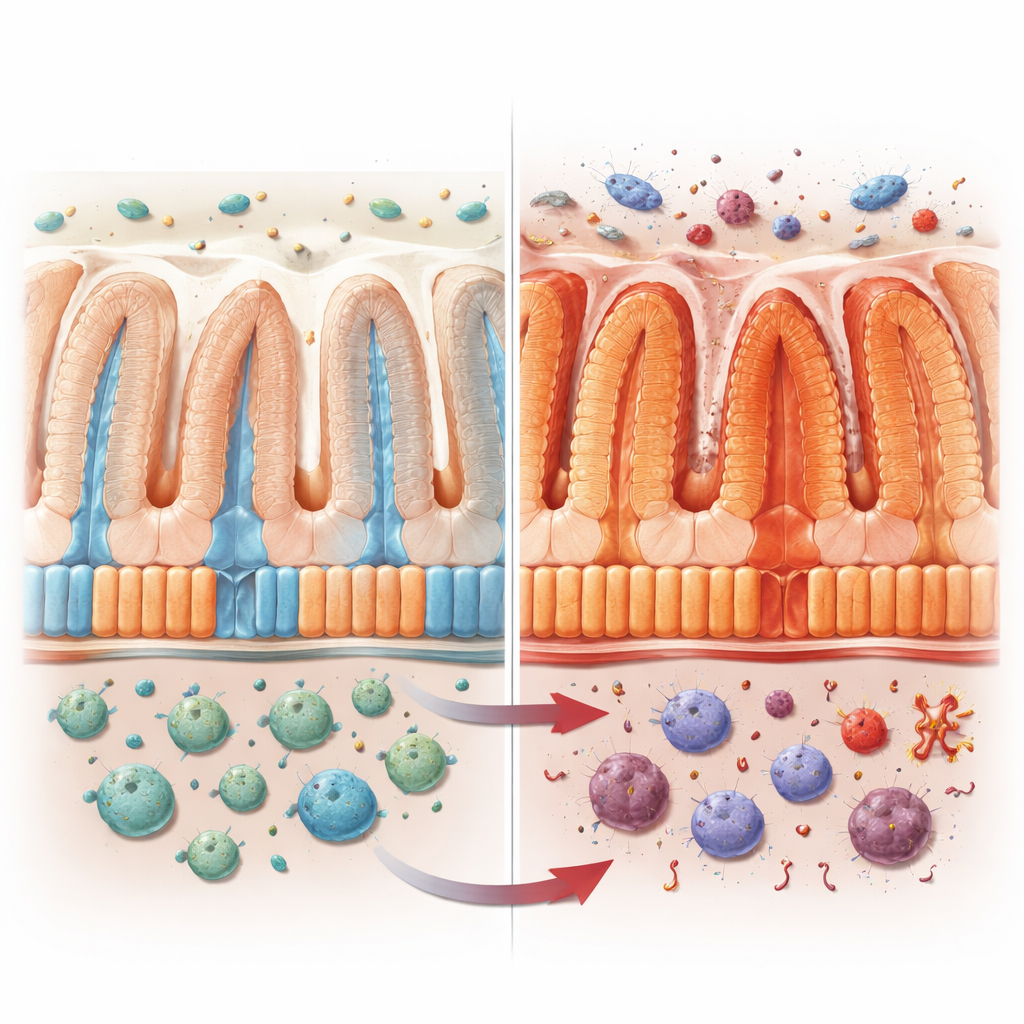
El trabajo cotidiano de las células del revestimiento intestinal
La superficie interna del intestino está revestida por enterocitos, células que constituyen la mayor parte de la barrera intestinal. Estas células no son todas iguales. Las situadas en lo profundo de los pliegues se centran en la defensa, fabricando sustancias antimicrobianas, mientras que las más próximas a la superficie se especializan en absorber azúcares, grasas, vitaminas y otros nutrientes. Juntas crean una línea de ensamblaje «zonificada» que mantiene al cuerpo nutrido y protegido. Los autores se propusieron entender cómo contribuye VRAC, un canal iónico sensible al volumen en estas células, a esa división del trabajo, en especial durante la inflamación.
Qué ocurre cuando la puerta falla
Para sondear el papel de VRAC, los investigadores generaron ratones que carecían de su componente clave, LRRC8A, solo en las células del revestimiento intestinal. En condiciones normales estos animales parecían sanos. Pero al exponerse a químicos que imitan la colitis o que promueven el cáncer de colon, perdieron más peso, tuvieron colones más cortos y dañados y desarrollaron más tumores que sus congéneres normales. Sus barreras intestinales se volvieron permeables, las uniones estrechas entre células se alteraron y aumentaron los genes vinculados con la inflamación y las defensas antimicrobianas, mientras que descendieron los genes responsables del transporte de nutrientes y grasas. Eliminar VRAC en células inmunitarias no produjo los mismos efectos, lo que sitúa al revestimiento intestinal como el sitio crítico.
Del abastecimiento al combate
Análisis de célula única y organoides intestinales en miniatura revelaron lo que sucedía dentro del tejido. Sin VRAC, los enterocitos no maduraron correctamente a lo largo del eje de criptas a superficie. Las células asociadas a la captación de nutrientes, especialmente en la superficie, se vieron reducidas, mientras que las células orientadas a la defensa en la base se expandieron. Esta reprogramación perjudicó el manejo de nutrientes: los organoides de ratones deficientes en VRAC absorbieron menos lípidos y glucosa. Una víctima central de este cambio fue el procesamiento de la vitamina A. Las enzimas que convierten la vitamina A dietaria en ácido retinoico —una molécula señalizadora que sostiene la identidad de los enterocitos, la reparación tisular y el equilibrio inmunitario— se redujeron drásticamente, y la actividad global de la retinoide deshidrogenasa cayó.
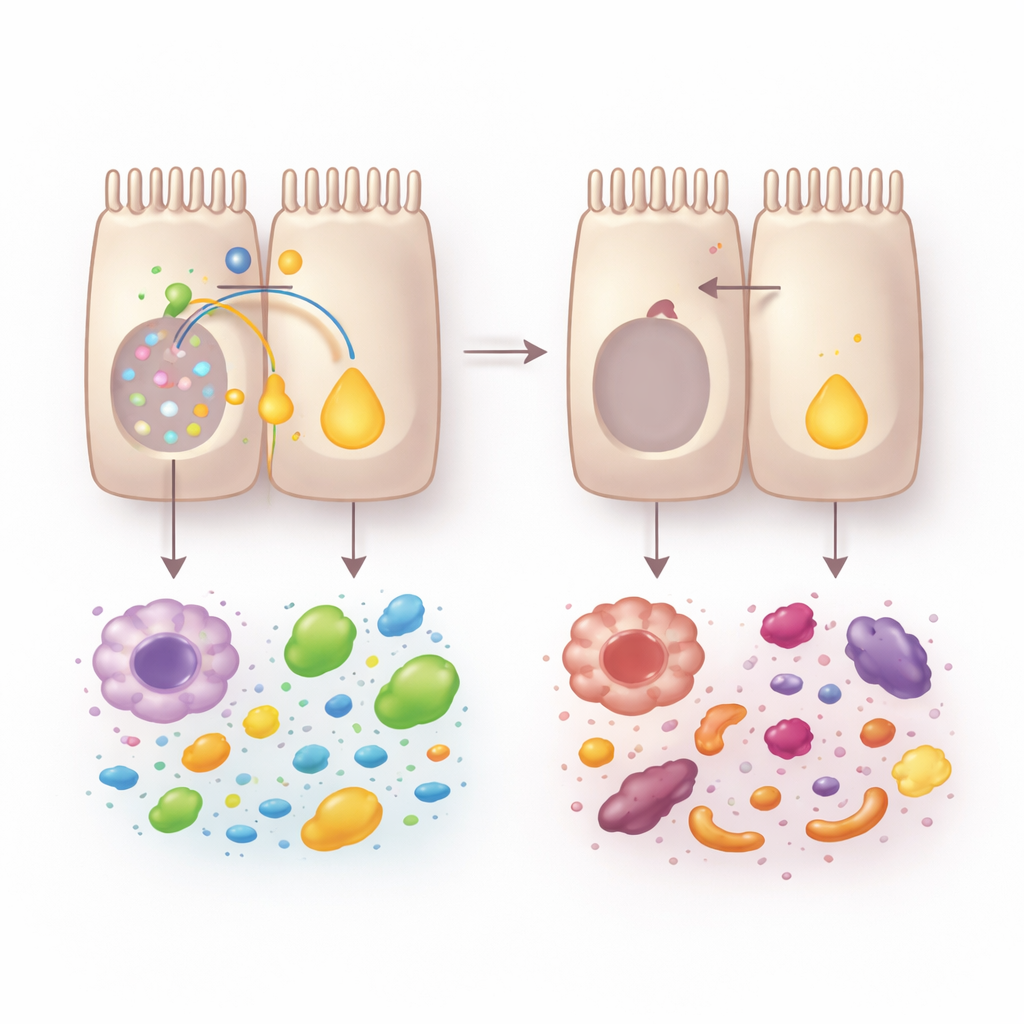
Las señales de vitamina A y los microbios beneficiosos rescatan la situación
Puesto que el ácido retinoico emergió como una vía clave, el equipo probó si restaurarlo podía contrarrestar el daño. Administrar a los ratones ácido retinoico todo-trans antes de inducir colitis redujo la pérdida de peso y el daño colónico, reactivó las enzimas de procesamiento de la vitamina A y mejoró la presencia de enterocitos maduros absorbiendo nutrientes. También restableció células inmunitarias útiles que producen IL-17 e IL-22, moléculas cruciales para reparar el revestimiento intestinal. Al mismo tiempo, la pérdida de VRAC alteró la microbiota: la diversidad disminuyó y las especies beneficiosas de Lactobacillus se redujeron. Estos cambios microbianos resultaron relevantes; igualar la microbiota mediante alojamiento conjunto de los animales o eliminándola con antibióticos borró gran parte de la diferencia entre ratones normales y deficientes en VRAC. Trasplantar heces de ratones deficientes en VRAC a receptores sanos empeoró la colitis, mientras que suplementar con cepas específicas de Lactobacillus potenció el metabolismo de la vitamina A, normalizó los niveles de péptidos antimicrobianos y reactivó las células inmunitarias protectoras.
Qué significa esto para la salud intestinal
En conjunto, el estudio muestra que VRAC en las células del revestimiento intestinal actúa como un reóstato, modulando cuánto esfuerzo invierte el intestino en absorber nutrientes frente a combatir microbios. Cuando falta VRAC, el sistema se bloquea en modo de alta defensa: aumentan la actividad antimicrobiana y la inflamación, disminuyen la absorción de nutrientes y la señalización de la vitamina A, y las bacterias beneficiosas se ven desplazadas. Al restaurar el ácido retinoico o reintroducir Lactobacillus amigables, los investigadores pudieron reequilibrar este sistema y mitigar la enfermedad en ratones. Para personas con afecciones como la enfermedad inflamatoria intestinal, estos hallazgos ponen de relieve los propios canales iónicos del revestimiento intestinal —y sus vínculos con vitaminas derivadas de la dieta y probióticos— como palancas prometedoras para futuras terapias.
Cita: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Palabras clave: enfermedad inflamatoria intestinal, epitelio intestinal, ácido retinoico, microbioma intestinal, probióticos