Clear Sky Science · ru
VRAC координирует компромисс между всасыванием питательных веществ и антимикробной защитой в энтероцитах при воспалении
Почему важно равновесие в кишечнике
Наши кишечники постоянно стоят перед дилеммой: им нужно извлекать питательные вещества из пищи и одновременно отражать нападения вредных микроорганизмов. В этом исследовании изучается, как малоизвестный «ворота» в кишечных клетках, называемый VRAC, помогает регулировать этот компромисс. Когда эти ворота дают сбой, тонкий баланс кишечника смещается в сторону чрезмерной защиты: ухудшаются процессы усвоения питательных веществ, нарушается состав микробиоты и развивается хроническое воспаление, напоминающее воспалительные заболевания кишечника.
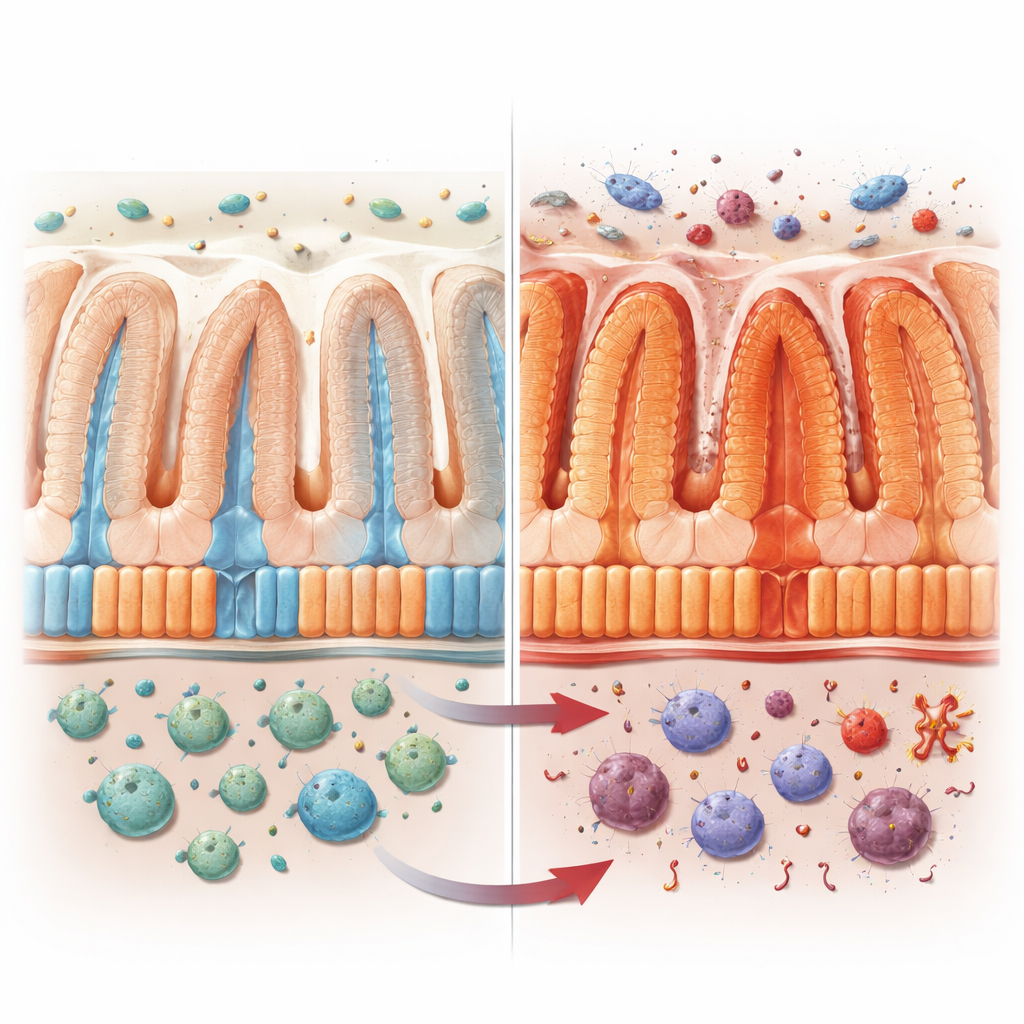
Повседневная работа клеток слизистой
Внутренняя поверхность кишечника выстлана энтероцитами — клетками, формирующими большую часть барьера кишечника. Эти клетки не одинаковы: те, что глубже в криптах, ориентированы на защиту и вырабатывают антимикробные вещества, тогда как клетки ближе к поверхности специализируются на всасывании сахаров, жиров, витаминов и других питательных веществ. Вместе они образуют «зонную» конвейерную систему, которая обеспечивает и питание, и защиту организма. Авторы работы стремились понять, какую роль в этом разделении обязанностей играет VRAC — ионный канал, чувствительный к объему клетки, особенно во время воспаления.
Что происходит, когда ворота ломаются
Чтобы выяснить роль VRAC, исследователи создали мышей с утратой ключевого компонента VRAC, LRRC8A, исключительно в клетках кишечной слизистой. В нормальных условиях эти животные выглядели здоровыми. Но при воздействии химических веществ, моделирующих колит или стимулирующих рак толстой кишки, они теряли больше веса, имели укороченные и более повреждённые ободочные кишки и развивали больше опухолей, чем их нормальные сородичи. Барьер кишечника становился проницаемым, плотные соединения между клетками нарушались, а экспрессия генов, связанных с воспалением и антимикробной защитой, резко возрастала, тогда как гены, отвечающие за транспорт питательных веществ и жиров, снижались. Удаление VRAC из иммунных клеток таких эффектов не вызывало, что указывает на эпителий кишечника как на критическую мишень.
Сдвиг от питания к обороне
Анализ по одной клетке и миниатюрные «кишечные в пробирке» органоиды показали, что происходило внутри ткани. Без VRAC энтероциты не созревали должным образом вдоль оси крипта‑поверхность. Клетки, связанные с усвоением питательных веществ, особенно на поверхности, истощались, тогда как защитно ориентированные клетки у основания расширялись. Эта перестройка ухудшала способность к усвоению: органоиды от VRAC‑дефицитных мышей поглощали меньше липидов и глюкозы. Центральной жертвой этого сдвига стала переработка витамина A. Ферменты, превращающие пищевой витамин A в ретиноевую кислоту — сигнальную молекулу, поддерживающую идентичность энтероцитов, заживление ткани и иммунный баланс — значительно уменьшались, и общая активность ретиновой дегидрогеназы падала.
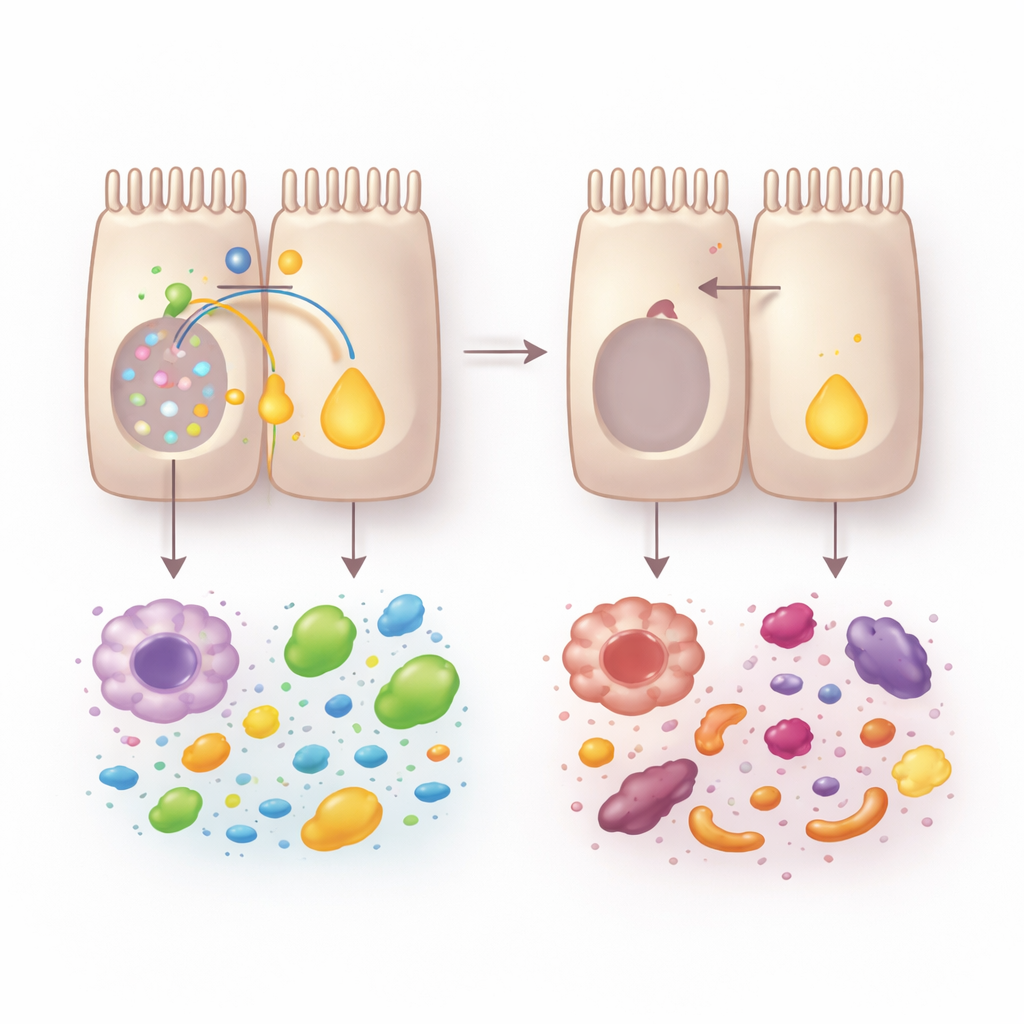
Сигналы витамина A и дружественные микробы в роли спасения
Поскольку ретиноевая кислота выявилась как ключевой путь, команда проверила, может ли её восстановление противостоять повреждениям. Введение всем‑транс ретиноевой кислоты мышам до индукции колита снизило потерю веса и повреждение ободочной кишки, восстановило ферменты, обрабатывающие витамин A, и увеличило число зрелых энтероцитов, всасывающих питательные вещества. Также восстановились полезные иммунные клетки, продуцирующие IL‑17 и IL‑22 — молекулы, важные для восстановления слизистой. В то же время утрата VRAC изменила микробиоту: разнообразие снизилось, а полезные виды Lactobacillus уменьшились. Эти микробные изменения оказались значимыми: выравнивание микробов совместным содержанием в одной клетке или уничтожение их антибиотиками сгладило большую часть различий между нормальными и VRAC‑дефицитными животными. Пересадка кала от VRAC‑дефицитных мышей здоровым реципиентам усугубляла колит, тогда как добавление определённых штаммов Lactobacillus усиливало метаболизм витамина A, нормализовало уровни антимикробных пептидов и восстанавливало защитные иммунные клетки.
Что это значит для здоровья кишечника
В целом исследование показывает, что VRAC в клетках кишечной слизистой действует как реостат, регулируя, сколько усилий кишечник вкладывает в поглощение питательных веществ по сравнению с борьбой с микробами. При отсутствии VRAC система застревает в режиме повышенной защиты: растёт антимикробная активность и воспаление, падают всасывание питательных веществ и сигналы витамина A, а полезные бактерии вытесняются. Восстановление ретиноевой кислоты или возвращение дружественных Lactobacillus позволяло исследователям восстановить равновесие и смягчить болезнь у мышей. Для людей с такими состояниями, как воспалительные заболевания кишечника, эти данные подчёркивают значение собственных ионных каналов слизистой кишечника — и их связей с витаминами из пищи и пробиотиками — как перспективных рычагов для будущих терапий.
Цитирование: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Ключевые слова: воспалительное заболевание кишечника, кишечный эпителий, ретиноиновая кислота, микробиом кишечника, пробиотики