Clear Sky Science · sv
VRAC samordnar kompromissen mellan näringsupptag och antimikrobiellt försvar i enterocyter vid inflammation
Varför tarmens balansakt spelar roll
Våra tarmar står inför ett ständigt dilemma: de måste suga upp näring från maten samtidigt som de försvarar sig mot skadliga mikrober. Denna studie undersöker hur en lite känd grind i tarmcellerna, kallad VRAC, hjälper till att hantera den kompromissen. När denna grind fungerar dåligt tippar tarmens känsliga balans mot överdrivet försvar, försämrad näringshantering, rubbat mikrobiota och kronisk inflammation liknande inflammatorisk tarmsjukdom.
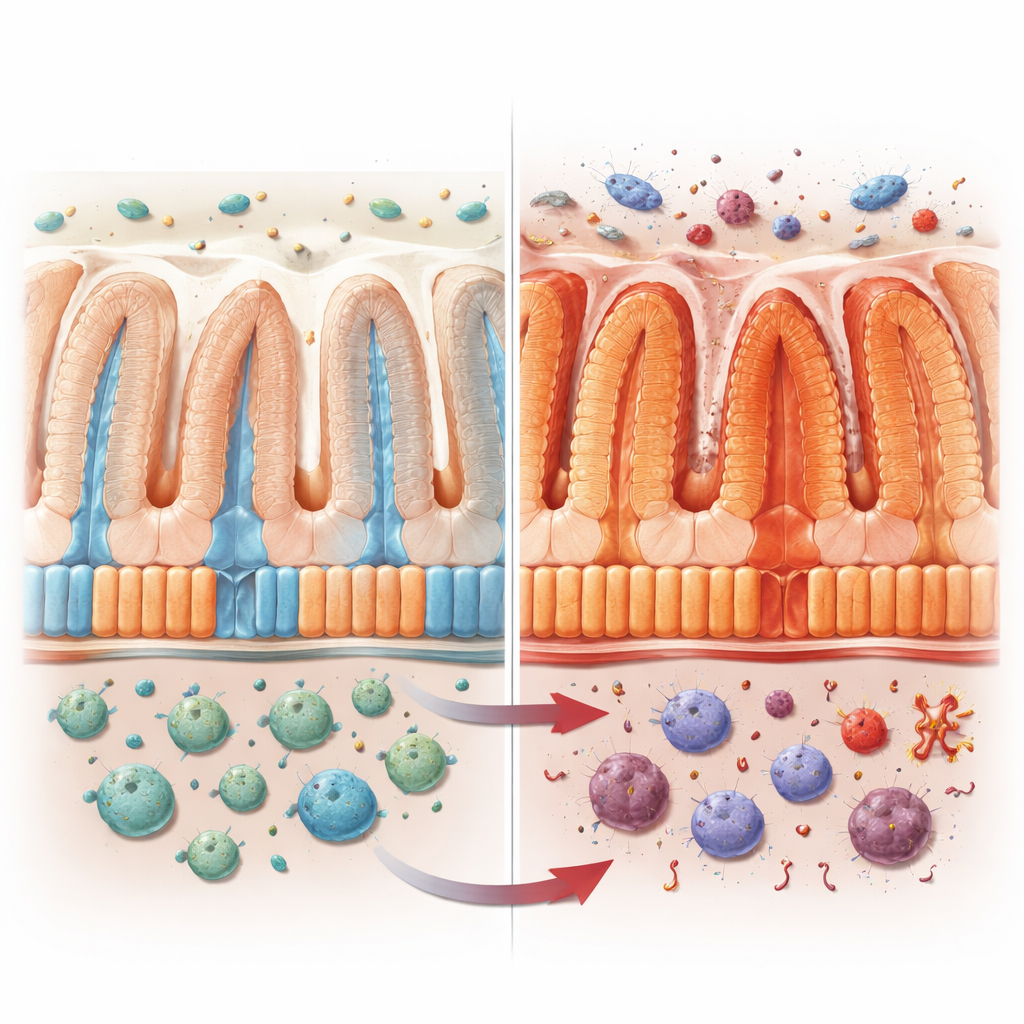
Tarmens dagliga arbete
Den inre ytan av tarmen är täckt av enterocyter, celler som bygger upp större delen av tarmbarriären. Dessa celler är inte alla likadana. De som sitter djupt i vecken fokuserar på försvar och producerar antimikrobiella substanser, medan de närmare ytan specialiserar sig på att absorbera socker, fett, vitaminer och andra näringsämnen. Tillsammans skapar de ett ”zonat” löpande band som håller kroppen både närd och skyddad. Författarna ville förstå hur VRAC, en volymsensorisk jonkanal i dessa celler, bidrar till denna arbetsfördelning, särskilt under inflammation.
Vad som händer när grinden fallerar
För att undersöka VRAC:s roll konstruerade forskarna möss som saknade dess nyckelkomponent, LRRC8A, endast i tarmens epitelceller. Under normala förhållanden såg dessa djur friska ut. Men när de utsattes för kemikalier som efterliknar kolit eller driver koloncancer förlorade de mer vikt, fick kortare och mer skadade kolon och utvecklade fler tumörer än sina normala kullsyskon. Deras tarmbarriärer läckte, täta junctions mellan cellerna stördes, och gener kopplade till inflammation och antimikrobiellt försvar ökade, medan gener för närings- och fetttransport minskade. Att ta bort VRAC från immunceller gav inte samma effekter, vilket pekar på tarmepitelet som den kritiska platsen.
Från födointag till strid
Encellsanalyser och små ”tarm-i-skål” organoider avslöjade vad som skedde i vävnaden. Utan VRAC mognade inte enterocyterna korrekt längs från krypta till yta. Celler kopplade till näringsupptag, särskilt vid ytan, minskade, medan försvarsorienterade celler vid basen ökade. Denna omsättning skadade näringshanteringen: organoider från VRAC-defekta möss absorberade mindre lipid och glukos. Ett centralt offer för denna förskjutning var vitamin A-omsättningen. Enzymer som omvandlar dietärt vitamin A till retinolsyra — en signalmolekyl som stöder enterocytidentitet, vävnadsreparation och immunbalans — minskade kraftigt, och den övergripande retinoaldehyddehydrogenasaktiviteten föll.
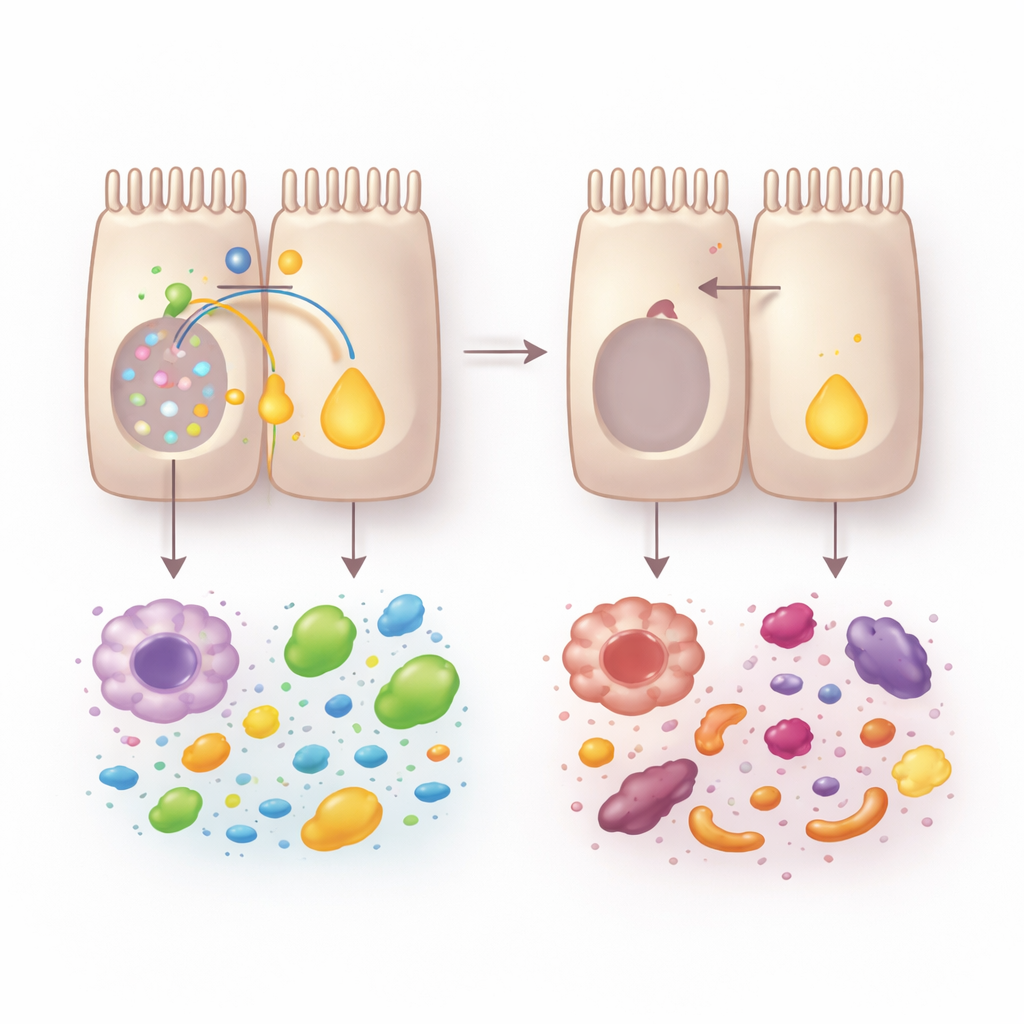
Vitamin A‑signalering och vänliga mikrober som räddning
Eftersom retinolsyra framträdde som en nyckelväg testade teamet om återställning av denna kunde motverka skadorna. Att ge mössen all-trans retinolsyra före kolit minskade viktnedgång och skador på kolon, återupplivade enzymer för vitamin A‑bearbetning och förbättrade förekomsten av mogna näringsabsorberande enterocyter. Det återställde också hjälpsamma immunceller som producerar IL-17 och IL-22, molekyler viktiga för att reparera tarmens yta. Samtidigt förändrade förlusten av VRAC mikrobiotan: diversiteten minskade och gynnsamma Lactobacillus‑arter sjönk. Dessa mikrobiella förändringar visade sig vara betydelsefulla; att utjämna mikrobiotan genom att sambo mjöss eller rensa den med antibiotika suddade ut mycket av skillnaden mellan normala och VRAC‑defekta djur. Att transplantera avföring från VRAC‑defekta möss till friska mottagare förvärrade kolit, medan tillskott av specifika Lactobacillus‑stammar ökade vitamin A‑metabolismen, normaliserade nivåer av antimikrobiella peptider och återupplivade skyddande immunceller.
Vad detta betyder för tarmhälsa
Sammanfattningsvis visar studien att VRAC i tarmepitelceller fungerar som en dimmer, som ställer in hur mycket resurser tarmen satsar på att absorbera näring kontra att bekämpa mikrober. När VRAC saknas låser sig systemet i ett högt försvarsläge: antimikrobiell aktivitet och inflammation ökar, näringsupptag och vitamin A‑signalering minskar, och gynnsamma bakterier trängs ut. Genom att återställa retinolsyra eller återintroducera vänliga Lactobacillus kunde forskarna återbalansera systemet och lindra sjukdomen hos möss. För människor med tillstånd som inflammatorisk tarmsjukdom lyfter dessa fynd fram tarmepitelets egna jonkanaler — och deras kopplingar till kostbaserade vitaminer och probiotika — som lovande verktyg för framtida terapier.
Citering: Yi, X., Zhang, S., Gu, X. et al. VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation. Nat Commun 17, 3146 (2026). https://doi.org/10.1038/s41467-026-69963-3
Nyckelord: inflammatorisk tarmsjukdom, intestinalt epitel, retinolsyra, tarmmikrobiom, probiotika